Dichlormid
Dichlormid ist ein von Stauffer Chemical entwickelter und 1972 eingeführter[3] Herbizid-Safener. Heute wird er von AstraZeneca vertrieben.[4]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
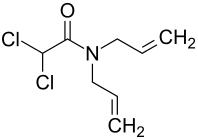 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Dichlormid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H11Cl2NO | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 208,09 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
130 °C (1,3 mPa)[1] | ||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (5 mg·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Dichlormid kann durch Reaktion von Dichloracetylchlorid und Diallylamin gewonnen werden.[5]
Verwendung
Dichlormid verstärkt die Verträglichkeit von Thiocarbamat- und Chloracetamid-Herbiziden gegenüber der Anbaukultur durch Erhöhung der Glutathion-S-Transferase-Aktivität. Dadurch wird der Abbau des Herbizids zu Glutathion-Konjugaten beschleunigt.[1] Andere Forscher haben festgestellt, dass Dichlormid die Inhibierung der Lipid-Biosynthese durch EPTC rückgängig macht.[3]
Es wird in Kombination mit dem Herbizid zur Unkrautbekämpfung vor allem in Mais eingesetzt.[1]
Zulassung
Da Acetochlor in der EU nicht zugelassen ist, wird auch Dichlormid hier nicht verwendet.
Einzelnachweise
- Eintrag zu Dichlormid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 21. März 2014.
- Datenblatt Dichlormid bei Sigma-Aldrich, abgerufen am 21. Mai 2017 (PDF).
- Aqel W Abu-Qare, Harry J Duncan: Herbicide safeners: uses, limitations, metabolism, and mechanisms of action. In: Chemosphere. Band 48, Nr. 9, September 2002, S. 965–974, doi:10.1016/S0045-6535(02)00185-6 (iranarticles.com [PDF]).
- AstraZeneca and its genetic research - Feeding the world or fuelling hunger? S. 18.
- Thomas A. Unger: Pesticide Synthesis Handbook. William Andrew, 1996, ISBN 0-8155-1853-6, S. 17 (eingeschränkte Vorschau in der Google-Buchsuche).
