Dexibuprofen
Dexibuprofen ist ein Arzneistoff aus der Gruppe der nichtsteroidalen Antiphlogistika (NSAR) zur Behandlung von Schmerzen und Entzündungen. Es handelt sich um das pharmakologisch wirksame (S)-Enantiomer des Racemats Ibuprofen und wurde 1996 erstmals patentiert. Die Wirkung beruht auf der Hemmung der Cyclooxygenasen (COX).
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
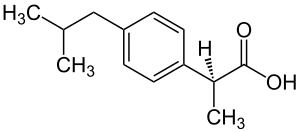 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Dexibuprofen | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C13H18O2 | |||||||||||||||||||||
| Kurzbeschreibung |
weiße Kristalle[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
M01AE14 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 206,28 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Da es etwa doppelt so wirksam sein soll, kommt man mit einer geringeren Arzneistoffmenge pro Tablette aus. Außerdem setzt die Wirkung dieses Schmerzmittels etwas schneller ein als beim Racemat Ibuprofen.
Da die körpereigene 2-Arylpropionyl-CoA-epimerase das Dexibuprofen zum Ibuprofen racemisieren kann, sind die therapeutischen Vorteile von Dexibuprofen gegenüber Ibuprofen umstritten. Aufgrund der niedrigeren Dosierung von Dexibuprofen gegenüber Ibuprofen können einerseits weniger Nebenwirkungen erwartet werden,[3] andererseits war in einer Studie an 178 Patienten mit Hüftgelenksarthrose die Nebenwirkungsrate von Dexibuprofen in etwa gleich wie die der doppelten Dosis der racemischen Form.[4]
Arzneimittelmarkt
Dexibuprofen ist seit 1993 in Österreich (Seractil)[5] und seit 2001 in Deutschland[6] (Deltaran)[7] zugelassen. In der Schweiz wurde Dexibuprofen 2001 im Markt eingeführt (Seractil).[8]
Weitere Präparatenamen in D-A-CH sind Atriscal (A), DexOptifen (CH), Eu-Med (A), Monactil (A), Movone (A), außerdem gibt es Generika.
Mit der 20. Verordnung zur Änderung der Arzneimittel-Verschreibungsverordnung wurde Dexibuprofen in Deutschland teilweise aus der Verschreibungspflicht entlassen,[9][10] jedoch gibt es Stand Februar 2022 noch keine Fertigarzneimittel die den nötigen Anforderungen für die rezeptfreie Abgabe entsprechen.[9]
Einzelnachweise
- Datenblatt Dexibuprofen bei Acros, abgerufen am 20. Februar 2010.
- Datenblatt (S)-(+)-Ibuprofen bei Sigma-Aldrich, abgerufen am 24. März 2011 (PDF).
- Paul F. White (2003): Can the Use of Specific Isomers Improve the Safety and Efficacy of Nonsteroidal Antiinflammatory Drugs? In: Anesth Analg. 97(2): S. 309–310; PMID 12873909.
- Dexibuprofen in der Rubrik «Arzneistoffe» der Pharmazeutischen Zeitung (05|20001), in: Pharmazeutische Zeitung Online, GOVI-Verlag, Stand: 19. April 2017. Abgerufen am 25. Februar 2022.
- Arzneispezialitätenregister der AGES, Betreiber/Herausgeber: BASG, Wien. Abgerufen am 25. Februar 2022.
- Antrag an den Sachverständigen-Ausschuss für Verschreibungspflicht des Bundesinstituts für Arzneimittel und Medizinprodukte auf Freistellung von der Verschreibungspflicht von Dexibuprofen (PDF), 13. Juli 2021; www.bfarm.de. Abgerufen am 25. Februar 2022.
- Arzneiverordnung in der Praxis, Ausgabe 1/2002 (PDF; 309 kB), Arzneimittelkommission der deutschen Ärzteschaft (AKDÄ).
- Gebro Pharma > Unternehmen > Milestones, Website der Gebro Pharma (Originator). Abgerufen am 25. Februar 2022.
- D. Hüttemann: Weg frei für mehrere neue OTC, www.pharmazeutische-zeitung.de, 14. Februar 2022.
- Bundesrat Drucksache 857/21 vom 29.12.21. Verordnung des Bundesministeriums für Gesundheit: Zwanzigste Verordnung zur Änderung der Arzneimittelverschreibungsverordnung (PDF; 1,8 MB). www.bundesrat.de, abgerufen am 25. Februar 2022.