Desloratadin
Desloratadin ist ein Arzneistoff aus der Gruppe der Antihistaminika, der zur Behandlung der allergischen Rhinitis und chronischen Urtikaria eingesetzt wird.[2] Desloratadin ist ein Abkömmling und Metabolit des Antihistaminikums Loratadin und wurde von dem Pharmaunternehmen Essex Pharma mit dem Auslaufen des Patentschutzes für Loratadin auf den Markt gebracht. Desloratadin unterlag bis 21. Februar 2020 in Deutschland der ärztlichen Verschreibungspflicht, dann wurde es ein Rezeptfreies Medikament (sog. OTC-Medikament, durch einen sog. OTC-Switch aus der Rezeptpflicht genommen).
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
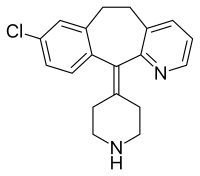 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Desloratadin | ||||||||||||||||||
| Andere Namen |
8-Chlor-11-(piperidin-4-yliden)-5,6-dihydro-11H-benzo[5,6]cyclohepta[1,2-b]pyridin (IUPAC) | ||||||||||||||||||
| Summenformel | C19H19ClN2 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code |
R06AX27 | ||||||||||||||||||
| Wirkstoffklasse | |||||||||||||||||||
| Wirkmechanismus | |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 310,82 g·mol−1 | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Außerhalb von Deutschland zugelassene Tabletten bleiben rezeptpflichtig.[3][4]
Wirkmechanismus
Der Wirkmechanismus Desloratadins entspricht dem Loratadins, als H1-Antihistaminikum blockiert es die speziellen Bindungsstellen für Histamin, die Histamin-H1-Rezeptoren, und hemmt somit die Histaminwirkungen (z. B. Hautrötung, Juckreiz, Blutdruckabfall und Bronchospasmen); weiterhin stabilisiert Desloratadin aber auch die Mastzellen, wodurch die Freisetzung von Histamin blockiert wird. Desloratadin wirkt zudem als FIASMA (funktioneller Hemmer der sauren Sphingomyelinase).[5]
Vergleich mit Loratadin
Im Unterschied zu Loratadin hat Desloratadin eine drei- bis vierfach höhere Affinität zum H1-Rezeptor. Daher kann Loratadin formal als Prodrug des Desloratadins angesehen werden. Darüber hinaus hat Desloratadin eine längere Plasmahalbwertszeit. Gemeinsam ist beiden Substanzen die Eigenschaft, dass an der Blut-Hirn-Schranke ein Rücktransport durch permeable Glykoproteine erfolgt,[6] sodass sowohl Loratadin als auch Desloratadin nur begrenzt in das Zentralnervensystem gelangen und dort weniger Nebenwirkungen wie z. B. Schläfrigkeit (Sedierung) verursachen können. Sie zählen daher beide zu den Antihistaminika der zweiten Generation.
Ein therapeutischer Vorteil von Desloratadin wird als marginal eingestuft, da auch Loratadin in der Leber nahezu vollständig in Desloratadin umgewandelt wird.[7] Die zeitliche Nähe zwischen dem Wegfall des Patentschutzes für Loratadin und der Markteinführung von Desloratadin legt nahe, dass auch dies ein Grund für dessen Einführung war.[8]
Handelsnamen
Aerius (D, A, CH, I, BG), Dasselta (D, A), Azomyr (A), Neoclarityn (A), LoranoPro (D), Desloratadin-ratiopharm (D), Desloratadin-Denk (D), Deslora-Denk (D)
Weblinks
Einzelnachweise
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von 13-chloro-2-(piperidin-4-ylidene)-4-azatricyclo[9.4.0.0³,⁸]pentadeca-1(15),3,5,7,11,13-hexaene im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 15. Januar 2020.
- Chronisch idiopathische Urtikaria: Desloratadin stoppt juckende Quaddeln, www.deutsche-apotheker-zeitung.de, 17. November 2002.
- Gesamte Rechtsvorschrift für Rezeptpflichtverordnung. Rechtsinformationssystem des Bundes. 23. Oktober 2014. Abgerufen am 12. April 2016.
- Verordnung über die Verschreibungspflicht von Arzneimitteln. Bundesministerium der Justiz und für Verbraucherschutz & juris GmbH. 30. November 2015. Abgerufen am 12. April 2016.
- Kornhuber J, Muehlbacher M, Trapp S, Pechmann S, Friedl A, Reichel M, Mühle C, Terfloth L, Groemer T, Spitzer G, Liedl K, Gulbins E, Tripal P: Identification of novel functional inhibitors of acid sphingomyelinase. In: PLoS ONE. 6, Nr. 8, 2011, S. e23852. doi:10.1371/journal.pone.0023852.
- https://www.ncbi.nlm.nih.gov/pubmed/?term=P-GLYCOPROTEIN+LIMITS+THE+BRAIN+PENETRATION+OF+NONSEDATING+BUT+NOT+SEDATING+H1-ANTAGONISTS
- Ulrich Schwabe, Dieter Paffrath: Arzneiverordnungs-Report 2004: Aktuelle Daten, Kosten, Trends und Kommentare. Springer, 2004, ISBN 3540213597.
- Antje-Christina Raasch: Strategie und Erfolgsfaktoren beim Patentauslauf des Antihistaminikums Lisino von essex pharma. In: Der Patentauslauf von Pharmazeutika als Herausforderung beim Management des Produktlebenszyklus. Springer, 2006, ISBN 978-3-8350-0632-4, S. 211–225.
- Rote Liste Online, Stand: August 2009.
- AM-Komp. d. Schweiz, Stand: August 2009.
- AGES-PharmMed, Stand: August 2009.