Dehydroascorbinsäure
Dehydroascorbinsäure (englisch dehydro ascorbic acid, DHA) ist eine chemische Verbindung aus der Gruppe der Ascorbinsäurederivate.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
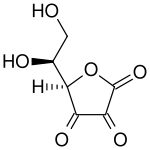 | ||||||||||||||||||||||
| L-Isomer von Dehydroascorbinsäure | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Dehydroascorbinsäure | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C6H6O6 | |||||||||||||||||||||
| Kurzbeschreibung |
beiger Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 174,11 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Biologische Funktion
Dehydroascorbinsäure (auch L-Dehydroascorbinsäure genannt) entsteht durch Oxidation von Ascorbinsäure. Im menschlichen Metabolismus kann sie zu L-Ascorbinsäure reduziert werden und damit Vitamin C regenerieren.[3] Die Oxidation der Ascorbinsäure zu Dehydroascorbinsäure erfolgt in vielen Geweben, die Rückverwandlung der Dehydroascorbinsäure in Ascorbinsäure scheint dagegen vorwiegend in der Leber zu erfolgen.[4]
Generell wird Vitamin C in Form von DHA durch Glucosetransporter, hauptsächlich GLUT-1, in die Mitochondrien der Zellen transportiert, da nur sehr wenige Zellen über spezifische Vitamin-C-Transporter verfügen.[5] Hierbei sind die meisten dieser Transporter Natriumionen-abhängig. Insbesondere das Gehirn ist auf eine Versorgung mit Ascorbinsäure angewiesen, das Vitamin kann jedoch nicht die Blut-Hirn-Schranke passieren.[6] Dieses Problem wird dadurch umgangen, dass Dehydroascorbinsäure durch Glucosetransporter, zum Beispiel GLUT1, durch die Schranke transportiert und in den Gehirnzellen zu Ascorbinsäure reduziert wird.
Es wird davon ausgegangen, dass Ascorbinsäure in Form von DHA intrazellulär transportiert wird. Hierbei soll extrazelluläre Ascorbinsäure zu DHA oxidiert, in die Zelle aufgenommen und dann wieder reduziert werden, da Ascorbinsäure selbst die Zelle nicht verlassen kann.[7] DHA ist instabiler als L-Ascorbinsäure. Je nach Reaktionsbedingungen (pH-Wert, An- beziehungsweise Abwesenheit von Reduktionsmitteln wie Glutathion) kann es entweder wieder zurück in Ascorbinsäure umgewandelt werden oder zu Diketogulonsäure (DKG) irreversibel hydrolysieren.[8][9]
Gewinnung
Reine Dehydroascorbinsäure kann durch Oxidation von Ascorbinsäure mit Sauerstoff in Methanol mit Hilfe eines Katalysators gewonnen werden.[10]
Eigenschaften
L-Dehydroascorbinsäure ist ein beiger Feststoff. Er liegt im festen Zustand als Dimer vor und wird in Lösung zum Monomer.[1] Dehydroascorbinsäure liegt in wässrigen Lösungen nahezu vollständig als Monohydrat (mono-DHA·H2O) vor. Dabei bildet es einen Bizyklus, was durch Kernspinresonanzspektroskopie nachgewiesen wurde. Möglicherweise kann es noch ein zweites Molekül Wasser aufnehmen, um dann ein Dihydrat auszubilden.[11] Auch Semi-Dehydroascorbinsäure sowie oxidierte Formen veresterter Ascorbinsäuren werden zur Gruppe der Dehydroascorbinsäure gezählt.
Einzelnachweise
- Datenblatt (L)-Dehydroascorbic acid bei Sigma-Aldrich, abgerufen am 4. Mai 2017 (PDF).
- Peter M. Collins: Dictionary of Carbohydrates. CRC Press, 2005, ISBN 978-0-8493-7765-5, S. 281 (eingeschränkte Vorschau in der Google-Buchsuche).
- Hartmut Dunkelberg, Thomas Gebel, Andrea Hartwig: Vitamine und Spurenelemente Bedarf, Mangel, Hypervitaminosen und Nahrungsergänzung. John Wiley & Sons, 2013, ISBN 978-3-527-65307-2, S. 78 (eingeschränkte Vorschau in der Google-Buchsuche).
- Lohmann: Der Stoffwechsel Zweiter Teil. Springer-Verlag, 2013, ISBN 978-3-662-21764-1, S. 383 (eingeschränkte Vorschau in der Google-Buchsuche).
- K. C. Sagun u. a.: Vitamin C enters mitochondria via facilitative glucose transporter 1 (Glut1) and confers mitochondrial protection against oxidative injury. In: FASEB Journal. 2005, 19 (12), S. 1657–1667, PMID 16195374 (PDF, freier Volltextzugriff).
- J. Huang u. a.: Dehydroascorbic acid, a blood-brain barrier transportable form of vitamin C, mediates potent cerebroprotection in experimental stroke. In: PNAS. 2001, 98, Nr. 20, S. 11720–11724, PMID 11573006 (PDF, freier Volltextzugriff).
- C. S. Tsao: An overview of ascorbic acid chemistry and biochemistry. In: Lester Packer, Jürgen Fuchs: Vitamin C in Health and Disease. Marcel Dekker Inc illustrated edition 1997, ISBN 0-8247-9313-7, S. 25–58.
- Y. Nishikawa und T. Kurata: Interconversion between dehydro-L-ascorbic acid and L-ascorbic acid. In: Bioscience, Biotechnology, and Biochemistry. 2000, 64 Nr. 3, S. 476–483, PMID 10803943, doi:10.1271/bbb.64.476, PDF (Memento vom 19. Dezember 2014 im Internet Archive), freier Volltextzugriff.
- Y. Nishikawa u. a: Identification of 3,4-dihydroxy-2-oxo-butanal (L-threosone) as an intermediate compound in oxidative degradation of dehydro-L-ascorbic acid and 2,3-diketo-L-gulonic acid in a deuterium oxide phosphate buffer. In: Bioscience, Biotechnology, and Biochemistry. 2001, 65, Nr. 8, S. 1707–1712, PMID 11577707, doi:10.1271/bbb.65.1707, PDF (Memento vom 19. Dezember 2014 im Internet Archive), freier Volltextzugriff.
- Wilhelm Friedrich: Vitamins. Walter de Gruyter, 1988, ISBN 978-3-11-010244-4, S. 936 (eingeschränkte Vorschau in der Google-Buchsuche).
- W. Bors und G. R. Buettner: The vitamin C radical and its reactions. In: Lester Packer, Jürgen Fuchs: Vitamin C in Health and Disease. Marcel Dekker Inc illustrated edition 1997, ISBN 0-8247-9313-7, S. 76.