Coniferylaldehyd
Coniferylaldehyd ist eine chemische Verbindung aus der Gruppe der Aldehyde.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
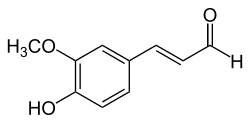 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Coniferylaldehyd | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C10H10O3 | ||||||||||||||||||
| Kurzbeschreibung |
gelboranger Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 178,18 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
1,156 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
175 °C (7 hPa)[1] | ||||||||||||||||||
| Löslichkeit |
löslich in Benzol und Ethanol[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Vorkommen
Coniferylaldehyd kommt natürlich als Bestandteil des Lignins vieler Pflanzen vor, was schon 1897 durch P. Klason angenommen wurde.[3][4]
Gewinnung und Darstellung
Coniferylaldehyd kann aus Methoxymethylvanillin gewonnen werden, das mit Acetaldehyd kondensiert und durch Säure von der Methoxymethyl-Gruppe befreit wird.[5] Es kann auch biochemisch (z. B. durch Cinnamoyl:CoA-Reduktase) dargestellt werden.[6]
Eigenschaften
Coniferylaldehyd ist ein gelboranger Feststoff,[1] der löslich in Benzol und Ethanol ist.[2]
Verwendung
Coniferylaldehyd eignet sich zur Verwendung in Studien über die antioxidativen und antiradikalischen Aktivitäten von Ferulaten unter Verwendung eines β-Carotin-Linoleat-Modellsystems bzw. eines DPPH-Radikalfängertests.[1]
Einzelnachweise
- Datenblatt Coniferylaldehyd, 98% bei Sigma-Aldrich, abgerufen am 6. November 2016 (PDF).
- Lide: CRC Handbook 87. Edition. CRC Press, 1998, ISBN 978-0-8493-0594-8, S. 648 (eingeschränkte Vorschau in der Google-Buchsuche).
- Paul Walden, Carl Graebe: Geschichte der organischen Chemie seit 1880. Springer-Verlag, 2013, ISBN 978-3-662-28693-7, S. 686 (eingeschränkte Vorschau in der Google-Buchsuche).
- Friedrich Emil Brauns, Dorothy Alexandra Brauns: The Chemistry of Lignin Covering the Literature for the Years 1949–1958. Elsevier, 2013, ISBN 978-1-4832-7595-6, S. 43 (eingeschränkte Vorschau in der Google-Buchsuche).
- Karl Freudenberg, Rösel Dillenburg: Coniferylaldehyd und Sinapinalkohol. In: Chemische Berichte. 84, 1951, S. 67, doi:10.1002/cber.19510840110.
- google.com: Patent EP0845532A2 – Syntheseenzyme für die Herstellung von Coniferylalkohol, Coniferylaldehyd … – Google Patente, abgerufen am 6. November 2016
