Benzylkalium
Benzylkalium ist eine Organokaliumverbindung mit der Summenformel C7H7K, die als luftempfindlicher, oranger Feststoff vorliegt. Wie fast alle Alkaliorganyle ist Benzylkalium hochreaktiv, sodass es sich in koordinierenden Lösungsmitteln wie Ethern und Aminen im Gegensatz zu Kohlenwasserstoffen langsam zersetzt.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
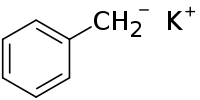 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Benzylkalium | ||||||||||||
| Summenformel | C7H7K | ||||||||||||
| Kurzbeschreibung |
rot-oranger Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 130,32 g·mol−1 | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Synthese
Eine frühe Synthese folgt einer zweistufigen Transmetallierung über p-Tolylkalium:[3]
Modernere synthetische Ansätze sind die Reaktion von Butyllithium mit Kalium-tert-butanolat und Toluol[1] oder der Reaktion von Toluol mit Kalium in der Gegenwart von Hexamethyldistannan[4].
Verwendung

Am häufigsten findet Benzylkalium wahrscheinlich als starke Base zur Herstellung von Kaliumsalzen Einsatz.[5][6] Auch Imidazoliumsalze können mittels Benzylkalium zu Carbenen deprotoniert werden.[7]
Obwohl für diese Zwecke in der Regel auch Kaliumhydrid eingesetzt werden kann, hat Benzylkalium den Vorteil, dass es molekular und nicht ionisch vorliegt und daher schneller reagiert.
Einzelnachweise
- L. Lochmann, J. Trekoval: Lithium-potassium exchange in alkyllithium/potassium t-pentoxide systems. In: Journal of Organometallic Chemistry. Band 326, Nr. 1, Mai 1987, S. 1–7, doi:10.1016/0022-328X(87)80117-1.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Henry Gilman, Henry A. Pacevitz, Ogden Baine: Benzylalkali Compounds 1. In: Journal of the American Chemical Society. Band 62, Nr. 6, 1. Juni 1940, S. 1514–1520, doi:10.1021/ja01863a054.
- Matthias Westerhausen, Wolfgang Schwarz: Neuartige Synthese und Molekülstruktur von Benzylkalium (thf) [KCH2C6H5]2 / Novel Synthesis and Molecular Structure of Benzyl Potassium (thf)[KCH2C6H5]2. In: Zeitschrift für Naturforschung B. 53, 1998, S. 625 (online). doi:10.1515/znb-1998-5-620
- Jacob B. Geri, Michael M. Wade Wolfe, Nathaniel K. Szymczak: The Difluoromethyl Group as a Masked Nucleophile: A Lewis Acid/Base Approach. In: Journal of the American Chemical Society. Band 140, Nr. 30, August 2018, S. 9404–9408, doi:10.1021/jacs.8b06093.
- Ryan J. Roberts, Nicolas Bélanger-Desmarais, Christian Reber, Daniel B. Leznoff: The luminescence properties of linear vs. kinked aurophilic 1-D chains of bis(dithiocarbamato)gold(i) dimers. In: Chemical Communications. Band 50, Nr. 24, 2014, S. 3148, doi:10.1039/c3cc47944g.
- Martin Niehues, Gerald Kehr, Roland Fröhlich, Gerhard Erker: Generation and Structural Characterization of an [(Imidazol-2-ylidene)HfCl5]-Anion/Imidazolium Cation Salt. In: Zeitschrift für Naturforschung B. 58, 2003, S. 1005–1008 (PDF, freier Volltext). doi:10.1515/znb-2003-1011