Benzoin-Addition
Die Benzoin-Addition (häufig, aber fälschlicherweise auch als Benzoin-Kondensation bezeichnet) ist die Addition von meist aromatischen Aldehyden, insbesondere Benzaldehyd, unter Cyanid-Katalyse zu aromatischen α-Hydroxyketonen (Benzoin). Der Mechanismus wurde bereits 1903 von Arthur Lapworth vorgeschlagen. Dargestellt wird die Reaktion am Beispiel der Reaktion zweier Moleküle Benzaldehyd zu Benzoin.
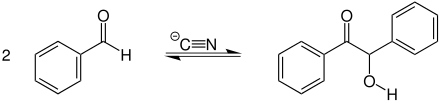 Übersichtsreaktion zur Benzoin-Addition
Übersichtsreaktion zur Benzoin-Addition
Mechanismus
Der Mechanismus der Reaktion wird ebenfalls an dem obigen Beispiel erläutert:
 Mechanismus der Benzoin-Addition
Mechanismus der Benzoin-Addition
In einem ersten Schritt erfolgt durch das Cyanid-Ion eine Umpolung des Carbonylkohlenstoffes am Benzaldehyd (1). Durch Anlagerung des Cyanidions an die Carbonylgruppe entsteht das Anion des entsprechenden Cyanhydrins. Aus diesem wird durch Übertragung des Protons vom Kohlenstoff zum Sauerstoff das tautomere Carbanion 2 gebildet, welches nun nukleophil ein weiteres Benzaldehyd angreift. Unter einem intramolekularen Protonentransfer und Abspaltung des Cyanids aus Molekül 3 wird das Produkt Benzoin (4) gebildet. Die Reaktion ist reversibel.[1] Das Cyanid ist dabei ein sehr spezifischer Katalysator. Es erleichtert durch seinen −I-Effekt die Wanderung des Protons vom Kohlenstoff- zum Sauerstoffatom und ermöglicht dadurch die nukleophile Addition des zweiten Aldehydmoleküls.
Die beiden Aldehydmoleküle haben verschiedene Rollen. Der Aldehyd, der sein Proton abgibt, wird als Donor, derjenige, der es aufnimmt, als Akzeptor bezeichnet. Einige Aldehyde können nur als Donor fungieren (z. B. 4-Dimethylaminobenzaldehyd), andere können beide Rollen übernehmen (z. B. Benzaldehyd). Dies ermöglicht die gezielte Synthese einiger unsymmetrischer Benzoine.
Die Reaktion kann durch die Verwendung bestimmter Thiazoliumsalze in basischem Milieu auch auf aliphatische Aldehyde und Gemische aus aliphatischen und (hetero)aromatischen Aldehyden ausgedehnt werden. Der Mechanismus ist im Wesentlichen dem obigen analog.
Die bei diesen Reaktionen erhaltenen α-Hydroxyketone werden auch als Acyloine bezeichnet und sind wichtige Ausgangsstoffe für weitergehende Synthesen, insbesondere von heterocyclischen Verbindungen.
Die Addition kann auch an α,β-ungesättigte Ketone (z. B. Methylvinylketon) erfolgen. Diese Variante wird als Stetter-Reaktion bezeichnet.
Das im Organismus vorkommende, dort für die Synthese von Acyloinen zuständige, Coenzym Thiamin enthält gleichermaßen ein solches Thiazoliumsalz.
Einzelnachweise
- H. Beyer, W. Walter, W. Francke: Lehrbuch der Organischen Chemie. 23. Auflage, S. Hirzel Verlag, Stuttgart, Leipzig 1998, ISBN 978-3-7776-0808-2.