Ammoniumhexachloroiridat
Ammoniumhexachloroiridat ist eine anorganische chemische Verbindung aus der Gruppe der Ammoniumverbindungen und Hexachloroiridate.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
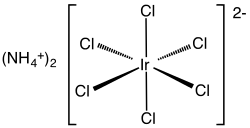 | ||||||||||
| Allgemeines | ||||||||||
| Name | Ammoniumhexachloroiridat | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | (NH4)2[IrCl6] | |||||||||
| Kurzbeschreibung |
schwarzroter bis schwarzer Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 441,01 g·mol−1 | |||||||||
| Aggregatzustand |
fest[2] | |||||||||
| Dichte |
2,86 g·cm−3 (25 °C)[2] | |||||||||
| Schmelzpunkt |
Zersetzung ab 200 °C[1] | |||||||||
| Löslichkeit |
wenig löslich in Wasser[3] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Ammoniumhexachloroiridat kann durch Reaktion einer Lösung von Dinatriumhexachloroiridat in Königswasser mit Ammoniumchlorid gewonnen werden.[3]
Eigenschaften
Ammoniumhexachloroiridat liegt in Form schwarzroter bis schwarze Oktaeder vor, die wenig löslich in Wasser sind. Oberhalb von 200 °C zersetzt es sich zu Iridium, Stickstoff, Ammoniumchlorid und Chlorwasserstoff.[1] Es besitzt eine Kristallstruktur vom Natriumhexachloroplatinat(IV)-Typ.[3] Sehr leicht lässt es sich zu Ammoniumhexachloroiridat(III) umsetzen.[4]
Verwendung
Ammoniumhexachloroiridat wird als Zwischenprodukt zur Herstellung von reinem Iridium aus iridiumhaltigen Erzen verwendet.[5]
Einzelnachweise
- George B. Kauffmann and Larry A. Teter: Ammonium hexachloroiridate(IV). In: Henry F. Holtzclaw, Jr. (Hrsg.): Inorganic Syntheses. Band 8. McGraw-Hill Book Company, Inc., 1966, S. 223–227 (englisch).
- Datenblatt Ammonium hexachloroiridate(IV), 99.99% trace metals basis bei Sigma-Aldrich, abgerufen am 17. Februar 2018 (PDF).
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 1736.
- L: RÖMPP Lexikon Chemie, 10. Auflage, 1996-1999 Band 3: H - L. Georg Thieme Verlag, 2014, ISBN 3-13-200011-6, S. 2258 (eingeschränkte Vorschau in der Google-Buchsuche).
- Josef K. Felixberger: Chemie für Einsteiger. Springer-Verlag, 2017, ISBN 978-3-662-52821-1, S. 339 (eingeschränkte Vorschau in der Google-Buchsuche).
