7,12-Dimethylbenzo(a)anthracen
7,12-Dimethylbenzo[a]anthracen, meist mit DMBA abgekürzt, ist ein polycyclischer aromatischer Kohlenwasserstoff (PAK). Der Grundkörper der Verbindung ist Benzo[a]anthracen. DMBA ist stark krebserregend, eines der potentesten Karzinogene[3] und einer der stärksten krebserregenden polycyclischen aromatischen Kohlenwasserstoffe.[4]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
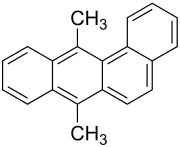 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 7,12-Dimethylbenzo[a]anthracen | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C20H16 | |||||||||||||||
| Kurzbeschreibung |
gelber Feststoff mit säuerlichem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 256,35 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
nicht eingestuft, da Verdacht auf krebserzeugende Wirkung[1] | |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Es wird in der Onkologie zum Auslösen von Tumoren in Modellorganismen verwendet.
Eigenschaften
DMBA bildet grünlich-gelbe Kristalle, die bei 122,5 °C schmelzen.[5] Es ist ausgesprochen schlecht löslich in Wasser. Lediglich 0,055 mg lösen sich in einem Liter Wasser bei 24 °C.[6] Der Oktanol-Wasser-Verteilungskoeffizient (log K) beträgt 5,70.[7] DMBA ist sehr gut löslich in Aceton sowie in Benzol.[5]
Verwendung
Aufgrund seiner starken krebserzeugenden Wirkung gibt es keine technische Anwendung für DMBA. In der Onkologie ist es ein häufig verwendetes Standard-Karzinogen, um bei Modellorganismen maligne Tumoren zu erzeugen.
DMBA wird dabei im Organismus von den P450-Enzymen zu Metaboliten abgebaut, die mit der DNA Addukte bilden.[8][9]
In den Modellorganismen können je nach Form der Applizierung Hautkrebs[10] oder Brustkrebs[11] erzeugt werden. Ebenso können Leukämien[12] und Tumoren in anderen Organen induziert werden.
Entdeckungsgeschichte
DMBA wurde erstmals 1938 von W. E. Bachmann und J. M. Chemerda synthetisiert.[13] Die krebserregende Potenz von DMBA wurde im gleichen Jahr ebenfalls von W. E. Bachmann und Kollegen an der University of Michigan entdeckt. Sie stellten dabei fest, dass DMBA in Mäusen doppelt so schnell Tumoren induziert wie 3-Methylcholanthren. Bei Variationen am Benzo[a]anthracen-Grundkörper konnten sie erkennen, dass die 7,12-Position der Methylgruppen für eine hohe Kanzerogenität verantwortlich ist.[14][15]
Literatur
- L. W. Chow u. a.: A rat cell line derived from DMBA-induced mammary carcinoma. In: Life Sciences 73, 2003, S. 27–40.
- T. Ishikawa u. a.: Inhibition of skin cancer by IP6 in vivo: initiation-promotion model. In: Anticancer Research 19, 1999, S. 3749–3752.
- H. E. Kleiner u. a.: Role of cytochrome p4501 family members in the metabolic activation of polycyclic aromatic hydrocarbons in mouse epidermis. In: Chemical Research in Toxicology 17, 2004, S. 1667–1674.
- E. Boyland: The history and future of chemical carcinogenesis. In: British Medical Bulletin 36, 1980, S. 5–10; PMID 7020830 (Review)
Einzelnachweise
- Eintrag zu 7,12-Dimethylbenz(a)anthracen in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. März 2019. (JavaScript erforderlich)
- Eintrag zu 7,12-Dimethylbenzo[a]anthracen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 16. September 2011.
- M. M. Coombs und T. S. Bhatt: Cyclopenta(a)phenanthrenes. CUP Archive, 1987, S. 8. ISBN 0-521-30123-8.
- E. L. Cavalieri u. a.: Comparative dose-response tumorigenicity studies of dibenzo[a,l]pyrene versus 7,12-dimethylbenz[a]anthracene, benzo[a]pyrene and two dibenzo[a,l]pyrene dihydrodiols in mouse skin and rat mammary gland. In: Carcinogenesis 12, 1991, S. 1939–1944; PMID 1934274.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-192.
- S. H. Yalkowsky und R. M. Dannenfelser: The AQUASOL dATAbASE of Aqueous Solubility. 5. Auflage, College of Pharmacy, 1992.
- C. Hansch u. a.: Exploring QSAR - Hydrophobic, Electronic, and Steric Constants. American Chemical Society, 1995, S. 166.
- P. D. Devanesan u. a.: Identification and quantitation of 7,12-dimethylbenz[a]anthracene-DNA adducts formed in mouse skin. In: Chemical Research in Toxicology 6, 1993, S. 364–371; PMID 7686408.
- N. V. RamaKrishna u. a.: Mechanism of metabolic activation of the potent carcinogen 7,12-dimethylbenz[a]anthracene. In: Chemical Research in Toxicology 5, 1992, S. 220–226, PMID 1643251.
- S. S. Bhattacharyya u. a.: A synthetic coumarin (4-Methyl-7 hydroxy coumarin) has anti-cancer potentials against DMBA-induced skin cancer in mice. In: European Journal of Pharmacology. April 2009, PMID 19393233
- H. Bartsch u. a.: Chronic exposure to a GSM-like signal (mobile phone) does not stimulate the development of DMBA-induced mammary tumors in rats: results of three consecutive studies. In: Radiation Research 157, 2002, S. 183–190, PMID 11835682 (Review).
- T. Sugiyama u. a.: 7,12-DMBA-induced rat leukemia: a review with insights into future research. In: Leukemia Research 26, 2002, S. 1053–1068, PMID 12443876.
- W. E. Bachmann und J. M. Chemerda: The synthesis of 9,10-dimethyl-1:2-benzanthracene, 9,10-diethyl-1:2-benzanthracene and 5,9,10-trimethyl-1:2-benzanthracene. In: Journal of the American Chemical Society 60, 1938, S. 1023.
- W. E. Bachmann u. a.: The rapid production of tumours by two new hydrocarbons. In: Yale J Biol Med. 11, 1938, S. 97–102, PMC 2601969 (freier Volltext).
- W. E. Bachmann u. a.: The rapid production of tumors by two new hydrocarbons. In: Yale J Biol Med. 73, 1939, S. 259–263, PMID 11765945.

