4-Hexylresorcin
4-Hexylresorcin leitet sich formal vom Resorcin ab. An Position 4 befindet sich ein Hexylrest. Als Lebensmittelzusatzstoff trägt es in der Europäischen Union die Bezeichnung E 586.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
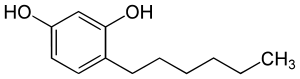 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | 4-Hexylresorcin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C12H18O2 | |||||||||||||||||||||
| Kurzbeschreibung |
hellrosafarbenes feinkristallines Pulver mit stechendem Geruch[3] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 194,27 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
333–335 °C (Zersetzung)[3] | |||||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (0,5 g·l−1 bei 20 °C)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Eigenschaften
4-Hexylresorcin ist in organischen Lösemitteln wie Ethanol, Benzol, Ether und Chloroform löslich; die Löslichkeit in Wasser ist nur gering.
Synthese
4-Hexylresorcin kann durch zwei aufeinanderfolgende Reaktionsschritte hergestellt werden. Zuerst kann eine Friedel-Crafts-Acylierung von Resorcin mit Hexanoylchlorid unter Katalyse mit AlCl3 durchgeführt werden um 4-Hexanoylresorcin zu erhalten. Die resultierende Keto-Gruppe kann anschließend mit amalgamiertem Zink und konzentrierter Salzsäure zum Alkyl-Rest reduziert werden[4]. Da bei dieser Syntheseroute stöchiometrische Mengen HCl freigesetzt werden und die Herstellung des entsprechenden Säurechlorids, durch SOCl2, ebenfalls HCl und SO2 freisetzt, ist es von großem Interesse umweltfreundlichere Synthesemethoden zu entwickeln[5]. Eine, vor allem industriell besser geeignete, Syntheseroute verwendet Capronsäure selbst als Lösemittel und gibt Zinkchlorid als Katalysator sowie Resorcin hinzu[6]. Die unter diesen Bedingungen entstandene Keto-Gruppe wird mit Wasserstoffgas und mit Raney-Nickel als Katalysator zum Alkyl-Rest reduziert. Bei dieser Syntheseroute entsteht zusätzlich ausschließlich stöchiometrisch Wasser. Des Weiteren läuft die Reduktion mit dem günstigeren Raney-Nickel unter deutlich milderen Bedingungen ab[7].
Physiologische Wirkung
4-Hexylresorcin reizt die Haut und Schleimhäute. Es wirkt anästhetisch, als Desinfektionsmittel antiseptisch und gegen parasitische Würmer als Anthelminthikum.
Verwendung
Der Stoff wird als Antioxidationsmittel bei frischen, gefrorenen und tiefgefrorenen Krebstieren eingesetzt.[8]
Einzelnachweise
- Eintrag zu E 586: 4-Hexylresorcinol in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 27. Juni 2020.
- Eintrag zu HEXYLRESORCINOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 21. März 2020.
- Datenblatt 4-Hexylresorcin (PDF) bei Merck, abgerufen am 29. Juni 2013.
- Jonathan Clayden, Nick Greeves, Stuart Warren: Organische Chemie. 2. Auflage. Springer Spektrum, 2013, ISBN 978-3-642-34715-3, S. 528, 596.
- Masato Kawamura, Dong-Mei Cui, Shigeru Shimada: Friedel–Crafts acylation reaction using carboxylic acids as acylating agents. Hrsg.: Tetrahedron. Band 62, 2006, S. 9201–9209.
- Wassmann-Wilken Suzanne, et al: Process for the synthesis of alkylresorcinols. US 2006/0129002 A1, Juni 2006.
- CJPH (Hrsg.): Improved Synthetic Process of 4-Hexylresorcinol[J]. 2016, S. 685-.
- ZZulV: Anlage 5 (zu § 5 Abs. 1 und § 7) Zusatzstoffe, die für Lebensmittel zur Konservierung oder als Antioxidationsmittel zugelassen sind
