Uranylperoxid
Uranylperoxid ist eine chemische Verbindung von Uran und Sauerstoff und zählt zu den Peroxiden. Es ist in Form seines Hydrats im Mineral Studtit enthalten.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| _ U6+ _ O2−, O− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Uranylperoxid | ||||||||||||||||||
| Andere Namen |
Urandioxid-peroxid | ||||||||||||||||||
| Verhältnisformel | UO4 | ||||||||||||||||||
| Kurzbeschreibung |
hellgelber Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 302 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
schlecht löslich in Wasser[1] | ||||||||||||||||||
| Gefahren- und Sicherheitshinweise | |||||||||||||||||||

Radioaktiv | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Allgemein kann Uranylperoxid aus einer Lösung von Uran(VI) durch Zugabe eines Peroxids, in der Regel Wasserstoffperoxidlösung, gewonnen werden. So wird aus einer siedenden Lösung von Uranylnitrat unter Zugabe von Wasserstoffperoxid und trocknen des Niederschlages das Dihydrat erhalten, während aus einer Lösung von Ammoniumuranyloxalat das Trihydrat gefällt wird.[1]
Eigenschaften
Kristallstruktur
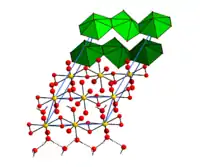
Die Kristallstruktur des Tetrahydrates besteht aus UO22+-Ionen, an die zwei Wassermoleküle und zwei Peroxidionen O22− koordiniert sind. Die Peroxidionen fungieren hierbei als μ2-Liganden, die jeweils zwei Uranatome "edge-on" verbinden. Die zusätzlichen Kristallwassermoleküle sind durch Wasserstoffbrückenbindungen an die Uranylperoxidketten gebunden.[6] Das Tetrahydrat ist bislang das einzige reine Uranylperoxid, das strukturell durch Röntgenbeugung charakterisiert wurde. Mithilfe der Dichtefunktionaltheorie konnte jedoch auch ein Strukturmodell für das Dihydrat erhalten werden, das gut mit früher veröffentlichten Röntgenbeugungsdaten übereinstimmt[7].
 Uranylperoxid
Uranylperoxid
Verwendung
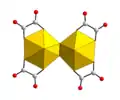
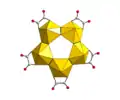
In jüngerer Zeit ist auch die Synthese von Peroxouranaten gelungen, die komplexe Käfigstrukturen aufweisen, die in ihrer Topologie den Fullerenen gleichen.[8] Diese können aus Uranylnitrat, Wasserstoffperoxid und einem Alkalihydroxid in wässriger Lösung gewonnen werden; in der Regel werden auch organische Moleküle – beispielsweise Amine – zugesetzt. Diese haben vermutlich eine Templatfunktion, ähnlich wie bei der Darstellung von Zeolithen. Auf Grund der Synthesebedingungen handelt es sich bei diesen Peroxouranverbindungen nicht um reine Uranylperoxide, da sie je nach Synthesemethode Fremdionen wie Li+ und organische Moleküle enthalten, die sich durch die bei der Strukturbestimmung verwendete Methode nicht immer nachweisen lassen.
Im System Kalium/Uranyl/Oxalat/Peroxid lassen sich durch Variation der Reaktionsbedingungen ähnliche Strukturen schrittweise aufbauen.[9]
Die genauere Untersuchung des Uran/Peroxid-Systems in den letzten Jahren wird durch die Beobachtung motiviert, dass sich durch Radiolyse in wässriger Lösung Wasserstoffperoxid bilden kann und Kenntnisse über das chemische Verhalten von Uran und anderen Actinoiden in der Gegenwart von Peroxid für die Lagerung radioaktiven Abfalls relevant sind.[10]
- Strukturen einiger Peroxouranate
Sicherheitshinweise
Wie alle Uranverbindungen, ist auch das Peroxid radioaktiv. Die spezifische Aktivität von frisch erzeugten Uranylperoxid aus irdischem Natururan beträgt 19930 Bq/g.
Einzelnachweise
- Georg Brauer: Uranperoxyd. In: Handbuch der Präparativen Anorganischen Chemie. Ferdinand Enke Verlag, Stuttgart 1954, S. 1081–1082.
- James E. Boggs, Munzire El-Chehabi: „The Thermal Decomposition of Uranium Peroxide, UO4·2H2O“, in: J. Am. Chem. Soc., 1957, 79 (16), S. 4258–4260; doi:10.1021/ja01573a003.
- Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag uranium compounds with the exception of those specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Uranverbindungen in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung.
- Peter C. Burns, Karrie-Ann Hughes: Studtite, [(UO2)(O2)(H2O)2](H2O)2: The first structure of a peroxide mineral. In: American Mineralogist. Band 88. Mineralogical Society of America, 2003, S. 1165–1168. (Abstract; PDF; 39 kB).
- Philippe F. Weck, Eunja Kim, Carlos F. Jové-Colón, David C. Sassani: Structures of uranyl peroxide hydrates: a first-principles study of studtite and metastudtite. In: Dalton Transactions, 2012, 41, S. 9748–9752 (doi:10.1039/c2dt31242e).
- Tori Z. Forbes, J. Gregory McAlpin, Rachel Murphy, Peter C. Burns: „Metal-Oxygen Isopolyhedra Assembled into Fullerene Topologies“, in: Angew. Chem. Int. Ed., 2008, 47, S. 2824–2827; doi:10.1002/ange.200705563.
- Ginger E. Sigmon, Jie Ling, Daniel K. Unruh, Laura Moore-Shay, Matthew Ward, Brittany Weaver, Peter C. Burns: „Uranyl-Peroxide Interactions Favor Nanocluster Self-Assembly“, in: J. Am. Chem. Soc., 2009, 131, S. 16648–16649; doi:10.1021/ja907837u; PMID 19919139.
- Sara Nilsson, Mats Jonsson: „H2O2 and radiation induced dissolution of UO2 and SIMFUEL pellets“, in: Journal of Nuclear Materials, 2011, 410 (1-3), S. 89–93; doi:10.1016/j.jnucmat.2011.01.020.
Literatur
- Ingmar Grenthe, Janusz Drożdżynński, Takeo Fujino, Edgar C. Buck, Thomas E. Albrecht-Schmitt, Stephen F. Wolf: Uranium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 253–698; doi:10.1007/1-4020-3598-5_5.