Trinitramid
Trinitramid ist eine Stickstoff-Sauerstoff-Verbindung, die formal als Stickstoffoxid gesehen werden kann.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
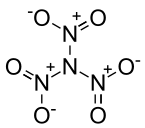 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Trinitramid | ||||||||||||
| Summenformel | N4O6 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 152,02 g·mol−1 | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Geschichte
Eine theoretische Berechnung aus dem Jahre 1993 sagte die Existenz als möglicherweise stabile Verbindung voraus.[2] Die erste Herstellung wurde 2011 von einer Arbeitsgruppe am Royal Institute of Technology in Stockholm beschrieben.[3]
Darstellung und Gewinnung
Die Herstellung erfolgt durch die Nitrierung von Kalium- bzw. Ammoniumdinitramidlösungen mittels Nitryltetrafluoroborat in Acetonitril bei tiefen Temperaturen.[3]
Eigenschaften
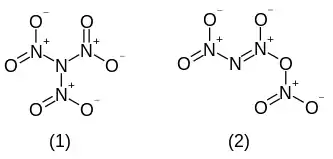
Die Verbindung wurde bisher nur in Lösung hergestellt. Der Nachweis erfolgte mittels IR-Spektroskopie und 14N-NMR-Spektroskopie.[3] Abgeleitet von der Herstellung durch Umsetzung von Dinitramidanionen und Nitrylkationen können zwei Konstitutionsisomere formuliert werden. Quantenchemische Berechnungen zeigen, dass die "echte" Trinitramidstruktur N(NO2)3 energetisch günstiger ist und somit auch nur im Experiment gefunden wurde.[4][3]
Verwendung
Eine Anwendung als Raketentreibstoff wurde postuliert.[3][5] Die Eignung als Beispielsubstanz bei der Erforschung von Materialien mit hoher Energiedichte ist eher möglich.[3]
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Montgomery Jr., J.A.; Michels, H.H.: Structure and stability of trinitramid in J. Phys. Chem. 97 (1993) 6774–6775, doi:10.1021/j100128a005.
- Rahm, M.; Dvinskikh, S.V.; Furo, I.; Brinck, T.: Experimental Detection of Trinitramide, N(NO2)3 in Angew. Chem. 123 (2011) 1177–1180, doi:10.1002/ange.201007047.
- Chen, Z.; Hamilton, T.P.: Ab Initio Calculation of the Heats of Formation of Nitrosamides: Comparison with Nitramides in J. Phys. Chem. A 103 (1999) 11026–11033, doi:10.1021/jp991735x.
- Discovery of New Molecule Could Lead to More Efficient Rocket Fuel, Science Daily, 22. Dezember 2010