Thorium(III)-iodid
Thorium(III)-iodid ist eine chemische Verbindung des Thoriums aus der Gruppe der Iodide.
| Kristallstruktur | |||||||
|---|---|---|---|---|---|---|---|
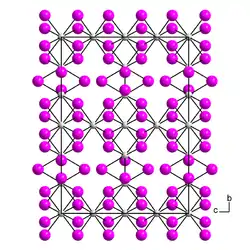 | |||||||
| _ Th3+ _ I− | |||||||
| Kristallsystem | |||||||
| Raumgruppe |
Cccm (Nr. 66) | ||||||
| Gitterparameter | |||||||
| Allgemeines | |||||||
| Name | Thorium(III)-iodid | ||||||
| Andere Namen |
Thoriumtriiodid | ||||||
| Verhältnisformel | ThI3 | ||||||
| Kurzbeschreibung |
schwarzer Feststoff[2] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 612,75 g·mol−1 | ||||||
| Aggregatzustand |
fest[2] | ||||||
| Löslichkeit |
reagiert mit Wasser[3] | ||||||
| Gefahren- und Sicherheitshinweise | |||||||

Radioaktiv | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Darstellung
Thorium(III)-iodid kann durch Reaktion von Thorium(IV)-iodid mit Thorium bei 450–550 °C gewonnen werden.[2]
Bei einer Reaktionszeit von zwei bis drei Tagen entsteht nadelförmiges α-Thorium(III)-iodid, während bei sehr langer Reaktionszeit die β-Form als kompakte Kristalle mit grünlich bis messingfarbenem Glanz entstehen.[5]
Ebenfalls möglich ist die direkte Darstellung aus den Elementen.[2]
Eigenschaften
Thorium(III)-iodid ist eine schwarze, violettstichige, meist schlecht durchkristallisierte Masse. Ausgebildete Kristalle zeigen unter dem Mikroskop starken Dichroismus von violett nach olivgrün und sind doppelbrechend. Oberhalb von 550 °C zerfällt Thorium(III)-iodid zu Thorium(IV)-iodid und Thorium(II)-iodid.[2] β-Thorium(III)-iodid hat eine orthorhombische Kristallstruktur mit der Raumgruppe Cccm (Raumgruppen-Nr. 66).[5] Die α-Form hat eine pseudoorthorhombische Kristallstruktur.[6]
Einzelnachweise
- H.P. Beck, C Strobel: ThI3, ein Janus unter den Verbindungen mit Metall-Metall-Wechselwirkungen. In: Angewandte Chemie, 1982, 94, S. 558–559 doi:10.1002/ange.19820940731.
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1142.
- R.A. Mackay, W. Henderson: Introduction to Modern Inorganic Chemistry, 6th edition. CRC Press, 2002, S. 263 (eingeschränkte Vorschau in der Google-Buchsuche).
- Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Lester R. Morss, Norman M. Edelstein, J. Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements (Set Vol.1-6…). Springer, 2010, ISBN 978-94-007-0211-0, S. 78,84 (eingeschränkte Vorschau in der Google-Buchsuche).
- Isabel Santos, A. Pires De Matos, Alfred G. Maddock: Compounds of thorium and uranium in low (< IV) oxidation states. In: A. G. Sykes (Hrsg.): Advances in Inorganic Chemistry. Band 34, 1989, S. 65–144, hier S. 84 (eingeschränkte Vorschau in der Google-Buchsuche).