Takai-Lombardo-Reaktion
Die Takai-Lombardo-Reaktion ist in der organischen Chemie eine Reaktion zur Methylenierung (sowie Olefinierung) von unreaktiven Ketonen. Sie ist mit der Takai-Methylenierung (nach dem japanischen Chemiker Kazuhiko Takai benannt) verwandt und wurde durch diese Reaktion inspiriert. Zum Einsatz kommt dabei das Lombardo-Reagenz, ein Methylenierungsreagenz, das von Luciano Lombardo publiziert wurde.[1]
Lombardo-Reagenz und Takai-Lombardo-Methylenierung
Das Lombardo-Reagenz wird in situ aus Titan(IV)-chlorid, elementarem Zink und Dibrommethan in THF hergestellt. Es ist eine milde, nicht-basische Methylenierung von Ketonen (Aldehyde reagieren unter gleichen Bedingungen zu dem Pinakol-Produkt). Ketone werden unter den Reaktionsbedingungen nicht enolisiert, das heißt α-chirale Zentren bleiben erhalten und werden nicht epimerisiert. Zahlreiche funktionelle Gruppen sind kompatibel mit dem Reagenz und den Reaktionsbedingungen wie THP-Ether, TBDMS-Ether, Acetale, Ester, Carbonsäuren, Alkohole und Lactone.[2]
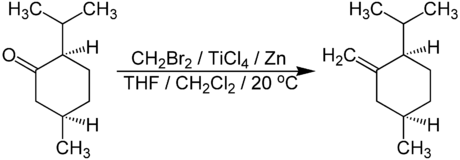
Takai-Lombardo-Olefinierung
Im Gegensatz zur Methylenierung konnte die Alkylidierung (Olefinierung; nicht zu verwechseln mit der Takai-Olefinierung) zunächst nicht zuverlässig reproduziert werden. Viele Zinkquellen enthielten Spuren von Blei, was die anfangs schlechte Reproduzierbarkeit erklärt. Durch Zusatz von katalytischen Mengen an Blei (Pb-Pulver oder PbCl2) ist es möglich, sterisch anspruchsvollere Alkylidengruppen zuverlässig zu transferieren.[3] Die Reaktion ist somit nicht auf Dibrommethan (CH2Br2) limitiert und lässt sich auf terminale Dibromide erweitern (RCHBr2), was die Takai-Lombardo-Reaktion zur Alternative für andere Olefinierungen (z. B. Wittig, Peterson, Julia) macht. Die ursprünglich schlechte Reproduzierbarkeit der Alkylidierung mit RCHBr2 hat dazu geführt, dass die Takai-Lombardo-Reaktion oft verkürzt als Methylenierung mit Dibrommethan wiedergegeben wird. Um Missverständnisse zu vermeiden, kann die Takai-Lombardo-Methylenierung mit Dibrommethan besser als beliebter Spezialfall der Takai-Lombardo-Reaktion betrachtet werden. Selbst wenn man die Olefinierung als Erweiterung der eigentlichen Reaktion mit dem Lobardo-Reagenz ansieht, können Lombardo-Methylenierung und Olefinierung deutlicher voneinander abgegrenzt und gemeinsam zur Takai-Lombardo-Reaktion zusammengefasst werden. Eine vergleichbare Unschärfe gibt es bei den verwandten Chrom-basierten Takai-Reaktionen (Methylenierung durch Takai-Reaktion sowie deren Erweiterung, die Takai-Utimoto Olefinierung); auch hier könnte sich eine schärfere sprachliche Abgrenzung bewähren.
Mechanismus
Der Reaktionsmechanismus der Reaktion ist unbekannt. Jedoch gibt es Vermutungen, dass die Reaktion über eine dimetallierte Spezies verläuft.
Einzelnachweise
- Luciano Lombardo: Methylenation of Carbonyl Compounds: (+)-3-METHYLENE-cis-p-METHANE In: Organic Syntheses. 65, 1987, S. 81, doi:10.15227/orgsyn.065.0081; Coll. Vol. 8, 1993, S. 386–392 (PDF).
- L. Lombardo: Methylenation of carbonyl compounds with Zn---CH2Br2---TiCl4. Application to gibberellins in Tetrahedron Lett. 23 (1982) 4293–4296. doi:10.1016/S0040-4039(00)88728-6.
- Kazuhiko Takai, Tadahiro Kakiuchi, Yasutaka Kataoka, Kiitiro Utimoto: A Novel Catalytic Effect of Lead on the Reduction of a Zinc Carbenoid with Zinc Metal Leading to a Geminal Dizinc Compound. Acceleration of the Wittig-Type Olefination with the RCHX2-TiCl4-Zn Systems by Addition of Lead. In: The Journal of Organic Chemistry. Band 59, Nr. 10, Mai 1994, ISSN 0022-3263, S. 2668–2670, doi:10.1021/jo00089a002.