Steviol
Steviol ist ein natürlich vorkommendes, chirales Diterpen aus der Gruppe der Kaurane bzw. Kaurene. Man findet es in den Blättern der südamerikanischen Pflanze Stevia rebaudiana in Form diverser Glycoside (Steviosid). Die Glycoside haben einen stark süßen Geschmack. Im Gegensatz zum stark süßen Steviosid ist Steviol geschmacklos.[1]
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
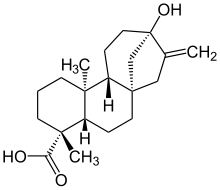 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Steviol | ||||||||||||
| Andere Namen |
(−)-13-Hydroxykaur-16-en-18-säure | ||||||||||||
| Summenformel | C20H30O3 | ||||||||||||
| Kurzbeschreibung |
kristalliner Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 318,45 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Vorkommen

Steviol kommt in Form seiner Glycoside in Stevia vor. Aus 1 kg der getrockneten Droge lassen sich bis zu 60 g Glycoside extrahieren.
Gewinnung und Darstellung
Steviol kann aus den Glycosiden durch eine enzymatische Hydrolyse mit dem Enzym Diastase gewonnen werden. Die säurekatalysierte Hydrolyse scheitert, da Steviol sich dabei in Isosteviol umlagert.
Eigenschaften
Physikalische Eigenschaften
Der optische Drehwert [α]D beträgt −65° (CHCl3).[1]
Chemische Eigenschaften
Steviol ist bis 200 °C temperaturbeständig.
Biologische Bedeutung
Steviol ist strukturell verwandt mit Gibberellinen. Entsprechend wirkt es schwach wuchsfördernd. Eine Mutante des Pilzes Gibberella fujikuroi wandelt Steviol um in 13-Hydroxygibberellin.[3] Steviol inhibiert die oxidative Phosphorylierung in Rattenmitochondrien und wirkt als Repellent gegen die Blattlaus Schizapis graminum.[4][5]
Steviol unterdrückt den Glukosestoffwechsel und die Translationsinitiation in Bauchspeicheldrüsenkrebszellen. Es hemmt auch die Glukoseaufnahme und Laktatproduktion in Bauchspeicheldrüsenkrebszellen (AsPC1 und HPAF-II) wirksam. Das tumorigene und metastatische Potenzial menschlicher Bauchspeicheldrüsenkrebszellen wird vermindert, indem Steviol Apoptose und Zellzyklusstillstand in der G1/M-Phase induziert. Die metabolische Verschiebung durch Steviol wurde durch die Unterdrückung der Phosphorylierung von mTOR und Translationsinitiationsproteinen (4E-BP1, eIF4e, eIF4B und eIF4G) vermittelt. Insgesamt deuten die Ergebnisse dieser Studie darauf hin, dass Steviol den Glukosestoffwechsel und die Translationsinitiation in Bauchspeicheldrüsenkrebszellen wirksam unterdrücken kann, um deren Aggressivität zu verringern. Bauchspeicheldrüsenkrebszellen sind hochgradig stoffwechselaktiv und typischerweise auf einen abnormen Glukosestoffwechsel umprogrammiert; daher sprechen sie schlecht auf therapeutische Maßnahmen an.[6]
Toxizität
Ames-Test (S9-Aktivierung, Chromosomenaberrationstest, Mikrokerntest und HPRT-Test): In in-vitro-Studien erwies sich Steviol als schwach mutagen und genotoxisch.[7][8][9] Die Wirkung wird Metaboliten des Steviols – wie dem 15-Oxosteviol – zugeschrieben. Aufgrund fehlender Daten sind Steviol-Glycoside in Nordamerika bisher nicht als Süßstoff zugelassen.
Nachweis
Steviol ist per HPLC analysierbar.[10]
Einzelnachweise
- Eintrag zu Steviol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Dezember 2014.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- John R. Bearder, Valerie M. Frydman, Paul Gaskin, Jake MacMillan, Colin M. Wels, Bernard O. Phinney: Fungal products. Part XVI. Conversion of isosteviol and steviol acetate into gibberellin analogues by mutant B1–41a of Gibberella fujikuroi and the preparation of [3H]gibberellin A20. In: J. Chem. Soc., Perkin Trans. 1 1976, S. 173–174. doi:10.1039/P19760000173.
- P.V. Vignais et al.: Effects of atractyligenin and its structural analogues on oxidative phosphorylation and on the translocation of adenine nucleotides in mitochondria. In: Biochim Biophys Acta., 1966 Jun 15, 118(3), S. 465–483; PMID 4226320.
- N.P. Nanayakkara et al.: Characterization and feeding deterrent effects on the aphid, Schizaphis graminum, of some derivatives of the sweet compounds, stevioside and rebaudioside A. In: J Nat Prod., 1987 May–Jun, 50(3), S. 434–441; PMID 3668559.
- Sonam Kumari et al.: Steviol Represses Glucose Metabolism and Translation Initiation in Pancreatic Cancer Cells. In: Biomedicines 2021, 9(12), 1814; https://doi.org/10.3390/biomedicines9121814
- P.J. Medon et al.: Safety assessment of some Stevia rebaudiana sweet principles. In: Fed. Proc., 1982, 41, S. 1568.
- M. Suttajit et al.: Mutagenicity and human chromosomal effect of stevioside, a sweetener from Stevia rebaudiana Bertoni. In: Environ Health Perspect. 1993 Oct. 101 Suppl 3, S. 53–56; PMID 8143647 PMC 1521159 (freier Volltext).
- T. Terai et al.: Mutagenicity of steviol and its oxidative derivatives in Salmonella typhimurium TM677. In: Chem Pharm Bull., 2002 Jul, 50(7), S. 1007–1010; PMID 12130868, doi:10.1248/cpb.50.1007.
- Harriet Wallin: Steviol Glycosides – Chemical and Technical Assessment. 63rd JECFA 2004 fao.org (PDF; 160 kB)