Shiga-Toxin
Shiga-Toxine sind nach dem japanischen Bakteriologen Kiyoshi Shiga benannte zytotoxische Proteine, produziert von Shigella dysenteriae, dem Erreger der Shigellosen oder Bakterienruhr, und nahe verwandte Proteine, die von Escherichia coli (Enterohämorrhagische Escherichia coli) produziert werden (Vero-Toxine).
| Shiga-Toxin, Untereinheit A (Shigella dysenteriae) | ||
|---|---|---|
| ||
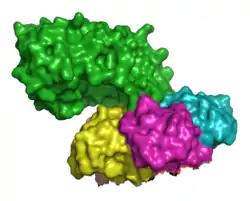
| Oberflächenmodell von A+5B nach PDB 1DM0 | ||
| Masse/Länge Primärstruktur | 293 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Monomer | |
| Bezeichner | ||
| Gen-Name(n) | stxA | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.2.2.22, Glykosidase | |
| Reaktionsart | Hydrolyse | |
| Substrat | N-Glykosid eines Adenin in 28S rRNA | |
| Produkte | defekte 28S rRNA | |
Das gesamte Shiga-Toxin besitzt eine Molmasse von rund 70.000 Dalton[1]; das Protein besteht aus zwei verschiedenen Untereinheiten, die über Disulfidbrücken miteinander verbunden sind. Die B-Untereinheit (7,6 kDa) ist fünffach vorhanden und sorgt für die Bindung an die Zelloberfläche und dafür, dass die A-Untereinheit (etwa 30 kDa[1]) in das Zellinnere geschleust wird, wo diese die Eiweißsynthese durch Spaltung der 28s-rRNA der Ribosomen hemmt. Es besitzt einen ausgeprägten Neurotropismus.
Shiga-Toxine zählen zu den Lektinen. Sie sind keine Enterotoxine und nicht für den Durchfall bei der Bakterienruhr verantwortlich, sondern – wie die ähnlichen Vero-Toxine – für deren hämolytischen Verlauf.
| Shiga-Toxin | ||
|---|---|---|
| ||
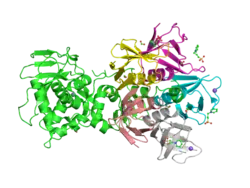
| Bindung von Adenin an Stx2, dem Shiga-Toxin 2 von Escherichia coli O157:H7 nach PDB 2ga4 | ||
| Masse/Länge Primärstruktur | 315+89 Aminosäuren (A+B) | |
| Sekundär- bis Quartärstruktur | Heterodimer | |
| Enzymklassifikation | ||
| EC, Kategorie | 3.2.2.22, N-Glycosylase | |
| Reaktionsart | Hydrolyse einer N-Glycosylbindung | |
| Substrat | rRNA (60S) + H2O | |
| Produkte | defekte rRNA (60S) | |
| Vorkommen | ||
| Übergeordnetes Taxon | Escherichia coli | |
Die Lektine Vero-Toxin 1 und Vero-Toxin 2 aus Escherichia coli werden aufgrund ihrer Ähnlichkeit zu Shiga-Toxin auch Shiga-like-toxin I/II (SLT I/II) oder Shiga-Toxin 1/2 (Stx1/Stx2) genannt. Sie beeinträchtigen die eukaryotische Proteinsynthese, indem sie die 60S-Untereinheit der Ribosomen auf katalytischem Weg inaktivieren. Die Elongation der Peptidkette wird dadurch beeinträchtigt, dass die Bindung von Aminoacyl-tRNA an die Ribosomen verhindert wird.
Von ihrer Struktur und Wirkungsweise her gehören Vero-Toxine und Shiga-Toxine zur gleichen Gruppe von Toxinen wie die Lektine Ricin und Abrin. Wie diese besitzen sie zwei Ketten bzw. Untereinheiten. Auffällig ist, dass ihre jeweilige Untereinheit genau an der gleichen Stelle wie Ricin A eine Spaltung der N-glykosidischen Bindung von Adenin in der 28S-rRNA verursacht. Diese Toxine wirken als spezifische RNA-N-Glycosidasen, welche Ribosomen inaktivieren.
Einzelnachweise
- Eintrag zu Shiga-Toxin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 28. Mai 2011.