Resiquimod
Resiquimod (R848) (Hersteller Spirig Pharma) ist ein noch in der Entwicklung befindlicher Arzneistoff aus der Gruppe der Immunmodulatoren (immune response modifier, IRM), der in der Behandlung von kleinem, oberflächlichem Basalzell-Hautkrebs (Weißer Hautkrebs; Basaliom), aktinischer Keratose, dem kutanen T-Zell-Lymphom[3] und Feigwarzen (Condylomata acuminata) eingesetzt werden soll.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
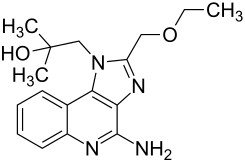 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Resiquimod | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C17H22N4O2 | |||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 314,382 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Es handelt sich bei Resiquimod um eine niedermolekulare Verbindung (small molecule).[4]
Klinische Angaben
Anwendungsgebiete (Indikationen)
Resiquimod wird derzeit in verschiedenen Indikationen geprüft, in erster Linie zur Behandlung der aktinischen Keratose.[5] Auch bei Herpes simplex-Virusinfektionen (Genitalherpes) zeigt es Wirkung,[6][7] darüber hinaus wird die Wirksamkeit als Adjuvans in der Therapie anderer viraler Erkrankungen, wie beispielsweise Hepatitis C studiert.[8][9]
Laufende Studien
Prospektive, randomisierte, teilweise verblindete, teils plazebokontrollierte multizentrische klinische Prüfung zur Untersuchung der geeigneten Dosierung, der Sicherheit, Verträglichkeit und Wirksamkeit eines äußerlich anwendbaren Resiquimod-Gels bei Patienten mit multiplen Läsionen einer aktinischen Keratose.[10]
Wirkungsmechanismus (Pharmakodynamik)
Resiquimod bindet an zwei Toll-like Rezeptoren TLR7 und TLR8, und gilt als Nachfolgesubstanz von Imiquimod, welches einen ähnlichen, aber schwächeren Wirkmechanismus besitzt und nur an TLR7 bindet.[11]
Geschichtliches
Resiquimod wurde von 3M Drug Delivery Systems entwickelt und 2010 an das schweizerische Pharmaunternehmen Spirig Pharma AG auslizenziert.[12]
Literatur
- K. Hattermann, S. Picard u. a.: The Toll-like receptor 7/8-ligand resiquimod (R-848) primes human neutrophils for leukotriene B4, prostaglandin E2 and platelet-activating factor biosynthesis. In: FASEB journal. Band 21, Nummer 7, Mai 2007, S. 1575–1585, doi:10.1096/fj.06-7457com, PMID 17264163.
- D. H. Dockrell, G. R. Kinghorn: Imiquimod and resiquimod as novel immunomodulators. In: The Journal of antimicrobial chemotherapy. Band 48, Nummer 6, Dezember 2001, S. 751–755. PMID 11733457 (Review).
Einzelnachweise
- Datenblatt Resiquimod, ≥98% (HPLC) bei Sigma-Aldrich, abgerufen am 15. Mai 2012 (PDF).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Public summary of opinion on orphan designationResiquimod for the treatment of cutaneous T-cell lymphoma Committee for Orphan Medicinal Products, der Europäischen Arzneimittel-Agentur vom 27. Mai 2016
- Gerd Plewig: Fortbildungswoche für Praktische Dermatologie und Venerologie e. V., Fortschritt durch Fortbildung 2006. Springer Verlag, 2007, ISBN 978-3-540-30514-9.
- R. M. Szeimies, J. Bichel, J. P. Ortonne, E. Stockfleth, J. Lee, T. C. Meng: A phase II dose-ranging study of topical resiquimod to treat actinic keratosis. In: Br J Dermatol. 159(1), 2008 Jul, S. 205–210. PMID 18476957
- J. J. Wu, D. B. Huang, S. K. Tyring: Resiquimod: a new immune response modifier with potential as a vaccine adjuvant for Th1 immune responses. In: Antiviral Research. Band 64, Nr. 2, November 2004, S. 79–83, doi:10.1016/j.antiviral.2004.07.002, PMID 15498602.
- K. H. Fife, T. C. Meng, D. G. Ferris, P. Liu: Effect of resiquimod 0.01% gel on lesion healing and viral shedding when applied to genital herpes lesions. In: Antimicrobial Agents and Chemotherapy. Band 52, Nr. 2, Februar 2008, S. 477–482, doi:10.1128/AAC.01173-07, PMID 18039918, PMC 2224757 (freier Volltext).
- M. A. Tomai, R. L. Miller, K. E. Lipson, W. C. Kieper, I. E. Zarraga, J. P. Vasilakos: Resiquimod and other immune response modifiers as vaccine adjuvants. In: Expert Review of Vaccines. Band 6, Nr. 5, Oktober 2007, S. 835–847, doi:10.1586/14760584.6.5.835, PMID 17931162.
- Development status of compounds that target TLRs for viral and bacterial infections, Targeting Toll-like receptors: emerging therapeutics? In: Nature Reviews Drug Discovery. 9, April 2010, S. 293–307. doi:10.1038/nrd3203
- Germany – BfArM, 2011-003943-23, Spirig Pharma AG WebSite: EU Clinical Trials Register (englisch).
- Peter Fritsch: Dermatologie und Venerologie. 2. Auflage. Springer Verlag, 2004, ISBN 3-540-00332-0.
- 3M Drug Delivery Systems Signs Agreement with Spirig Pharma AG. Pressemeldung der 3M Drug Delivery Systems vom 16. Dezember 2010 (englisch).