Natriumbromit
Natriumbromit ist eine anorganische chemische Verbindung des Natriums aus der Gruppe der Bromite.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
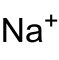 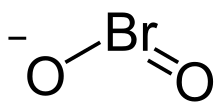 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Natriumbromit | |||||||||||||||
| Summenformel | BrNaO2 | |||||||||||||||
| Kurzbeschreibung |
schwach gelblicher Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 134,89 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
2,22 g·cm−3[2] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Natriumbromit kann durch Reaktion von Strontiumbromit mit Natriumcarbonat gewonnen werden.[5]
Natriumbromit kann auch nach einer relativ komplexen Methode hergestellt werden, in der die Verbindung aus Natriumhydroxid, Brom und Chlor hergestellt wird.[6]
Eigenschaften
Natriumbromit ist ein schwach gelblicher Feststoff, der löslich in Wasser ist. Die Verbindung und ihr Trihydrat sind an der Luft nicht beständig. Sie ziehen Feuchtigkeit an und zersetzen sich dadurch. Ihre wässrige Lösungen reagieren alkalisch und sind ebenfalls unbeständig, wobei ein Alkalizusatz eine Stabilisierung bewirkt. Natriumbromit ist ein starkes Oxydationsmittel.[1] Das Trihydrat besitzt eine trikline Kristallstruktur mit der Raumgruppe P1 (Raumgruppen-Nr. 2).[2]
Bei Temperaturen über 100 °C zersetzt sich die Verbindung.[7]
Verwendung
Natriumbromit wird in der Textilveredlung (Entschlichtungsmittel für den oxidativen Stärkeabbau[8]) verwendet.[9] Durch Reaktion mit Bariumchlorid kann Bariumbromit gewonnen werden.[5]
Einzelnachweise
- Andreas Agster: Färberei- und textilchemische Untersuchungen. Springer-Verlag, 2013, ISBN 978-3-642-64978-3, S. 98 (eingeschränkte Vorschau in der Google-Buchsuche).
- William Levason, J. Steven Ogden u. a.: Characterization of sodium bromite by x-ray crystallography and bromine K-edge EXAFS, IR, Raman, and NMR spectroscopies. In: Journal of the American Chemical Society. 111, 1989, S. 6210, doi:10.1021/ja00198a035.
- Wiley Online Library: Sodium Bromite - Procter - - Major Reference Works - Wiley Online Library, abgerufen am 17. April 2019
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Richard C. Ropp: Encyclopedia of the Alkaline Earth Compounds. Newnes, 2012, ISBN 0-444-59553-8, S. 91 (eingeschränkte Vorschau in der Google-Buchsuche).
- Google Patents: US4650658A - Stable crystals of sodium bromite trihydrate - Google Patents, abgerufen am 17. April 2019
- TOSHIF UMI KAGEYAMA: On the Stability of Sodium Bromite. In: NIPPON KAGAKU KAISHI. 1972, S. 1064, doi:10.1246/nikkashi.1972.1064.
- Peter Paetzold: Chemie Eine Einführung. Walter de Gruyter, 2009, ISBN 978-3-11-021135-1, S. 728 (eingeschränkte Vorschau in der Google-Buchsuche).
- Hans P. Latscha, Helmut A. Klein: Anorganische Chemie Chemie-Basiswissen I. Springer-Verlag, 2013, ISBN 978-3-662-05762-9, S. 389 (eingeschränkte Vorschau in der Google-Buchsuche).