Molybdän(III)-chlorid
Molybdän(III)-chlorid ist eine anorganische chemische Verbindung des Molybdäns aus der Gruppe der Chloride.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
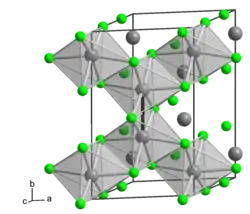 | |||||||||||||||||||
| _ Mo3+ _ Cl− Kristallstruktur von α-MoCl3 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Molybdän(III)-chlorid | ||||||||||||||||||
| Andere Namen |
Molybdäntrichlorid | ||||||||||||||||||
| Verhältnisformel | MoCl3 | ||||||||||||||||||
| Kurzbeschreibung |
roter Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 202,30 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
3,58 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Molybdän(III)-chlorid kann durch Reaktion von Molybdän(V)-chlorid mit Wasserstoff, Zinn(II)-chlorid oder metallischem Molybdän gewonnen werden.[2]
Eigenschaften
Molybdän(III)-chlorid ist ein kupferrotes bis braunes Pulver, das bei Zimmertemperatur unter Schutzgas unbegrenzt haltbar ist. An feuchter Luft erfolgt eine langsame Hydrolyse und Oxidation. Es ist unlöslich in Wasser, verdünnter Salzsäure, Aceton, Tetrachlorkohlenstoff, Benzol, und Ethanol, dafür löslich in verdünnter Salpetersäure und konzentrierter Schwefelsäure. Oberhalb von 410 °C erfolgt Disproportionierung in Molybdän(II)-chlorid und Molybdän(IV)-chlorid. Die Verbindung kommt in zwei Modifikationen vor. Die α-Form hat eine monokline Kristallstruktur ähnlich der vom Aluminium(III)-chlorid-Typ mit der Raumgruppe C2/m (Raumgruppen-Nr. 12), a = 609,2 pm, b = 974,5 pm, c = 727,5 pm, β = 124,6°. Diese Form besteht aus MoCl6-Oktaedern, wobei jeder Oktaeder über Kanten mit drei benachbarten Oktaedern verknüpft ist. Der Abstand zu einem der benachbarten Mo-Atome beträgt 274,7 pm, welches eine kovalente Mo–Mo-Bindung impliziert. Die β-Form hat ebenfalls eine monokline Kristallstruktur mit der Raumgruppe C2/c (Nr. 15), a = 611,5 pm, b = 981,4 pm, c = 1190,6 pm, β = 91,0°.[2] Es existiert auch noch ein Trihydrat.[4]
Einzelnachweise
- Datenblatt Molybdenum(III) chloride, 99.95% trace metals basis bei Sigma-Aldrich, abgerufen am 2. Juli 2013 (PDF).
- Georg Brauer: Handbuch der präparativen anorganischen Chemie. 3., umgearb. Auflage. Band III. Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1531.
- Alan K. Mallock: Molybdenum(III) chloride. In: Robert W. Parry (Hrsg.): Inorganic Syntheses. Band 12. McGraw-Hill Book Company, Inc., 1970, ISBN 07-048517-8 (defekt), S. 178–181 (englisch).
- Hermann Jehn, Wolfgang Kurtz, Dietrich Schneider, Ursula Trobisch, Joachim Wagner: Mo Molybdenum. Springer Science & Business Media, 2013, ISBN 978-3-662-06327-9, S. 281 (eingeschränkte Vorschau in der Google-Buchsuche).
