Mikrowellenspektroskopie
Die Mikrowellenspektroskopie bzw. (reine) Rotationsspektroskopie ist eine zur Gruppe der Molekülspektroskopie gehörende Untersuchungsmethode, welche Informationen über Rotationen von Molekülen liefert. Daraus lassen sich Moleküle identifizieren und weitere grundlegender Eigenschaften, wie z. B. die Bindungsstärke gewinnen. Sie dient vorzugsweise der Untersuchung von Gasen und Flüssigkeiten. Grundlage der Methode ist die Absorption von elektromagnetischen Wellen im Wellenlängenbereich von ca. 1 cm – 100 µm (Frequenzbereich von ca. 0,5–100 GHz) durch die Anregung von Molekülrotationen und damit einhergehende Übergänge zwischen den Niveaus der Hyperfeinstruktur. Im Gegensatz zur elektronischer und Schwingungsspektroskopie, welche auch Rotationsaufspaltung enthalten können, ist die störende Dopplerverbreitung bei den geringen Frequenzen der Mikrowellen kleiner.[1]
Theorie
Theoretisch kann das Rotationsspektrum durch das Modell des starren Rotators in der Regel gut beschrieben werden. Hierbei werden Moleküle nach Ihrem Aufbau und Symmetrie in linearer-, sphärischer-, symmetrischer- und asymmetrischer Rotator unterteilt.
Sphärisch- und linearer Rotator
Die Rotation eines Moleküls, bei dem Trägheitsmomente um alle drei Hauptträgheitsachsen überein stimmen (sphärischer Rotator, z. B. CH4, CCl4) oder bei dem der Drehimpuls bezüglich der Hauptachse null wird (linearer Rotator, z. B. CO2, HCl, C2H2) kann durch einen starren Rotator mit seiner Rotationsenergie beschrieben werden:
Dabei ist das Trägheitsmoment um die Rotationsachse, die Rotationquantenzahl, das plancksches Wirkungsquantum, die Lichtgeschwindigkeit und die Rotationskonstante. Bei der Rotation von Molekülen erfahren die Atome Zentrifugalkräfte, was zu einer Zentrifugalverzerrung führt. In der Realität ist dieser Effekt bei Übergängen zwischen niedrigen Rotationsniveaus vernachlässigbar.[2]
Symmetrischer Rotator
Der symmetrische Rotator (z. B. CH3Cl, NH3, C6H6) lässt sich bezüglich seiner Trägheitsmomente in zwei Komponenten aufteilen: zwei identische und ein unterschiedliches Trägheitsmoment. Die Rotationsenergie wird nun durch folgende Gleichung beschrieben:[3]
Hierbei ist die Quantenzahl des Drehimpulses bezüglich der Hauptachse, die Rotationskonstanten und verfeinern sich zu folgenden Ausdrücken:
Rotationsspektrum
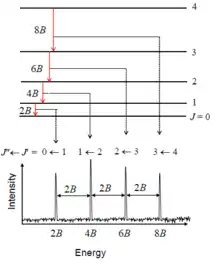
Das nebenstehende Bild zeigt den Zusammenhang zwischen den energetischen Rotationsniveaus und einem Rotationsspektrum. Die Differenz zweier Rotationsniveaus entspricht der Energie eines Rotationsübergangs , was im Spektrum durch einen Peak sichtbar wird. Hierbei zeigt sich die lineare Abhängigkeit der Energieniveaus von der Rotationskonstante. Die Linienabstände haben stets den gleichen Abstand von , was die Interpretation von Rotationsspektren erleichtert.
Die Intensität der einzelnen Peaks resultiert aus der Population des Rotationsniveaus aus dem der Übergang erfolgt. Da Moleküle stets eine gewisse Temperatur besitzen, ist nach der Boltzmann-Verteilung die Besetzung der Rotationsniveaus gegeben.[2] Die Population der Rotationsniveaus, welche sich durch die Intensität der einzelnen Übergängen ergibt, kann somit auch Rückschluss auf die Probentemperatur liefern.
Experimentelle Umsetzung
Als Messverfahren kann zum einen bei verschiedenen Frequenzen die Absorption gemessen werden, oder man bedient sich der Fouriertransformation und wertet eine zeitabhängige Absorption nach den darin enthaltenen Frequenzen aus (analog zur NMR-Spektroskopie). Weil die spontane Übergangswahrscheinlichkeit für Emission wegen der geringen Übergangsfrequenz extrem klein ist, wird die Rotationsspektroskopie meist in Absorption gemessen.[4]
Probenform
Allgemein eignen sich nur Moleküle zur Mikrowellenspektroskopie, die ein Dipolmoment besitzen. Mikrowellenspektren von Gasen zeichnen sich durch scharfe Absorptionslinien aus, da eine freie Rotation der Moleküle möglich ist. Um exakte bzw. möglichst eindeutig zuzuordnende Absorptionsspektren zu erhalten, muss die Wechselwirkung der Moleküle (siehe Druckverbreiterung) untereinander minimiert werden. Meistens wird deswegen mit geringen Mengen gasförmiger Spezies in großen Messbehältern unter geringem Druck gearbeitet.[4]
Die Mikrowellenspektroskopie kann auch zur Aufklärung von Struktur und Dynamik von Flüssigkeiten genutzt werden. Die Spektren von Flüssigkeiten zeichnen sich gegenüber anderen durch sehr breite Absorptionsbanden aus, die durch mehrere Frequenzbereiche gehen. Im Mikrowellenspektrum liefern Moleküle einen Beitrag, die ein Dipolmoment aufweisen. Die Stärke des Dipolmoments geht vorzugsweise in die Stärke der Absorption ein, wogegen die Geschwindigkeit der Molekülbewegung (Taumelrotation) die Lage der Absorptionsbande auf der Frequenzskala bestimmt. Man findet im Allgemeinen einen Zusammenhang zwischen der Viskosität einer Flüssigkeit und der Bewegungsgeschwindigkeit der Dipole.
Versuchsaufbau
Rauscharme Mikrowellen im Bereich von 1 bis 100 GHz können durch ein Reflex-Klystron erzeugt werden. Hierbei ist die spektrale Variation schwierig, was hingegen Carcinotrons und Magnetrons erlauben. Auch Mikrowellengeneratoren aus Halbleitern wie GaAs (Gunndiode) oder InP (Avalanche-Diode) werden verwendet. Die Detektion des Signals erfolgt meist mit einer Mikrowellendiode. Zur weiteren Verbesserung des Signal-Rausch-Verhältnis kann die zu untersuchende Probe einem elektrisches Wechselfeld ausgesetzt werden. Die Energieniveaus der Moleküle werden folglich durch den Stark-Effekt verschoben. Das erhaltene Messsignal wird durch die bekannte Frequenz der Feldmodulation korrigiert und mit einem Versuch ohne elektrisches Wechselfeld verglichen.[4]
Interpretation
Durch Anwenden das für die entsprechende Molekülsymmetrie passende Modell (sphärisch, linear, symmetrisch etc.) lassen sich die gesuchten Molekülgrößen bestimmen. Üblicherweise lassen sich Mikrowellenspektren mathematisch mit einer Überlagerung von Debye-Funktionen (benannt nach Peter Debye) beschreiben, wobei jeder einzelnen Debye-Funktion ein Bewegungsvorgang zugeordnet wird.
Anwendung
Mit Hilfe der Mikrowellenspektroskopie von Gasen können Informationen gewonnen werden, wie z. B.:
- Bindungslängen in einfach aufgebauten Molekülen
- Konformationen bestimmter chemischer Verbindungen, die sogenannte Rotationshyperfeinstrukturen im Absorptionsspektrum aufweisen,
- Strukturen kurzlebiger, nicht isolierbarer Spezies, die ebenfalls Rotationshyperfeinstrukturen ergeben, mit Hilfe der Molekularstrahl-Methode,
- elektronische Umgebung bzw. Elektronendichte-Verteilung um bestimmte Atomkerne herum, die sog. Quadrupolhyperfeinstrukturen im Absorptionsspektrum aufweisen.
Die Mikrowellenspektroskopie wird hauptsächlich in der Physikalischen Chemie zur Erforschung von Moleküleigenschaften eingesetzt, die über andere Methoden gar nicht oder nur schwer zu erlangen sind. Dies ist beispielsweise in Astrophysik und Radioastronomie der Fall, um Moleküle im Weltall zu identifizieren oder die Temperatur von Materie im All zu bestimmen. In heutiger Forschung wurde die Mikrowellenspektroskopie zunehmend zugunsten von elektronischer oder Schwingungsspektroskopie mit Rotationsauflösung verdrängt.
Geschichte
Etwa ein halbes Jahrhundert nach der Entdeckung und dem Verständnis der Mikrowellenstrahlung durch Michael Faraday, James Clerk Maxwell und Heinrich Hertz, wurde die Mikrowellenspektroskopie 1946 erstmals angewandt.[5]
1963 wurde mit einem Radioteleskop OH- als erstes Molekül im Weltall detektiert. In den folgenden Jahren wurde eine Reihe von Emissionen von unbekannten Übergängen gemessen. Während die Moleküle OH− und NH3 Schwingungsübergänge zeigten, waren alle anderen gemessenen Übergänge der Moleküle mit permanenten Dipolmoment reine Rotationsübergänge. Die Zuordnung gelang mittels Vergleich mit Laborversuchen. Da die Moleküle im Weltall eine gewisse Geschwindigkeit gegenüber dem Radioteleskop besitzen, mussten die Spektren um den Doppler-Effekt korrigiert werden. Es wurden so lineare und zyklische Moleküle mit einer Atomzahl von 2 bis 13 gefunden. Im Nebel Sagittarius B2, der sich mit einer Geschwindigkeit von 60 km/s bewegt, wurde somit z. B. Cyanoacetylen detektiert.[6]
Literatur
- Reinhard Demuth, Friedhelb Kober: Grundlagen der Spektroskopie. Moritz Diesterweg / Otto Salle und Sauerländer, Frankfurt/Main 1977, ISBN 3-425-05481-3, S. 48–63.
- Wolfgang Demtröder: Molekülphysik: Theoretische Grundlagen und experimentelle Methoden. Oldenbourg Wissenschaftsverlag, 2003, ISBN 978-3-486-24974-3, S. 362–366.
- J. Michael Hollas: Modern Spectroscopy. 4. Auflage. Wiley, Chichester 2004, ISBN 978-0-470-84416-8, S. 103–135.
- Claus Czeslik, Heiko Semann, Roland Winter: Basiswissen Physikalische Chemie. Teubner, Wiesbaden 2007, ISBN 978-3-8351-0047-3, S. 310–313.
- C. H. Townes, A. L. Schawlow: Microwave Spectroscopy. Courier Corporation, Chichester 2013, ISBN 978-0-486-16231-7.
Einzelnachweise
- Alan Carrington: Rotational spectroscopy of diatomic molecules. Cambridge University Press, Cambridge 2003, ISBN 0-511-06420-9.
- Heiko Seemann, Roland Winter: Basiswissen physikalische Chemie. 2., überarb. Auflage. Teubner, Wiesbaden 2007, ISBN 3-8351-0047-5.
- Julio De Paula: Physical chemistry. 9th ed. W.H. Freeman and Co, New York 2010, ISBN 978-1-4292-1812-2.
- Hans Christoph Wolf: Molekülphysik und Quantenchemie: Einführung in die experimentellen und theoretischen Grundlagen. 5. Auflage. Springer, Berlin 2006, ISBN 3-540-30314-6.
- Walter Gordy: Microwave spectroscopy. Introductory paper: quadrupole couplings, dipole moments and the chemical bond. In: Discussions of the Faraday Society. Band 19, 1955, ISSN 0366-9033, S. 14, doi:10.1039/df9551900014.
- J. Michael Hollas: Modern Spectroscopy. 4. Auflage. Wiley, Chichester 2004, ISBN 978-0-470-84416-8.