Magnesiumthiosulfat
Magnesiumthiosulfat ist das stabile Magnesiumsalz der in freiem Zustand instabilen Thioschwefelsäure.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
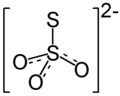 | ||||||||||
| Allgemeines | ||||||||||
| Name | Magnesiumthiosulfat | |||||||||
| Andere Namen |
Magnesiumhyposulfit | |||||||||
| Summenformel | MgS2O3 | |||||||||
| Kurzbeschreibung |
weißer Feststoff (Hexahydrat)[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse |
| |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Dichte |
1,82 g·cm−3 (20 °C)[2] | |||||||||
| Siedepunkt |
Zersetzung ab 170 °C[2] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Magnesiumthiosulfat wird durch Einrühren von Schwefel in kochende Magnesiumsulfitlösung hergestellt:[4]
Sie kann auch durch Reaktion von Bariumthiosulfat mit Magnesiumsulfat gewonnen werden.[5]
Eigenschaften
Magnesiumthiosulfat-Hexahydrat bildet farblose Kristalle. Diese verlieren bei 170–420 °C ihr Kristallwasser.[1] Das Hexahydrat hat eine orthorhombische Kristallstruktur mit der Raumgruppe Pnma (Raumgruppen-Nr. 62).[5]
Magnesiumthiosulfat ist ein Reduktionsmittel.
Verwendung
Auguste Lumière entwickelte aus der ursprünglichen Fotochemikalie das intravenös zu spritzende Medikament Magnesiumthiosulfat (damaliger Handelsname: Emgé).[6]
Magnesiumthiosulfat wurde auch als Blutstabilisator verwendet.[7]
Einzelnachweise
- Y. Elerman, J. W. Bats, H. Fuess: Deformation density in complex anions. IV. Magnesium thiosulfate hexahydrate, MgS2O3.6H2O. In: Acta Crystallographica Section C Crystal Structure Communications. Band 39, Nr. 5, 15. Mai 1983, S. 515–518, doi:10.1107/s0108270183005338.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Inorganic Compounds, S. 4-74.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Real-Encyclopädie der gesammten Pharmacie, 1886, S. 479 (urn:nbn:de:hbz:061:2-16018-p0489-2)
- A. Visweswaramurthy: Proton magnetic resonance study of the crystal structure of magnesium thiosulphate hexahydrate, MgS2O3.6H2O. In: Acta Crystallographica. Band 16, Nr. 10, 1963, ISSN 0365-110X, S. 933–935, doi:10.1107/S0365110X63002528 (iucr.org).
- Magnesium thiosulfuricum (Memento des Originals vom 23. November 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- O. Schürch, H. Willenegger, H. Knoll: Blutkonservierung und Transfusion von konserviertem Blut. Springer-Verlag, 1942, ISBN 978-3-7091-9877-3, S. 109–111 (Google Books).