Kaliumhexafluorogermanat
Kaliumhexafluorogermanat ist eine anorganische chemische Verbindung des Kaliums aus der Gruppe der Germanate.
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
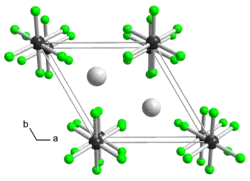 | ||||||||||
| _ K+ _ Ge4+ _ F− | ||||||||||
| Kristallsystem |
trigonal | |||||||||
| Raumgruppe |
P3m1 (Nr. 164) | |||||||||
| Gitterparameter |
a= 5,62 Å, c = 4,65 Å | |||||||||
| Allgemeines | ||||||||||
| Name | Kaliumhexafluorogermanat | |||||||||
| Andere Namen |
| |||||||||
| Verhältnisformel | K2[GeF6] | |||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 264,83 g·mol−1 | |||||||||
| Aggregatzustand |
fest[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
835 °C[2] | |||||||||
| Löslichkeit | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Kaliumhexafluorogermanat kann durch Reaktion von Germaniumdioxid mit Flusssäure und Kaliumchlorid gewonnen werden.[1]
Eigenschaften
Kaliumhexafluorogermanat ist ein weißer, nicht hygroskopischer Feststoff, der wenig löslich in Wasser ist. Bei 18 °C lösen sich 5,4 g/l, bei 100 °C 25,8 g/l Wasser.[3] Er kommt in drei Modifikationen vor,[4] wobei die Umwandlungen bei 240 °C und 500 °C erfolgen. Bei Raumtemperatur existiert eine trigonale Kristallstruktur mit der Raumgruppe P3m1 (Raumgruppen-Nr. 164) und den Gitterparametern a= 5,62 Å und c = 4,65 Å.[5]
Einzelnachweise
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 231.
- Datenblatt Potassium hexafluorogermanate bei Sigma-Aldrich, abgerufen am 25. Mai 2017 (PDF).
- Gmelins Handbuch der Anorganischen Chemie, Germanium, System Nummer 45, Achte Auflage, Verlag Chemie GmbH, Berlin 1931, Seite 60.
- Peter Paetzold: Chemie: Eine Einführung. Walter de Gruyter, 2009, ISBN 3-11-021135-1, S. 217 (eingeschränkte Vorschau in der Google-Buchsuche).
- J.L. Hoard, W.B. Vincent: Structures of Complex Fluorides. Potassium Hexafluogermanate and Ammonium Hexafluogermanate. In: Journal of the American Chemical Society, 61(10), 1939, S. 2849–2852, doi:10.1021/ja01265a082.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.