Inclisiran
Inclisiran (Handelsname Leqvio) ist ein Arzneistoff zur Behandlung erhöhter Cholesterinspiegel (Hypercholesterinämie) oder der gemischten Dyslipidämie (Fettstoffwechselstörung einhergehend mit zu hohen Spiegeln von Lipiden wie Cholesterin und Triglyzeriden oder beidem).
| Nukleinsäure | |
|---|---|
 | |
| Nukleoside: A = Adenosin, C = Cytidin, G = Guanosin, U = Uridin, dT = Desoxythymidin | |
| Allgemeines | |
| Freiname | Inclisiran[1] |
| Andere Namen |
|
| Identifikatoren | |
| CAS-Nummer |
1639324-58-5 |
| Wikidata | |
| Wirkstoffdaten | |
| DrugBank | |
| ATC-Code |
C10AX16 |
| Wirkstoffgruppe | |
| Wirkmechanismus | |
| Eigenschaften | |
| Größe |
|
| Struktur |
Synthetisches doppelsträngiges siRNA-Oligonukleotid |
Es gehört zur Gruppe der RNAi-Therapeutika.
Eigenschaften
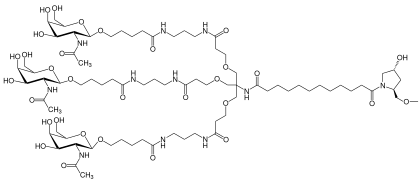
Inclisiran ist eine synthetisch hergestellte small interfering RNA (siRNA), die am Sense-Strang mit einer verzweigten N-Acetylgalactosamin-Verbindung (L96) konjugiert ist.[2] L96 erleichtert die Aufnahme in die Leberzellen (Hepatozyten). Intrazellulär hemmt die siRNA über den Mechanismus der RNA-Interferenz die Translation des Proteins PCSK9. Diese Serinprotease wirkt im Fettstoffwechsel und ist ein Angriffspunkt (target) für die lipidsenkende Behandlung.[3] Es kommt zur Erhöhung der LDL-Rezeptoren auf der Oberfläche der Hepatozyten, wodurch LDL-Cholesterin vermehrt abgebaut wird, so dass die Blutspiegel absinken.
Pharmazeutisch verwendet wird das Natriumsalz Inclisiran-Natrium,[4] ein weißes bis blassgelbes, hygroskopisches Pulver.[2]
Anwendung
In der EU besteht unter dem Namen Leqvio die Zulassung zur Behandlung Erwachsener mit einer primären Hypercholesterinämie (familiär und nicht-familiär) oder mit einer gemischten Dyslipidämie. Die Therapie sollte begleitend zu einer Diät erfolgen. Die Anwendung erfolgt gemäß Zulassung:[5]
- in Kombination mit einem Statin oder einem Statin mit anderen lipidsenkenden Therapien bei Patienten, die damit die LDL-C-Ziele nicht erreichen, oder
- allein oder in Kombination mit anderen lipidsenkenden Therapien bei Patienten mit Statin-Intoleranz oder wenn ein Statin kontraindiziert ist.
Das Mittel wird subkutan gespritzt und braucht nach den ersten beiden Dosen mit dreimonatigem Abstand nur halbjährlich verabreicht werden.[6]
Nebenwirkungen und Anwendungsbeschränkungen
Als Nebenwirkungen wurden Reaktionen an der Injektionsstelle beobachtet. Erfahrungen mit der Anwendung bei Schwangeren liegen nicht bzw. nur begrenzt vor. In tierexperimentelle Studien ergaben sich keine Hinweise auf schädliche Wirkungen.[5]
Inclisiran ist kein Substrat, Inhibitor oder Induktor für gängige Wirkstofftransporter oder für Cytochrom P450, weswegen keine klinisch bedeutsamen Wechselwirkungen mit anderen Arzneimitteln zu erwarten sind.[5]
Entwicklung und Zulassung
Inclisiran wurde von The Medicines Company entwickelt, die die Rechte von Alnylam Pharmaceuticals erworben hat.[7] 2019 gab Novartis die Übernahme von The Medicines Company bekannt.[8]
Anfang 2020 informierte Novartis, dass das Phase-III-Studien-Programm eine starke und dauerhafte Reduktion des LDL-Cholesterins unter der Gabe von Inclisiran gezeigt habe und im Dezember 2019 ein Zulassungsantrag bei der FDA eingereicht worden sei für den Einsatz bei sekundären Präventionspatienten mit atherosklerotischen Herz-Kreislauf-Erkrankungen (ASCVD) und familiärer Hypercholesterinämie (FH).[9]
Ein Zulassungsantrag bei der Europäischen Arzneimittel-Agentur (EMA) wurde im Januar 2020 eingereicht. Am 15. Oktober 2020 empfahl der zuständige Ausschuss für Humanarzneimittel die Zulassung,[10] infolgedessen die EU-Kommission Leqvio im Dezember 2020 in der Europäischen Union zuließ.[10]
Eine Zulassung in den USA seitens der Food and Drug Administration (FDA) steht noch aus. Im Juli 2021 beantwortete Novartis den im Dezember 2020 ausgestellten Complete Response Letter (CRL) der FDA, in dem noch offene Punkte im Zusammenhang mit der Inspektion einer Produktionsanlage eines Drittanbieters adressiert worden waren. Bezüglich der Wirksamkeit oder Sicherheit von Inclisiran hatte die FDA keine Bedenken geäußert.[11]
Weblinks
Einzelnachweise
- INN Recommended List 76, World Health Organisation (WHO), 9. September 2016.
- Committee for Medicinal Products for Human Use (CHMP): Assessment report - Leqvio. 15. Oktober 2020 (europa.eu [PDF]).
- Kevin Fitzgerald, Suellen White, Anna Borodovsky, Brian R. Bettencourt, Andrew Strahs: A Highly Durable RNAi Therapeutic Inhibitor of PCSK9. In: The New England Journal of Medicine. Band 376, Nr. 1, 5. Januar 2017, S. 41–51, doi:10.1056/NEJMoa1609243, PMID 27959715, PMC 5778873 (freier Volltext).
- Externe Identifikatoren von bzw. Datenbank-Links zu Inclisiran-Natrium: CAS-Nummer: 1639324-62-1, Wikidata: Q106427970. Summenformel: C529H664F12N176Na43O316P43S6. Molare Masse: 17.284,75 g·mol−1
- Zusammenfassung der Merkmale des Arzneimittels. Dezember 2020 (europa.eu [PDF]).
- L. Naßwetter: Cholesterinsenkung bald halbjährlich statt täglich? In: DAZ.online. August 2020.
- Medicines Company's PCSK9 drug hits phase 3 efficacy goals. Abgerufen am 31. März 2021 (englisch).
- Novartis to acquire The Medicines Company for USD 9.7 bn, adding inclisiran, a potentially transformational investigational cholesterol-lowering therapy to address leading global cause of death. Abgerufen am 31. März 2021 (englisch).
- Novartis successfully completes acquisition of The Medicines Company, adding a potentially first-in-class, investigational cholesterol-lowering therapy inclisiran. 6. Januar 2020, abgerufen am 31. März 2021 (englisch).
- Leqvio. European Medicines Agency, abgerufen am 31. März 2021 (englisch).
- Novartis announces Complete Response Resubmission for inclisiran New Drug Application, PM Novartis vom 6. Juli 2021, abgerufen am 7. Juli 2021