Histon H1
Histon H1 ist ein intrinsisch ungeordnetes Protein,[1] das im Zellkern vorkommt. Es ist eines der fünf Haupt-Histon-Proteine des Chromatins in eukaryotischen Zellen. Neben seiner Funktion als Gerüst für den DNA-Doppelstrang spielt es eine Rolle bei der Transkription. Es gibt mindestens sechs verschiedene Varianten von H1, die mit H1.1 bis H1.5 und H10 bezeichnet werden. Außer in einfachen Organismen wie der Bäckerhefe kommen alle Varianten in Tieren und Pflanzen vor.
| H1 histone family, member 0 | ||
|---|---|---|
| ||
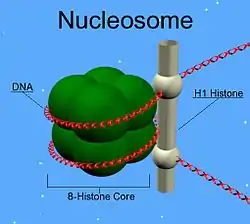
| Schemazeichnung Nukleosom mit Histon H1 (stabförmig) | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 193 Aminosäuren; 20,7 kDa | |
| Bezeichner | ||
| Gen-Namen | H1.0 ; H1F0; H1FV; H10 | |
| Externe IDs | ||
| Vorkommen | ||
| Übergeordnetes Taxon | Eukaryoten | |
| Orthologe | ||
| Mensch | Maus | |
| Entrez | 3005 | 14958 |
| Ensembl | ENSG00000189060 | ENSMUSG00000048769 |
| UniProt | P07305 | P10922 |
| Refseq (mRNA) | NM_005318 | NM_008197 |
| Refseq (Protein) | NP_005309 | NP_032223 |
| Genlocus | Chr 22: 36.53 – 36.53 Mb | Chr 15: 78.86 – 78.86 Mb |
| PubMed-Suche | 3005 | 14958 |
Biosynthese
Beim Menschen liegt das Gen für die Variante H1(0) auf Chromosom 22, alle anderen Varianten sind in einer Gruppe auf Chromosom 6 zu finden. Vom Translationsprodukt wird jeweils das Start-Methionin abgespalten. Die Länge und die Molekülmasse des resultierenden Proteins können aus der Tabelle abgelesen werden.
| Variante | Protein Länge (aa) | Protein Masse (kDa) | UniProt-Eintrag |
|---|---|---|---|
| H1(0) | 193 | 20,7 | P07305 |
| H1.1 | 214 | 21,7 | Q02539 |
| H1.2 | 212 | 21,2 | P16403 |
| H1.3 | 220 | 22,2 | P16402 |
| H1.4 | 218 | 21,7 | P10412 |
| H1.5 | 225 | 22,4 | P16401 |
| H1.T | 206 | 21,9 | P22492 |
Biologische Funktion
Histon H1 markiert die Position, an der sich die DNA um das Histonoctamer schlingt. In der G1-Phase des Zellzyklus beginnt die Phosphorylierung des Proteins und schreitet bis zum Ende der Zelle fort, ist jedoch nicht gleich verteilt über den Zellkern; man vermutet, dass aktive (stark transkribierte) Gene und hoher Phosphorylierungsgrad von H1 zusammenhängen.
H1 wird auch poly(ADP-ribosyl)iert. Diese Veränderung, bei der 60 bis 80 ADP-Ribose-Moleküle an mehreren Stellen an H1 angehängt werden (beispielsweise durch das Enzym PARP-1), führt zu einer Öffnung des Nukleosoms und hängt mit der DNA-Reparatur zusammen.[2]
Einzelnachweise
- Alessandro Borgia, Madeleine B. Borgia, Katrine Bugge, Vera M. Kissling, Pétur O. Heidarsson, Catarina B. Fernandes, Andrea Sottini, Andrea Soranno, Karin J. Buholzer, Daniel Nettels, Birthe B. Kragelund, Robert B. Best, Benjamin Schuler: Extreme disorder in an ultrahigh-affinity protein complex. In: Nature. Band 555, 1. März 2018, S. 61–66, doi:10.1038/nature25762.
- Ronald Berezney, Kwang W. Jeon (Hrsg.): Structural and Functional Organization of the Nuclear Matrix. Academic Press, 1995, ISBN 0123645654, S. 214–217.