Haloform-Reaktion
Die Haloform-Reaktion (auch Einhorn-Reaktion) ist eine organisch-chemische Reaktion. Dabei werden Methylketone durch Einwirkung von Hypohalogeniten bzw. Halogenen (Chlor, Brom oder Iod) in alkalischer Lösung unter Verlust der Methylgruppe zur Carbonsäure gespalten.[1][2] Aus dem abgespaltenen Kohlenstoffatom entsteht dabei ein Trihalogenmethan (z. B. Tribrommethan):
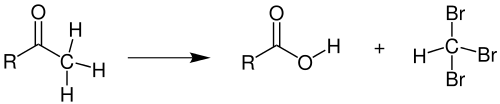 Übersicht der Halogenierung
Übersicht der Halogenierung
Die Haloform-Reaktion wurde früher auch analytisch eingesetzt, um Methylketone oder Alkohole mit einer CH3–CHOH-Gruppierung nachzuweisen. Beim Einsatz von Iod als Halogen entsteht Iodoform, das einen charakteristischen Geruch aufweist, wodurch es leicht nachzuweisen ist.[3] Diese Analysenmethode wird auch Iodoformprobe genannt.[4]
Reaktionsmechanismus
Die Reaktion verläuft unter sehr milden Bedingungen mit meist sehr guten Ausbeuten und toleriert das Vorhandensein weiterer funktioneller Gruppen im Edukt. Im Folgenden wird der angenommene Reaktionsmechanismus unter Verwendung von Brom als Halogen gezeigt.
Erster Schritt
 Halogenierung der Haloform-Reaktion[5]
Halogenierung der Haloform-Reaktion[5]
Zunächst wird das eingesetzte Keton 1 durch eine Base (hier Hydroxidion) an seiner Methylgruppe deprotoniert, wodurch ein Enolat 2 entsteht, das auf Grund der Keto-Enol-Tautomerie mit einem in α-Stellung deprotonierten Keton im Gleichgewicht steht. Das Enolat 2 kann nun mit einem Halogenmolekül (hier exemplarisch ein Brommolekül) reagieren, sodass ein in α-Stellung einfach bromiertes Keton 3 sowie ein Bromidion entsteht. Das Bromidion ist für die weitere Reaktion irrelevant. Durch den elektronenziehenden Bromsubstituenten ist die Wiederholung dieses Reaktionsschrittes begünstigt, wodurch quantitativ das in α-Stellung dreifach bromierte Keton 4 erhalten wird.
Zweiter Schritt
 Mechanismus der basenkatalysierten Halogenierung[6]
Mechanismus der basenkatalysierten Halogenierung[6]
Das Keton 4 wird von einem Hydroxidion nucleophil angegriffen. Dabei entsteht (formal) ein Alkoholat 5, das durch Umlagerung seiner Elektronen in eine Carbonsäure 6 und ein Tribrommethan-Anion 7 zerfällt. Das Anion 7 stabilisiert seine Ladung durch den −I-Effekt der Halogenatome und ist dadurch eine gute Abgangsgruppe. Im wässrigen Milieu wird es rasch zu Bromoform 8 protoniert.
Die Haloform-Reaktion ist ebenfalls mit Alkoholen durchführbar, die eine CH3–CHOH-Gruppierung enthalten,[3] wobei der Alkohol zunächst zum Keton dehydriert wird. Auch Ethanol reagiert in dieser Weise, wobei als Zwischenprodukt Acetaldehyd entsteht.
Verwendung von Trihalogenmethanen
Trihalogenmethane finden z. B. Anwendung bei der Herstellung von Reizgasen oder Desinfektionsmitteln.[6] Das wohl bekannteste Trihalogenmethan ist Chloroform. Früher wurde es häufig als Betäubungsmittel eingesetzt, heute dient es jedoch hauptsächlich als Lösungsmittel.
Einzelnachweise
- F. A. Carey, R. J. Sundberg: Organische Chemie, Wiley-VCH Verlag 2004, ISBN 3-527-29217-9.
- Louis F. Fieser und Mary Fieser: Organische Chemie, 2. Auflage, Verlag Chemie, Weinheim 1982, ISBN 3-527-25075-1, S. 405–406.
- Rainer Beckert, Hans-Joachim Knölker, Egon Fanghänel, Peter Metz, Wolf D. Habicher und Klaus Schwetlick: Organikum, 23. Auflage, Wiley-VCH Verlag, 2009, ISBN 978-3-527-32292-3, S. 454–455.
- Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 605.
- organische-chemie.ch: Haloform-Reaktion
- K. Peter C. Vollhardt, Neil E. Schore: Organische Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, 2005, 4. Auflage, H. Butenschön, ISBN 3-527-31380-X, S. 923.