Fettsäure-Synthase
Die Fettsäure-Synthase (FAS) ist das Enzym, das in Säugetieren und Pilzen den Aufbau von Fettsäuren, besonders Palmitinsäure, aus Acetyl-CoA und Malonyl-CoA katalysiert. Dies ist der Hauptprozess der Lipogenese und lebenswichtig zur Speicherung von Energie in allen Organen und Körperteilen. Im Menschen wird besonders viel FAS in Gehirn, Lunge und Leber erzeugt.[1]
| Fettsäure-Synthase | ||
|---|---|---|
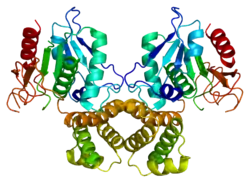 | ||
| nach 1XKT | ||
|
Vorhandene Strukturdaten: 1XKT, 2CG5, 2JFD, 2JFK, 2PX6, 3HHD, 3TJM, 4PIV, 4W82, 4W9N | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 2511 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Bezeichner | ||
| Gen-Namen | FASN FAS; OA-519; SDR27X1 | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 2.3.1.85, Transferase | |
| Reaktionsart | Verlängerung einer ACP-Fettsäurekette um zwei C-Atome | |
| Substrat | Acetyl-CoA + n Malonyl-CoA + 2n NADPH | |
| Produkte | Langkettige Fettsäure + (n+1) CoA + n CO(2) + 2n NADP(+) | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 2194 | 14104 |
| Ensembl | ENSG00000169710 | ENSMUSG00000025153 |
| UniProt | P49327 | P19096 |
| Refseq (mRNA) | NM_004104 | NM_007988 |
| Refseq (Protein) | NP_004095 | NP_032014 |
| Genlocus | Chr 17: 82.08 – 82.1 Mb | Chr 11: 120.81 – 120.82 Mb |
| PubMed-Suche | 2194 | 14104 |
Der Syntheseprozess besteht aus sieben Einzelreaktionen, die sechsmal hintereinander in derselben Reihenfolge durchgeführt werden. Jede der Einzelreaktionen hat am Fettsäure-Synthase-Molekül ein eigenes katalytisches Zentrum. Es handelt sich also um ein multifunktionelles Enzym. Die genaue Lage dieser katalytischen Zentren zueinander ist Gegenstand der Forschung. In Pflanzen und Bakterien übernehmen einzelne Enzyme die Aufgabe der FAS.[2]
Regulation
Die FAS wird in vielen Tumor-Zelllinien überexprimiert, ebenso bei Hepatitis B- und Hepatitis-C-Virusinfektion; FAS-Hemmung führt außerdem zu verringerter HCV-Virusreplikation. Es wird vermutet, dass gesundheitsfördernde Wirkungen von Pflanzenstoffen wie Epigallocatechin-3-gallat (Grüner Tee) oder Farnesol und Inhaltsstoffen aus Olivenöl auf einer Hemmung der FAS beruhen. Die Fettsäure-Synthase ist damit interessantes Target für die Pharmaindustrie.[3][4][5][6][7][8][9]
Expression der FAS wird durch SREBP-1c angeregt, das seinerseits bei Sauerstoffmangel blockiert wird – dann wird durch Herunterfahren der aufwändigen Fettsäuresynthese Energie gespart. In der Zellmembran lokalisierte FAS ist mit Caveolin-1 assoziiert.[10][11]
Katalysierter Prozess
Siehe Artikel Fettsäuresynthese.
Einzelnachweise
- UniProt P49327
- A. Witkowski, V. S. Rangan u. a.: Structural organization of the multifunctional animal fatty-acid synthase. In: European Journal of Biochemistry Band 198, Nummer 3, Juni 1991, S. 571–579. PMID 2050137.
- De Vincentiis M, Di Cello P, Censi F, et al: Immunohistochemical expression of fatty acid synthase, Ki-67 and p53 in squamous cell carcinomas of the larynx. In: Int. J. Biol. Markers. 23, Nr. 3, 2008, S. 176–81. PMID 18949744.
- Wang KF, Wu B: [Fatty acid synthase and prostate cancer]. In: Zhonghua Nan Ke Xue. 14, Nr. 8, August 2008, S. 740–2. PMID 18817351.
- Kim K, Kim KH, Kim HH, Cheong J: Hepatitis B virus X protein induces lipogenic transcription factor SREBP1 and fatty acid synthase through the activation of nuclear receptor LXRalpha. In: Biochem. J.. 416, Nr. 2, Dezember 2008, S. 219–30. doi:10.1042/BJ20081336. PMID 18782084.
- Yang W, Hood BL, Chadwick SL, et al: Fatty acid synthase is up-regulated during hepatitis C virus infection and regulates hepatitis C virus entry and production. In: Hepatology. 48, Nr. 5, November 2008, S. 1396–403. doi:10.1002/hep.22508. PMID 18830996.
- Menendez JA, Vazquez-Martin A, Oliveras-Ferraros C, et al: Analyzing effects of extra-virgin olive oil polyphenols on breast cancer-associated fatty acid synthase protein expression using reverse-phase protein microarrays. In: Int. J. Mol. Med.. 22, Nr. 4, Oktober 2008, S. 433–9. PMID 18813848.
- Witkiewicz AK, Nguyen KH, Dasgupta A, et al: Co-expression of fatty acid synthase and caveolin-1 in pancreatic ductal adenocarcinoma: implications for tumor progression and clinical outcome. In: Cell Cycle. 7, Nr. 19, Oktober 2008, S. 3021–5. PMID 18802406.
- Duncan RE, Archer MC: Farnesol decreases serum triglycerides in rats: identification of mechanisms including up-regulation of PPARalpha and down-regulation of fatty acid synthase in hepatocytes. In: Lipids. 43, Nr. 7, Juli 2008, S. 619–27. doi:10.1007/s11745-008-3192-3. PMID 18509688.
- Choi SM, Cho HJ, Cho H, Kim KH, Kim JB, Park H: Stra13/DEC1 and DEC2 inhibit sterol regulatory element binding protein-1c in a hypoxia-inducible factor-dependent mechanism. In: Nucleic Acids Res.. 36, Nr. 20, November 2008, S. 6372–85. doi:10.1093/nar/gkn620. PMID 18838394. PMC 2582599 (freier Volltext).
- Di Vizio D, Adam RM, Kim J, et al: Caveolin-1 interacts with a lipid raft-associated population of fatty acid synthase. In: Cell Cycle. 7, Nr. 14, Juli 2008, S. 2257–67. PMID 18635971.
Weblinks
- Joashi-Tope/reactome.org: Conversion of Butyryl-ACP to Palmitoyl-ACP