Eisenpolymaltose
Eisen-III-hydroxid-Polymaltose-Komplex (Eisenpolymaltose) ist ein makromolekularer Komplex, bestehend aus Eisen(III)-hydroxid (dreiwertiges Eisen, Fe3+) und Polymaltose. Der Eisenkomplex wird als Arzneistoff angewendet zur oralen Behandlung des Eisenmangels ohne Anämie (latenter Eisenmangel) oder mit Anämie (manifester Eisenmangel, Eisenmangelanämie). Vor der Anwendung sollte der Eisenmangel diagnostisch und labortechnisch gesichert sein (z. B. tiefes Ferritin, tiefe Transferrin-Sättigung).
| Allgemeines | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Name | Eisenpolymaltose | ||||||||||||
| Andere Namen |
| ||||||||||||
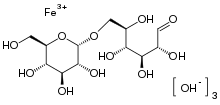
| Summenformel | C12H25FeO14 | ||||||||||||
| Kurzbeschreibung |
dunkelroter bis dunkelbrauner Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Arzneistoffangaben | |||||||||||||
| ATC-Code |
B03AB05 | ||||||||||||
| Wirkstoffklasse |
orale Eisenpräparate | ||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | variabel | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Toxikologische Daten | |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Das Arzneimittel ist seit 1978 auf dem Markt und in über 85 Ländern zugelassen.
Pharmakologie
Wirkungsweise
Der Wirkstoff wird im Dünndarm, vorwiegend im Zwölffingerdarm und im Leerdarm, aufgenommen. Die Absorption erfolgt über einen kontrollierten, aktiven Mechanismus. Es findet keine passive Diffusion statt, was gewährleistet, dass praktisch kein nicht an Transferrin gebundenes Eisen in das Blut gelangt[4]. Das aufgenommene Eisen wird vorwiegend in der Leber als Ferritin (Speichereisen) gespeichert und von dort dem Körper für verschiedenen Funktionen, hauptsächlich zum Einbau in Hämoglobin in den roten Blutkörperchen, zur Verfügung gestellt, wo es dem Transport von Sauerstoff im Blut dient.
Die Aufnahme in die Erythrozyten des über Eisenpolymaltose-Komplex oral zugeführten Eisens korreliert mit der Resorption im Darm, wobei die relative Resorption mit zunehmender Dosierung abnimmt, und je höher ausfällt, je ausgeprägter der Eisenmangel ist[5]. Wie bei allen oralen Eisenpräparaten wird nur ca. 10–15 % des Eisens resorbiert[6]. Eine Dosis von 100 mg Eisen ist also notwendig, damit 10 mg aufgenommen werden.
Pharmakokinetik
Nach der Verabreichung wird das maximale Resorptionsvermögen bereits nach 30 Minuten erreicht und eine kontinuierlich steigende Resorption ist über 24 Stunden zu beobachten[7]. Das nicht aufgenommene Eisen wird über den Stuhl ausgeschieden.
Klinische Wirksamkeit und Sicherheit
Die Wirksamkeit und Sicherheit wurde in zahlreichen klinischen Studien und bei verschiedenen Populationen untersucht und dokumentiert,[8] unter anderem bei Kindern, Jugendlichen, Erwachsenen und Senioren sowie bei schwangeren Frauen und bei stillenden Müttern.
In der Studie von Ortiz et al.[9] wurde Eisenpolymaltose 100 mg 2xtäglich im Vergleich mit Eisensulfat 100 mg 2xtäglich in einem randomisierten, offenen, multizentrischen, kontrollierte Studiendesign bei schwangeren Frauen mit Eisenmangelanämie untersucht. Die Studiendauer betrug 90 Tage. Es zeigte sich eine Verbesserung des Hämoglobins nach 90 Tagen um 2,16 g/dl (Eisenpolymaltose) und 1,93 g/dl (Eisensulfat). Die Ferritinspiegel nach 90 Tagen betrugen 179 ng/ml (Eisenpolymaltose) und 157 ng/ml (Eisensulfat). Nebenwirkungen traten bei 29,3 % der Patienten unter Eisenpolymaltose und bei 56,4 % unter Eisensulfat auf.
Die randomisierte, offene Studie bei Kindern mit Eisenmangelanämie von Yasa et al.[10] untersuchte Eisenpolymaltose 5 mg/kg Körpergewicht in einer Verabreichung pro Tag im Vergleich mit Eisensulfat 5 mg/kg Körpergewicht, aufgeteilt auf 2 Verabreichungen pro Tag, die Studiendauer betrug 4 Monate. Es resultierte eine Verbesserung des Hämoglobins nach 4 Monaten um 2,3 g/dl (Eisenpolymaltose) und 3 g/dl (Eisensulfat). Es wurden weniger gastrointestinale Nebenwirkungen unter Eisenpolymaltose beobachtet und der mittlere Akzeptanzwert nach 4 Monaten war höher mit Eisenpolymaltose als mit Eisensulfat.
Die randomisierte, multizentrische, doppelblinde Studie bei Erwachsenen mit Eisenmangelanämie von Langstaff et al.[11] prüfte Eisenpolymaltose 100 mg 2xtäglich im Vergleich mit Eisensulfat 60 mg 3xtäglich über 9 Wochen. Eine Verbesserung des Hämoglobins war in beiden Gruppen nach 3, 6 und 9 Wochen zu beobachten, wobei nach 3 und 6 Wochen in der Eisensulfat-Gruppe die Verbesserung ausgeprägter war. Nach 9 Wochen war die Verbesserung in beiden Gruppen vergleichbar groß. Nebenwirkungen traten bei 22 % der Patienten unter Eisenpolymaltose auf und bei 25 % der Patienten unter Eisensulfat.
Gegenanzeigen und Anwendungsbeschränkungen
Bei einer bekannten Überempfindlichkeit oder Unverträglichkeit gegenüber dem Wirkstoff oder einem der Hilfsstoffe darf Eisenpolymaltose nicht angewendet werden. Bei Anämien, die eine andere Ursache als Eisenmangel haben, wird kein Eisenpräparat verabreicht. Bei bekannter Eisenüberladung oder Eisenverwertungsstörung dürfen Eisenpräparate ebenfalls nicht verabreicht werden.
Eisenpolymaltose darf nicht gleichzeitig mit parenteralen Eisenpräparaten verabreicht werden. Wechselwirkungen mit anderen Medikamenten oder mit Nahrungsmitteln sind nicht bekannt.
Nebenwirkungen
Als übliche Nebenwirkungen mit einer Häufigkeit zwischen 1 % und 10 % wurden unter anderen Stuhlverfärbungen, Durchfall, Übelkeit und Dyspepsie beobachtet. Unübliche Nebenwirkungen mit einer Häufigkeit zwischen 0,1 % und 1 % umfassten unter anderen Verstopfung, Erbrechen, Bauchschmerzen, Zahnverfärbung, Juckreiz und Kopfschmerzen. Als sehr seltene Nebenwirkungen mit einer Häufigkeit zwischen 0,1 % und 0,01 % wurden allergische Reaktionen beschrieben.
Handelsnamen und Darreichungsformen
Ferrum Hausmann (D), Maltofer (CH), Ferrosig
Eisenpolymaltose gibt es als Film- oder Kautablette und in flüssiger Form als Sirup, Trinklösung oder Tropfen.
Einzelnachweise
- Eintrag zu Ferric Carboxymaltose (Technical Grade) bei Toronto Research Chemicals, abgerufen am 27. Januar 2022 (PDF).
- Biosynth Carbosynth: Ferric carboxymaltose | 53858-86-9 | Biosynth Carbosynth, abgerufen am 29. Januar 2022
- Eintrag zu Iron polymaltose in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 7. April 2017.
- P. Geisser: Safety and efficacy of iron(III)-hydroxide polymaltose complex / a review of over 25 years experience. In: Arzneimittelforschung. Band 57, Nummer 6A, 2007, S. 439–452, doi:10.1055/s-0031-1296693, PMID 17691594 (Review).
- P. Geisser, S. Burckhardt: The pharmacokinetics and pharmacodynamics of iron preparations. In: Pharmaceutics. Band 3, Nummer 1, Januar 2011, S. 12–33, doi:10.3390/pharmaceutics3010012, PMID 24310424, PMC 3857035 (freier Volltext).
- J. P. Kaltwasser, E. Werner, M. Niechzial: Bioavailability and therapeutic efficacy of bivalent and trivalent iron preparations. In: Arzneimittelforschung. Band 37, Nummer 1A, Januar 1987, S. 122–129, PMID 3566867.
- P. Geisser, S. Burckhardt: The pharmacokinetics and pharmacodynamics of iron preparations. In: Pharmaceutics. Band 3, Nummer 1, Januar 2011, S. 12–33, doi:10.3390/pharmaceutics3010012, PMID 24310424, PMC 3857035 (freier Volltext).
- J. E. Toblli, R. Brignoli: Iron(III)-hydroxide polymaltose complex in iron deficiency anemia / review and meta-analysis. In: Arzneimittelforschung. Band 57, Nummer 6A, 2007, S. 431–438, doi:10.1055/s-0031-1296692, PMID 17691593 (Review).
- R. Ortiz, J. E. Toblli, J. D. Romero, B. Monterrosa, C. Frer, E. Macagno, C. Breymann: Efficacy and safety of oral iron(III) polymaltose complex versus ferrous sulfate in pregnant women with iron-deficiency anemia: a multicenter, randomized, controlled study. In: J. Matern. Fetal. Neonatal. Med. Band 24, Nummer 11, November 2011, S. 1347–1352, doi:10.3109/14767058.2011.599080, PMID 21859366.
- B. Yasa, L. Agaoglu, E. Unuvar: Efficacy, Tolerability, and Acceptability of Iron Hydroxide Polymaltose Complex versus Ferrous Sulfate: A Randomized Trial in Pediatric Patients with Iron Deficiency Anemia. In: Int J Pediatr. Band 2011, 2011, S. 524520, doi:10.1155/2011/524520, PMID 22121379, PMC 3206382 (freier Volltext).
- RJ. Langstaff, P. Geisser, WG. Heil, JM. Bowdler. Treatment of iron-deficiency anaemia: a lower incidence of adverse effects with Ferrum Hausmann than ferrous sulphate. In: British Journal of Clinical Research. Band 4, 1993; 191–198.