Disintegrine
Disintegrine sind Polypeptide, die erstmals aus dem Gift verschiedener Vipern (Viperidae) isoliert wurden. Die Sequenz findet sich aber auch als Disintegrin-Domäne in einer Reihe humaner Enzyme, den ADAM-Metalloproteasen. Bisher sind über 25 verschiedene Disintegrine aus Schlangengift isoliert worden.
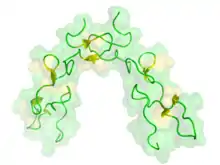
Aufbau
Disintegrine sind wasserlösliche cysteinreiche nicht-enzymatische Peptide, die in Schlangengift aus 41 bis 84 Aminosäuren bestehen. In den ADAM-Proteasen besteht die Sequenz der Disintegrin-Domäne meist aus ungefähr 90 Aminosäuren. Fast alle Disintegrine und Disintegrin-Domänen, so beispielsweise auch ADAM15, enthalten die RGD-Sequenz (Arg-Gly-Asp), die beispielsweise an αvβ3-Integrine bindet.[1] Andere Disintegrine der ADAMs können an andere Integrine binden. ADAM28 bindet an α4β1[2]
Im Schlangengift bewirken die Disintegrine eine verminderte Blutgerinnung durch die Bindung an den Fibrinogen-Bindungsrezeptor – das Integrin αIIbβ3 – der Thrombozyten.[3]
Die RGD-Sequenz, oder wie im Fall von Obtustatin die KTS-Sequenz, wird am Ende einer Schleifenstruktur des Peptids dem jeweiligen Rezeptor präsentiert.[4]
Anwendung
Die hochspezifische Bindung an verschiedene Rezeptoren machen die Disintegrine zu potenziellen Wirkstoffen zur Behandlung einer Reihe von Erkrankungen. Die antikoagulative Wirkung kann beispielsweise zur Vorbeugung vor Thromben genutzt werden.[5] Weltweit werden die Disintegrine für die Therapie von Krebs, Asthma und Osteopenie erprobt.[6]
Speziell die hohe Affinität zu bestimmten Integrinen, die beim Tumorwachstum wichtig für die Neubildung von Blutgefäßen (Angiogenese) sind (beispielsweise αvβ3), ist dabei von Interesse.[7]
Beispiele
Auswahl einiger Schlangen-Disintegrine.
| Name | nAminosäuren | nCystein | Spezies |
| Albolabrin[8] | 73 | 12 | Weißlippen-Bambusotter (Trimeresurus albolabris) |
| Rhodostomin[3] | 68 | 12 | Malayische Mokassinotter (Calloselasma rhodostoma) |
| Trigramin[9] | 72 | 12 | Grüne Bambusotter (Trimeresurus gramineus) |
| Batroxostatin[10] | 71 | 12 | Gewöhnliche Lanzenotter (Bothrops atrox) |
| Elegantin[11][12] | 73 | 12 | Trimeresurus elegans |
| Applagin[8] | 71 | 12 | Wassermokassinotter (Agkistrodon piscivorus) |
| Barbourin[13][14] | 73 | 12 | Zwergklapperschlange (Sistrurus m. barbouri) |
| Bitistatin[4][15] | 83 | 14 | Puffotter (Bitis arietans) |
| Obtustatin[16] | 41 | 8 | Levanteotter (Macrovipera lebetina) |
| Echistatin[16][17] | 49 | 8 | Gemeine Sandrasselotter (Echis carinatus) |
| Eristostatin[16][18] | 49 | 8 | MacMahon-Viper (Eristicophis macmahoni) |
| Halysin[19][20] | 71 | 12 | Halysotter (Gloydius halys) |
| Kistrin[19][21] | 68 | 12 | Malayische Mokassinotter (Calloselasma rhodostoma) |
| Mambin[19][22] | 59 | 8 | Jamesons Mamba (Dendroaspis jamesoni) |
| Tergeminin[14] | 73 | 12 | Westliche Massassauga (Sistrurus catenatus tergeminus) |
| Triflavin[23] | 70 | 12 | Habu-Schlange (Trimeresurus flavoviridis) |
Einzelnachweise
- D. F. Seals und S. A. Courtneidge: The ADAMs family of metalloproteases: multidomain proteins with multiple functions. In: Genes Dev 17, 2003, S. 7–30. PMID 12514095 (Review)
- L. C. Bridges u. a.: The lymphocyte metalloprotease MDC-L (ADAM 28) is a ligand for the integrin α4β1. In: J Biol Chem 277, 2002, S. 3784–3792. PMID 11724793
- C. P. Chang u. a.: Positional importance of Pro53 adjacent to the Arg49-Gly50-Asp51 sequence of rhodostomin in binding to integrin alphaIIbbeta3. In: Biochem J 357, 2001, S. 57–64. PMID 11415436, PMC 1221928 (freier Volltext)
- L. C. Knight und J. E. Romano: Functional expression of bitistatin, a disintegrin with potential use in molecular imaging of thromboembolic disease. In: Protein Expr Purif 39, 2005, S. 307–319. PMID 15642483
- K. Stocker: Anwendung von Schlangengiftproteinen in der Medizin. (PDF; 182 kB) In: Schweiz Med Wochenschr 129, 1999, S. 205–216.
- M. A. McLane u. a.: Disintegrins in health and disease. In: Front Biosci 13, 2008, S. 6617–6637. PMID 18508683 (Review)
- S. Swenson u. a.: Anti-angiogenesis and RGD-containing snake venom disintegrins. In: Curr Pharm Des 13, 2007, S. 2860–2871. PMID 17979731 (Review)
- J. J. Calvette u. a.: Identification of the disulfide bond pattern in albolabrin, an RGD-containing peptide from the venom of Trimeresurus albolabris: significance for the expression of platelet aggregation inhibitory activity. In: Biochemistry 30, 1991, S. 5225–5229. PMID 2036389
- T. F. Huang u. a.: Trigramin. A low molecular weight peptide inhibiting fibrinogen interaction with platelet receptors expressed on glycoprotein IIb-IIIa complex. In: J Biol Chem 262, 1987, S. 16157–16163. PMID 3680247
- B. Rucinski u. a.: Batroxostatin, an Arg-Gly-Asp-containing peptide from Bothrops atrox, is a potent inhibitor of platelet aggregation and cell interaction with fibronectin. In: Biochim Biophys Acta 1054, 1990, S. 257–262. PMID 2207176
- J. Williams u. a.: Elegantin and albolabrin purified peptides from viper venoms: homologies with the RGDS domain of fibrinogen and von Willebrand factor. In: Biochim Biophys Acta 1039, 1990, S. 81–89. PMID 2191722
- A. Scaloni u. a.: Amino acid sequence and molecular modelling of glycoprotein IIb-IIIa and fibronectin receptor iso-antagonists from Trimeresurus elegans venom. In: Biochem J 319, 1996, S. 775–782. PMID 8920980
- H. Minoux u. a.: Structural analysis of the KGD sequence loop of barbourin, an alphaIIbbeta3-specific disintegrin. In; J Comput Aided Mol Des 14, 2000, S. 317–327. PMID 10815769
- R. M. Scarborough u. a.: Barbourin. A GPIIb-IIIa-specific integrin antagonist from the venom of Sistrurus m. barbouri. In: J Biol Chem 266, 1991, S. 9359–9362. PMID 2033037
- J. J. Calvetea u. a.: The disulphide bond pattern of bitistatin, a disintegrin isolated from the venom of the viper Bitis arietans. In: FEBS Letters 416, 1997, S. 197–202. PMID 9369214
- C. Marcinkiewicz u. a.: Obtustatin: a potent selective inhibitor of alpha1beta1 integrin in vitro and angiogenesis in vivo. In: Cancer Res 63, 2003, S. 2020–2023. PMID 12727812
- Z. R. Gan u. a.: Echistatin. A potent platelet aggregation inhibitor from the venom of the viper, Echis carinatus. In: J Biol Chem 263, 1988, S. 19827–19832. PMID 3198653
- J. Tian u. a.: Inhibition of melanoma cell motility by the snake venom disintegrin eristostatin. In: Toxicon 49, 2007, S. 899–908. PMID 17316731
- L. C. Knight u. a.: Comparison of iodine-123-disintegrins for imaging thrombi and emboli in a canine model. In: J Nucl Med 37, 1996, S. 476–482. PMID 8772651
- T. F. Huang u. a.: Halysin, an antiplatelet Arg-Gly-Asp-containing snake venom peptide, as fibrinogen receptor antagonist. In: Biochem Pharmacol 42, 1991, S. 1209–1219. PMID 1888330
- T. Yasuda u. a.: Kistrin, a polypeptide platelet GPIIb/IIIa receptor antagonist, enhances and sustains coronary arterial thrombolysis with recombinant tissue-type plasminogen activator in a canine preparation. In: Circulation 83, 1991, S. 1038–1047. PMID 1900221
- R. S. McDowell u. a.: Mambin, a potent glycoprotein IIb-IIIa antagonist and platelet aggregation inhibitor structurally related to the short neurotoxins. In: Biochemistry 31, 1992, S. 4766–4772. PMID 1591238
- T. F. Huang u. a.: A potent antiplatelet peptide, triflavin, from Trimeresurus flavoviridis snake venom. In: Biochem J 277, 1991, S. 351v357. PMID 1859363
Literatur
- R. J. Gould u. a.: Disintegrins: a family of integrin inhibitory proteins from viper venoms. In: Proc Soc Exp Biol Med 195, 1990, S. 168–171. PMID 2236100 (Review)
- J. A. Williams: Disintegrins: RGD-containing proteins which inhibit cell/matrix interactions (adhesion) and cell/cell interactions (aggregation) via the integrin receptors. In: Pathol Biol (Paris) 40, 1992, S. 813–821. PMID 1484742 (Review)
- S. Niewiarowski u. a.: Disintegrins and other naturally occurring antagonists of platelet fibrinogen receptors. In: Semin Hematol 31, 1994, S. 289–300. PMID 7831574 (Review)
- T. F. Huang: What have snakes taught us about integrins? In: Cell Mol Life Sci 54, 1998, S. 527–540. PMID 9676572 (Review)
- R. M. Kini: Anticoagulant proteins from snake venoms: structure, function and mechanism. In: Biochem J 397, 2006, S. 377–387. PMID 16831131 (Review), PMC 1533313 (freier Volltext)
- C. H. Yang: Inhibition of retinal pigment epithelial cell-induced tractional retinal detachment by disintegrins, a group of Arg-Gly-Asp-containing peptides from viper venom. In: Invest Ophthalmol Vis Sci 37, 1996, S. 843–854. PMID 8603869
- M. A. McLane u. a.: Disintegrins. In: Curr Drug Targets Cardiovasc Haematol Disord 4, 2004, S. 327–355. PMID 1557895 (Review)
- X. Lu u. a.: Snake venom metalloproteinase containing a disintegrin-like domain, its structure-activity relationships at interacting with integrins. In: Curr Med Chem Cardiovasc Hematol Agents 3, 2005, S. 249–260. PMID 15974889
- C. Barja-Fidalgo u. a.: Disintegrins: integrin selective ligands which activate integrin-coupled signaling and modulate leukocyte functions. In: Braz J Med Biol Res 38, 2005, S. 1513–1520. PMID 16172744 (Review)
- J. A. Williams: Disintegrins: RGD-containing proteins which inhibit cell/matrix interactions (adhesion) and cell/cell interactions (aggregation) via the integrin receptors. In: Pathol Biol (Paris) 40, 1992, S. 813–821. PMID 1484742 (Review)
- K. Grimm: Induktion der Integrin vermittelten Synthese und Aktivierung von Matrix Metalloproteinasen durch Schlangengift Metalloproteinasen in dermalen Fibroblasten. Dissertation, Universität zu Köln, 2003. urn:nbn:de:hbz:38-13157
Weblinks
- T. Wolf: Schlangengift gegen Krebs. In: Die Welt vom 2. Februar 2008
- T. Wolf: Schlangengift gegen Krebs, Alzheimer und Parkinson. In: Berliner Morgenpost vom 3. Februar 2008