Diketopyrrolopyrrol-Pigmente
Diketopyrrolopyrrol-Pigmente (DPP-Pigmente) sind sehr lösemittel- und witterungsbeständige polyzyklische Farbmittel, die bei der Herstellung verschiedener Lacke und bei der Einfärbung von Kunststoffen Verwendung finden. Obwohl auch Vertreter mit Farbstoffeigenschaften existieren, sind mit der Bezeichnung DPP zumeist die Pigmente gemeint.

Geschichte
DPP-Pigmente wurden erstmals 1974 in geringen Mengen über eine Reformatzki-Reaktion in den Laboratorien der damaligen Ciba-Geigy (CH-Basel) synthetisiert. Nach umfangreichen Arbeiten zur Optimierung der Synthese kam 1986 das erste Produkt auf den Markt. Nach dem Ablauf des Patentes wurden ab 2004 mehrere Konkurrenzprodukte, insbesondere für den wichtigsten Vertreter, C.I. Pigment Red 254, von europäischen und asiatischen Firmen herausgebracht, die für einen starken Preisverfall sorgten.[1][2]
Chemische Struktur
DPP-Pigmente basieren auf der stickstoffhaltigen, heterocyclischen Verbindung Diketopyrrolopyrrol. Darin sind zwei Fünfringe der Substanz Pyrrol anelliert; an zweien zum Stickstoffatom α-ständigen Kohlenstoffatomen (Positionen eins und vier) besitzen die Pigmente jeweils eine Carbonylgruppe (Diketo) und sind damit auch Lactame.
Die bicyclischen Chromophore leiten sich formal auch vom Octahydropentalen (Bicyclo[3.3.0]octan) ab, bei dem C-2 und C-5 durch Stickstoffatome ersetzt sind (2,5-Diaza-Octahydropentalen oder 2.5-Diaza-bicyclo[3.3.0]octan). Man erhält somit als Grundkörper das 2,5-Dihydropyrrolo[3,4-c]pyrrol-1,4-dion (nach IUPAC) oder einfacher Diketopyrrolopyrrol.
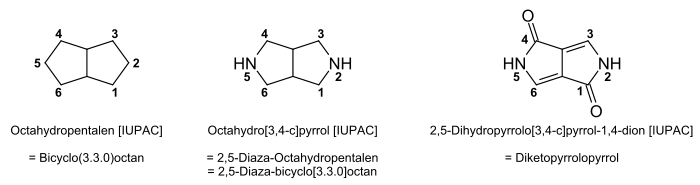 Nomenklatur
Nomenklatur
Der Grundkörper ist bei den benutzten Vertretern in 3- und 6-Position mit Aryl-Resten substituiert. Neuere DPP-Pigmente sind auch N-substituiert, womit eine höhere Farbbandbreite und veränderte Lösungseigenschaften erreicht werden können.[3]
Die weitere Substitution der Aryl-Reste bestimmt im Wesentlichen die Eigenschaften der wichtigsten Vertreter. Die Variante mit unsubstituierten Aryl-Resten ist im Colour Index unter C.I. Pigment Red 255 geführt.
Herstellung
Bernsteinsäurediester werden mit doppelt molaren Mengen geeignet substituierter Benzonitrilen mit starken Basen kondensiert. Das erhaltene Rohpigment wird durch Erhitzen in Lösemittel konditioniert (thermische Nachbehandlung). Durch eine formale Hydrolyse des Grundkörpers lässt sich die Struktur wieder auf die Bernsteinsäure zurückführen:

N-substituierte Aryldiketopyrrolopyrrole können durch die Kondensation von Lactonen mit Arylaminen bei Anwesenheit von Hilfsstoffen wie Dicyclohexylcarbodiimid (DCC) als leuchtend rote Pigmente dargestellt werden, die eine rote bis orangeroten Feststofffluoreszenz aufweisen.[3]
Wichtigste Vertreter
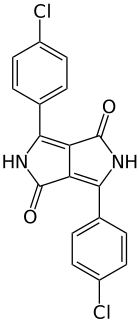
Der mit weitem Abstand wichtigste Vertreter dieser Pigmentgruppe ist C.I. Pigment Red 254, umgangssprachlich auch Pyrrolrot oder DPP-Rot genannt, das sich von C.I. Pigment Red 255 durch ein Cl-Atom in para-Stellung an beiden Aryl-Gruppen unterscheidet. Eine Phenyl- bzw. tert-Butyl-Gruppe führt zu C.I. Pigment Red 264 (DPP-Rubin) bzw. C.I. Pigment Orange 73 (DPP-Orange). Die drei letztgenannten Vertreter sind zwar auf dem Markt anzutreffen, werden aber im Gegensatz zum eher universell verwendeten DPP-Rot eher für spezifische Anwendungen verwendet.[4]
Eigenschaften
DPP-Pigmenten ergeben hochreine Farbtöne im Bereich von gelbstichigem Orange bis zu blaustichigem Violett bzw. Rubin (Farbton). Im Einzelnen decken die wichtigsten Vertreter die folgenden Farbtonbereiche ab:
- C.I. Pigment Orange 73 → Reines, rotstichiges Orange
- C.I. Pigment Red 255 → Reines, gelbstichiges Rot bzw. Scharlach
- C.I. Pigment Red 254 → Mittleres Rot
- C.I. Pigment Red 264 → Tiefes Rubin (Farbton)
DPP-Pigmente sind sehr beständig gegen Licht, Wetter, Lösemittel, Hitze und Chemikalien, so dass sie für hochwertige Formulierungen geeignet sind.[5][6]
Durch geeignete Substituenten können auch lösliche DPP hergestellt werden, die wegen ihrer großen Stokes-Verschiebung und sehr guten Fluoreszenzquantenausbeute in Farbstoff-Lasern oder Fluoreszenz-Solarkollektoren einsetzbar sind.[7]
Anwendungen
Die in der Öffentlichkeit bekannteste Anwendung ist der Automobillack. Diese Bekanntheit basiert im Wesentlichen auf dem prägnanten Farbton Ferrari-Rot, dessen Formulierungen zum Großteil auf C.I. Pigment Red 254 basieren. Im Bereich der hochwertigen Industrielacke werden DPP-Pigmente ebenfalls eingesetzt, hier aber hauptsächlich im hochwertigen Segment. Für die Innenanwendungen kommen meist preiswertere Azopigmente der Naphthol-AS-Gruppe zum Einsatz, wie z. B. C.I. Pigment Red 112 oder C.I. Pigment Red 170. Im Automobilbereich ist neben C.I. Pigment Red 254 insbesondere C.I. Pigment Red 264 von Bedeutung, da es aufgrund seiner höheren Transparenz auch für dunkelrote Metallic-Farbtöne eingesetzt werden kann.
Aufgrund ihrer hohen Hitze- und Wetterbeständigkeiten werden die DPP-Pigmente auch in Anwendungsgebieten, die hohe Anforderungen an die Temperaturbeständigkeit stellen, eingesetzt. Zu diesen gehören beispielsweise die Kunststoffmassenfärbung, Pulverlacke und Coil Coating (Bandlackierung) verwendet. Dort werden die Pigmente ebenfalls hauptsächlich für die Außenanwendung bevorzugt, während im Innenbereich billigere Pigmente eingesetzt werden.
Ein weiteres Einsatzgebiet sind Dispersionsfarben. Der Einsatz erfolgt hier ebenfalls zumeist im Außenbereich. Da Fassadenfarben aber weitaus weniger in der Lage sind, die darin enthaltenen Pigmente zu schützen, ist generell der Einsatz organischer Pigmente in einer solchen Matrix fragwürdig, worüber sich selbst die Hersteller nicht einig sind. Dennoch ist die Verwendung von DPP-Pigmenten, vor allem von C.I. Pigment Red 254 und C.I. Pigment Orange 73 gebräuchlich.[8][9]
Toxikologie
Vertreter wie C.I. Pigment Red 254 (CAS-Nummer: 84632-65-5) oder C.I. Pigment Orange 71 (CAS-Nummer: 84632-50-8) besitzen eine so geringe Toxizität (LD50 > 5.000 mg/kg oral bzw. > 2.000 mg/kg dermal), dass sie als Farbmittel Kunststoffen bis zu 1 % zugesetzt werden dürfen.[10]
Einzelnachweise
- Produktbroschüre Clariant
- Produktbroschüre CINIC.
- H. Langhals, T. Grundei, T. Potrawa, K. Polborn: Highly photostable organic fluorescent pigments – a simple synthesis of N-arylpyrrolopyrrolediones (DPP), In: Liebigs Ann. 1996, 679–682.
- W. Herbst, K.Hunger: Industrielle Organische Pigmente. Wiley-VCH 2004
- A. Goldschmidt, H.-J. Streitberger: BASF Handbuch Lackiertechnik. Vincentz Network 2002, ISBN 3-87870-324-4.
- W. Herbst, K.Hunger: Industrielle Organische Pigmente. Wiley-VCH 2004.
- H. Langhals, T. Potrawa, H. Nöth, G. Linti: Der Einfluß von Packungseffekten auf die Feststofffluoreszenz von Diketopyrrolopyrrolen (PDF; 1,8 MB), Angew. Chem. 1989, 101, 497–499; Angew. Chem. Int. Ed. Engl. 1989, 28, 478–480.
- Clariant, PA Division; Pigments for architectural coatings; 2007.
- Ciba; Pigments for decorative coatings; 2007.
- Verband der Mineralfarbenindustrie e.V.: Farbmittel für Lebensmittelbedarfsgegenstände und -verpackungen aus Kunststoffen. Aspekte der Produktsicherheit (PDF; 1,2 MB), 2002.