Delamanid
Delamanid (Handelsname Deltyba, Hersteller Otsuka Pharmaceutical) ist ein Arzneistoff aus der Gruppe der Dihydro-Nitroimidazooxazole, der in der Behandlung von multiresistenter Tuberkulose eingesetzt wird.[2]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
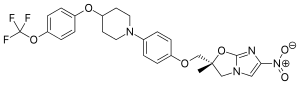 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Delamanid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C25H25F3N4O6 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
J04AK06 | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 534,49 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Anwendungsgebiet
Am 28. April 2014 erteilte die Europäische Kommission Delamanid als Deltyba eine Zulassung zur Behandlung der multiresistenten Tuberkulose in der gesamten Europäischen Union.[3] In der EU hat Deltyba den Status eines Orphan-Arzneimittels.[4] Es wird eingesetzt, wenn die Standardmedikamente Isoniazid (INH), Rifampicin (RMP), Ethambutol (EMB), Pyrazinamid (PZA) und Streptomycin (SM) versagen.[5]
Erstmals beschrieben wurde der Wirkstoff 2003 unter dem Entwicklungscode OPC-67683.[6]
Wirkungsmechanismus
Delamanid stört den Zellwandaufbau über eine Hemmung der Biosynthese von Mykolsäuren (IC50 = 0,036 μg/mL bzw. 0,021 μg/mL).[2]
Wechselwirkungen
Delamanid interagiert mit starken Induktoren des Leberenzyms Cytochrom P450 3A4, zum Beispiel Carbamazepin, sowie mit anderen Arzneimitteln, die die QT-Zeit verlängern.[7]
Aufnahme und Verteilung im Körper
Nach oraler Aufnahme wird nach 4–5 h die maximale Konzentration erreicht. Die Halbwertszeit nach Ende der Einnahme liegt bei 38 h. Nach 10–14 Tagen wird das Steady state (Gleichgewichtskonzentration) erreicht.[8]
Siehe auch
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Eintrag zu Delamanid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. Mai 2015.
- Zusammenfassung des EPAR für die Öffentlichkeit. EMA, April 2014, abgerufen am 4. April 2017., EU/1/13/875, abgerufen am 11. Mai 2020.
- Union Register of medicinal products for human use – Deltyba, EU/1/13/875, abgerufen am 12. Mai 2020.
- Medscape Deutschland: Multiresistente Tuberkulose: Bald zwei neue Wirkstoffe in der EU zugelassen?, 16. Januar 2014.
- Makoto Matsumoto, Hiroyuki Hashizume, Tatsuo Tomishige, Masanori Kawasaki, Hidetsugu Tsubouchi, Hirofumi Sasaki, Yoshihiko Shimokawa, Makoto Komatsu: OPC-67683, a Nitro-Dihydro-Imidazooxazole Derivative with Promising Action against Tuberculosis In Vitro and In Mice. In: PLoS Medicine. Band 3, Nr. 11, 2006, S. e466, doi:10.1371/journal.pmed.0030466 (englisch).
- D. Biermann: EU-Zulassung von Delamanid gegen multiresistente Tuberkulose, Pharmazeutische Zeitung, 14. Mai 2014.
- A. S. Xavier, M. Lakshmanan: Delamanid: A new armor in combating drug-resistant tuberculosis. In: Journal of Pharmacology & Pharmacotherapeutics. Band 5, Nummer 3, Juli 2014, S. 222–224, doi:10.4103/0976-500X.136121, PMID 25210407, PMC 4156838 (freier Volltext).