Cyanidin-3-O-glucosid
Cyanidin-3-O-glucosid ist ein Pflanzenfarbstoff (engl. plant pigment), der in zahlreichen Blütenblättern und Früchten vorkommt. Der Naturstoff gehört zur Gruppe der Anthocyane und besteht aus der farbgebenden Komponente Cyanidin sowie Glucose, die durch eine glykosidische Bindung verknüpft sind. Cyanidin-3-O-glucosid ist ein Kation (Flavyliumkation). In den Pflanzen liegt die chemische Verbindung als Salz mit den Anionen von Carbonsäuren vor. Das mit Chlorwasserstoff (Salzsäure) erzeugte Chlorid diente zur Reinigung und Isolierung.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
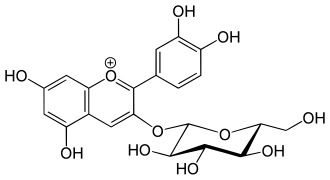 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Cyanidin-3-O-glucosid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C21H21ClO11 | ||||||||||||||||||
| Kurzbeschreibung |
violettes Pulver (Chlorid)[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 484,84 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest (Chlorid)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Geschichte
Das Glucosid wurde von Richard Willstätter und E. K. Bolton in den Blütenblättern der Winteraster (Chrysanthemum indicum L.) nachgewiesen und als Chlorid isoliert.[2] Die Autoren nannten es daher Chrysanthemin. Es erwies sich als identisch mit dem Anthocyan Asterin.[3]
Vorkommen
Abgesehen von den oben erwähnten Blüten, kommt Cyanidin-3-O-glucosid in vielen Früchten und Beeren vor, z. B. in wilden Erdbeeren (Fragaria vesca L.) und Süßkirschen (Prunus avium L.), der Blauen Heckenkirsche (Lonicera caerulea L.). Weintrauben enthalten das Glucosid neben weiteren Anthocyanen. So gelangt es auch in Traubensäfte und Rotweine.[4][5][6]
 Aus Chrysanthemum indicum wurde das Glucosid erstmals isoliert
Aus Chrysanthemum indicum wurde das Glucosid erstmals isoliert Cyanidin-3-O-glucosid ist an der roten Färbung der Süßkirsche beteiligt
Cyanidin-3-O-glucosid ist an der roten Färbung der Süßkirsche beteiligt
Gewinnung und Darstellung
Die erste Synthese von Cyanidin-3-O-glucosid (als Chlorid) wurde von Shinzo Murakami, Alexander Robertson und Robert Robinson im Jahr 1931 mitgeteilt.[7]
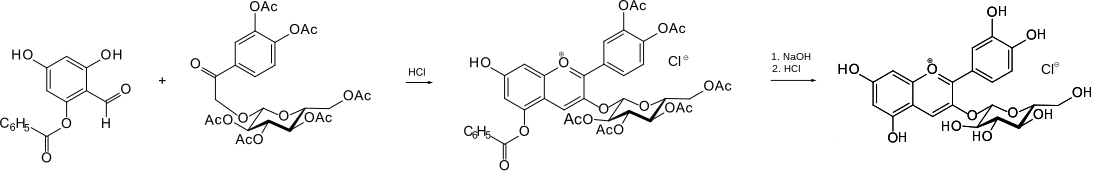
Diese Synthese beruhte auf dem für die Aglykone Pelargonidin und Cyanidin beschriebenen Prinzip durch Kondensation zweier molekularer Bausteine, die zum Teil geschützte OH-Gruppen enthalten (Allan-Robinson-Kondensation). Für die Synthese des Glucosids wurde die OH-Gruppe des zweiten Bausteins durch einen Glucosylrest ersetzt. Nach der Kondensation zum Flavyliumsalz wurden die Acyl-Schutzgruppen durch Behandeln mit Natronlauge entfernt. Bei der Neutralisation mit Salzsäure entstand das Cyanidin-3-O-glucosidchlorid.
Eine neuere Synthese ging vom (+)-Catechin aus.[8]
-Catechin.svg.png.webp)
Verwendung
Cyanidin-3-O-glucosid ist unter anderem der Hauptbestandteil der Anthocyanine in den Schalen schwarzer Sojabohnen. Der Extrakt daraus wird unter dem Namen Kuromanin (registriertes Warenzeichen) als die Sehfunktion verbesserndes Mittel (Visual Function Improving Agent) gehandelt. Für diese Verwendung wurde das Präparat patentiert.[9]
Biologische Bedeutung
Cyanidin-3-O-glucosid kann als Antioxidans gegen „Oxidativen Stress“ wirken. Es fängt freie Radikale ab, hemmt Entzündungen und soll gegen Herzkrankheiten und sogar Krebs vorbeugen. Aus diesem Grund werden Lebensmittel mit hohem Gehalt an Cyanidinglucosid und anderen Anthocyanidinen empfohlen.[10] Die Beeren der Blauen Heckenkirsche (Lonicera caerulea L.) enthalten einen hohen Anteil an Polyphenolen, hauptsächlich Cyanidin-3-O-glucosid. Nach den Autoren soll die Einnahme der Beeren bzw. des Glucosids einen lang anhaltenden Schutz des Herzens bewirken. Dies wird auf eine Veränderung des Mikrobioms zurückgeführt.[11]
Nachweis
Extrakte pflanzlichen Materials wurden und werden durch chromatographische Methoden analysiert. Zur Identifizierung dienen die üblichen Methoden der instrumentellen Analytik, wie Massenspektrometrie, NMR-Spektroskopie. Früher wurden chemische Farbreaktionen zum Nachweis herangezogen, z. B. mit Eisen(III)-chlorid. Diese sind jedoch weniger spezifisch. Beispielsweise entsteht eine blaue Farbe, wenn Cyanidinglucosid mit einer wässrigen Lösung von Natriumcarbonat behandelt wird.
Einzelnachweise
- Datenblatt Cyanidin-3-O-glucosid bei Sigma-Aldrich, abgerufen am 4. Januar 2022 (PDF).
- Richard Willstätter, E. K. Bolton: Justus Liebigs Annalen der Chemie, Jg. 1917, Bd. 412, S. 136
- Robert Robinson, Richard Willstätter: In: Berichte der deutschen Chemischen Gesellschaft, Jg. 1928, Bd. 61, S. 2503
- Emma Cantos, Juan Carlos Espín, Francisco A. Tomás-Barberán: Varietal Differences among the Polyphenol Profiles of Seven Table Grape Cultivars Studied by LC/DAD/MS-MS. In: Journal of Agricultural and Food Chemistry Jg. 2002, Bd. 50, Heft 20, S. 5691–5696. doi:10.1021/jf0204102.
- Nicolas Landrault, Patrick Poucheret, Patrice Ravel, Francis Gasc, Gérard Cros, Pierre-Louis Teissedre: Antioxidant Capacities and Phenolics Levels of French Wines from Different Varieties and Vintages. In: Journal of Agricultural and Food Chemistry Jg. 2001, Bd. 49, Heft 7, S. 3341–3348. doi:10.1021/jf010128f.
- Silvia Mangani, Giacomo Buscioni, Luca Collina, Eugenio Bocci, Massimo Vincenzini: Effects of Microbial Populations on Anthocyanin Profile of Sangiovese Wines Produced in Tuscany, Italy. In: American Journal of Enology and Viticulture, Jg. 2011, Bd. 62, Dezember-Heft, S. 487–494; Vorveröffentlichung 31. August 2011; doi:10.5344/ajev.2011.1104.
- Shinzo Murakami, Alexander Robertson, Robert Robinson: Experiments on the synthesis of anthocyanins. Part VI. A synthesis of chrysanthemin chloride. In: Journal of the Chemical Society. Jg. 1931, S. 2665–2671. doi:10.1039/JR9310002665.
- Tadao Kondo, Kin-ichi Oyama, Saki Nakamura, Daisuke Yamakawa, Kazunari Tokuno, and Kumi Yoshida: Novel and Efficient Synthesis of Cyanidin 3-O-d-Glucoside from (+)-Catechin via a Flav-3-en-3-ol as a Key Intermediate. In: Organic Letters, Jg. 2006, Bd. 8, Heft 16, S. 3609–3612. doi:10.1021/ol0614976.
- Japanisches Patent Nr. JPB0004247833
- Sandra Maria Barbalho, Alda Maria M. Bueno Ottoboni, Adriana Maria Ragassi Fiorini, Élen Landgraf Guiguer, Claudia Cristina Teixeira Nicolau, Ricardo de Alvares Goulart, Uri Adrian Prync Flato. Grape juice or wine: which is the best option?. In: Critical Reviews in Food Science and Nutrition, Jg. 2020, Bd. 60, Heft 22, S. 3876–3889, doi:10.1080/10408398.2019.1710692.
- Mirella Trinei, Andrea Carpi, Roberta Menabo, Mariangela Storto, Monica Fornari, Alessandra Marinelli, Simone Minardi, Mirko Riboni, Francesca Casciaro, Fabio DiLisa, Katia Petroni, Chiara Tonelli, Marco Giorgio: Dietary intake of cyanidin-3-glucoside induces a long-lasting cardioprotection from ischemia/reperfusion injury by altering the microbiota. In: The Journal of Nutritional Biochemistry, Jg. 2021, 108921. doi:10.1016/j.jnutbio.2021.108921.