Clostridium perfringens α-Toxin
Clostridium perfringens α-Toxin ist ein Enzym aus der Gruppe der Phospholipasen von Clostridium perfringens und ein mikrobielles Exotoxin.
| Phospholipase C | ||
|---|---|---|
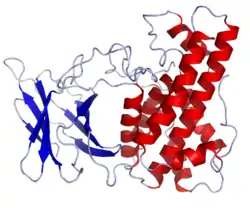 | ||
| nach PDB 1CA1 | ||
| Andere Namen |
Alpha-toxin, Hämolysin, Lecithinase, Phosphatidylcholin-Cholinphosphohydrolase | |
| Masse/Länge Primärstruktur | 398 Aminosäuren, 45.598 Da | |
| Bezeichner | ||
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 3.1.4.3 | |
| Orthologe (Clostridium perfringens) | ||
| Entrez | 29569865 | |
| UniProt | Q9RF12
| |
| PubMed-Suche | 29569865 | |
Eigenschaften
Das α-Toxin von C. perfringens ist eine Phospholipase C und bindet Zinkionen. Es ist der Haupt-Virulenzfaktor von C. perfringens.[1] Es wirkt bei Eukaryoten als Hämolysin. Als Phospholipase C hydrolysiert es Phosphatidylcholin und Sphingomyelin, wodurch es zur Lyse der Zellmembran kommt. Das freigesetzte Diacylglycerol wirkt als sekundärer Botenstoff und aktiviert den Arachidonsäure-Signalweg und die Proteinkinase C, wodurch in Folge weitere Phospholipasen aktiviert werden und die Zellmembran weiter abgebaut wird. Der N-terminale Bereich der Aminosäuren 1–250 enthält die Enzymaktivität, während der C-terminale Bereich der Aminosäuren 251–370 die Bindung an die Zellmembran vermittelt.[2] α-Toxin ist strukturell mit den Phospholipasen aus Bacillus cereus, Clostridium bifermentans und Listeria monocytogenes verwandt.[3] Der C-terminale Bereich ist zudem entfernter mit der pankreatischen Lipase, der Sojabohnen-Lipoxygenase und Synaptotagmin I verwandt.[4]
Die Phospholipase C katalysiert folgende Reaktion:
Phosphatidylcholin + H2O → 1,2-Diacyl-sn-glycerol + Phosphocholin
Anwendungen
Clostridium perfringens α-Toxin wird als Antigen in Impfstoffen gegen Infektionen mit C. perfringens untersucht.[5]
Weblinks
Einzelnachweise
- M. M. Awad, A. E. Bryant, D. L. Stevens, J. I. Rood: Virulence studies on chromosomal alpha-toxin and theta-toxin mutants constructed by allelic exchange provide genetic evidence for the essential role of alpha-toxin in Clostridium perfringens-mediated gas gangrene. In: Molecular microbiology. Band 15, Nummer 2, Januar 1995, S. 191–202, PMID 7746141.
- M. Oda, Y. Terao, J. Sakurai, M. Nagahama: Membrane-Binding Mechanism of Clostridium perfringens Alpha-Toxin. In: Toxins. Band 7, Nummer 12, Dezember 2015, S. 5268–5275, doi:10.3390/toxins7124880, PMID 26633512, PMC 4690130 (freier Volltext).
- J. Sakurai, M. Nagahama, M. Oda: Clostridium perfringens alpha-toxin: characterization and mode of action. In: Journal of biochemistry. Band 136, Nummer 5, November 2004, S. 569–574, doi:10.1093/jb/mvh161, PMID 15632295.
- C. E. Naylor, J. T. Eaton, A. Howells, N. Justin, D. S. Moss, R. W. Titball, A. K. Basak: Structure of the key toxin in gas gangrene. In: Nature structural biology. Band 5, Nummer 8, August 1998, S. 738–746, doi:10.1038/1447, PMID 9699639.
- M. Nagahama: Vaccines against Clostridium perfringens alpha-toxin. In: Current pharmaceutical biotechnology. Band 14, Nummer 10, 2013, S. 913–917, PMID 24372250.