Chromocen
Chromocen, mit der Formel [Cr(C5H5)2], ist eine metallorganische Verbindung aus der Familie der Metallocene. Die Summenformel wird oft mit [Cr(Cp)2] abgekürzt. Es bildet einen dem Ferrocen analogen Sandwichkomplex, folgt aber nicht der 18-Elektronen-Regel, da es nur 16 Valenzelektronen besitzt. Chromocen wurde erstmals 1953 beschrieben.[5]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
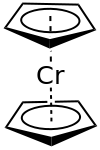 | ||||||||||||||||
| Ekliptische Konformation | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Chromocen | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C10H10Cr | |||||||||||||||
| Kurzbeschreibung |
roter kristalliner Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 182,18 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,43 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
nahezu unlöslich[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Herstellung
Chromocen wird durch Reaktion von Chrom(II)-chlorid mit Cyclopentadienylnatrium, üblicherweise in Tetrahydrofuran (THF) als Lösungsmittel, hergestellt. Im ersten Schritt wird zunächst das wasserfreie Chrom(II)-chlorid synthetisiert:[6]
Auch die direkte Herstellung aus Chrom(II)-chlorid, Cyclopentadien und Natrium ist möglich:[7]
Das analoge Decamethylchromocen, Cr[C5(CH3)5]2, wird analog der ersten Reaktion unter Verwendung von Pentamethylcyclopentadienyllithium, LiC5(CH3)5 hergestellt.
Eigenschaften
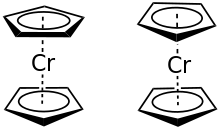
Chromocen ist ein roter kristalliner Feststoff. In der Kristallstruktur von Chromocen wurde mittels Röntgenstrukturanalyse die mittlere Cr–C-Bindungslänge mit 215,1(13) pm ermittelt.[8][9] Wie im Ferrocen sind auch im Chromocen die Cyclopentadienyl-Ringe auf Deckung (ekliptisch) und nicht gestaffelt angeordnet.[9] Die Dissoziationsenergie für die Cp–Cr-Bindung wird, je nach Literatur, mit 179 kJ·mol−1 bzw. 279 kJ·mol−1 angegeben.[9][10] Der mittlere Abstand zwischen den Ringen liegt bei 370 pm.[11] Chromocen ist an der Luft und gegenüber Wasser sehr reaktiv[1][9] und kann sich unter Umständen bei Luftkontakt spontan entzünden.
Verwendung
Auf silikatische Trägersubstanzen aufgebrachtes Chromocen fungiert als Katalysator bei der Polymerisation von Ethylen und anderen 1-Alkenen.[12][13] In den 1960ern wurde dieser Prozess von Union Carbide zur Polymerisation von Ethylen entwickelt.[14][15] Dabei zersetzt sich das Chromocen an der silikatischen Oberfläche unter Bildung von hochreaktiven organometallischen Zentren, welche die katalytische Wirksamkeit ergeben. Die Struktur und Wirkungsweise des Union Carbide Katalysators wurde von Janet Blümel eingehend untersucht.[16] Chromocen basierte Katalysatoren haben, gegenüber Ziegler-Katalysatoren, welche aluminiumorganische Verbindungen enthalten, den Vorteil, dass das hergestellte Polyethylen nur eine geringe Geruchsbelästigung zeigt.[17] Alternativ kann als Substrat (Trägersubstanz) auch Porenbeton eingesetzt werden.[18]
Einzelnachweise
- Christoph Elschenbroich: Organometallchemie. B. G. Teubner Verlag, 2008, ISBN 978-3-8351-0167-8 (S. 452 in der Google-Buchsuche).
- E. Weiss, E. O. Fischer: Zur Kristallstruktur von Di-cyclopentadienyl-chrom(II). In: Z. Anorg. Allg. Chem. Band 284, 1956, S. 69–72, doi:10.1002/zaac.19562840109.
- Datenblatt Bis(cyclopentadienyl)chromium (PDF) bei Strem, abgerufen am 10. Januar 2012.
- Datenblatt Bis(cyclopentadienyl)chromium(II) bei Sigma-Aldrich, abgerufen am 4. Dezember 2011 (PDF).
- E. O. Fischer, W. Hafner: Di-cyclopentadienyl-chrom. In: Zeitschrift für Naturforschung B. 8, 1953, S. 444–445 (online).
- Chromocen (PDF, 117 kB)
- Patent EP0652224B1: Process for the preparation of metallocenes in a one-step synthesis.
- Kevin R. Flower, Peter B. Hitchcock: Crystal and molecular structure of chromocene (η5-C5H5)2Cr. In: Journal of Organometallic Chemistry. 1996, 507. S. 275–277. doi:10.1016/0022-328X(95)05747-D.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1699–1700.
- James E. Huheey, Ellen A. Keiter, Richard Keiter: Anorganische Chemie: Prinzipien von Struktur und Reaktivität. de Gruyter Verlag, 2003, ISBN 3-11-017903-2 (S. 797 in der Google-Buchsuche).
- F. Jellinek: Die Struktur des Osmocens. In: Zeitschrift für Naturforschung B. 14, 1959, S. 737–738 (online).
- Patent DE4306105A1: Modifizierte geträgerte Chromocen-Katalysatorsysteme.
- Manfred Dieter Lechner, Klaus Gehrke, Eckhard H. Nordmeier: Makromolekulare Chemie: ein Lehrbuch für Chemiker, Physiker. (S. 93 in der Google-Buchsuche).
- Ralf Alsfasser, Erwin Riedel, H. J. Meyer: Moderne Anorganische Chemie. de Gruyter Verlag, ISBN 978-3-11-019060-1 (Seite 708 in der Google-Buchsuche).
- Dirk Steinborn: Grundlagen der metallorganischen Komplexkatalyse. Vieweg + Teubner, 2007, ISBN 978-3-8348-0581-2 (S. 158 in der Google-Buchsuche).
- Katalysator-Träger-Wechselwirkungen: Struktur und Wirkungsweise des Union Carbide-Katalysators (Chromocen/Silica) (PDF, 207 kB)
- Patent EP1109859B1: Low odor polyethylene blends.
- Patent DE10314369B4: Production of polymerization catalyst, used in polymerization of olefins, including styrene, especially ethylene, uses porous cement concrete as support for application of metallocene derivative.
