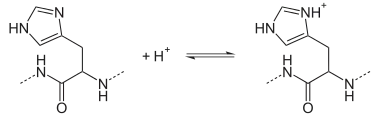Bohr-Effekt
Der Bohr-Effekt bezeichnet das Sinken der Affinität von Hämoglobin (Hb) zu Sauerstoff, wenn der pH-Wert sinkt oder die CO2-Konzentration steigt. Gemeinsam mit der kooperativen Bindung von Sauerstoff und dem im Rapoport-Luebering-Zyklus durch das Enzym Bisphosphoglyceratmutase gebildeten allosterischen Effektor 2,3-Bisphosphoglycerat gewährleistet diese Eigenschaft die optimale Funktion des Hämoglobins als Sauerstofftransporter.
Der Effekt ist nach seinem Entdecker, dem dänischen Physiologen Christian Bohr (1855–1911), Vater des Physikers Niels Bohr, benannt.
Grundlagen
Das Hämoglobin vermittelt die Aufgabe des Blutes, Sauerstoff von der Lunge zu den verbrauchenden Organen zu transportieren. Hierzu muss das Hämoglobin in der Lage sein, in den Lungenkapillaren den dort reichlich in der Atemluft vorhandenen Sauerstoff zu binden und ihn in den Zielorganen wieder abzugeben, wo er für den Energiestoffwechsel gebraucht wird.
Hämoglobin kommt in zwei Konformationen vor: der tense Form (T), die Sauerstoff schlecht bindet, und der relaxed Form (R), die Sauerstoff gut bindet. Beide Formen stehen miteinander in einem Gleichgewicht, das abhängig von der Umgebung zur einen oder anderen Seite verschoben ist.
Für die Steuerung der Sauerstoffbindung und -freisetzung sind mehrere Eigenschaften des Hämoglobins zuständig. Der Bohr-Effekt gewährleistet eine bevorzugte Freisetzung von Sauerstoff in stoffwechselaktiven Geweben. Dabei spielen im Wesentlichen zwei Faktoren eine wichtige Rolle: Stoffwechselaktive Gewebe, wie beispielsweise Muskeln bei sportlicher Aktivität, weisen einen erhöhten CO2-Gehalt und einen erniedrigten pH-Wert auf. Beides ist durch Anreicherung von Stoffwechselprodukten zu erklären: Kohlenstoffdioxid entsteht bei der Zellatmung und reagiert, katalysiert durch das Enzym Carboanhydrase, mit Wasser zu Hydrogencarbonat und Protonen – der pH-Wert sinkt:
Die Senkung des pH-Wertes wird verstärkt, wenn für die Zellatmung nicht genügend Sauerstoff zur Verfügung steht. Dann kann das in der Glykolyse gewonnene Pyruvat nicht über den Citrat-Zyklus abgebaut werden. Es kommt durch Stillstand des Citrat-Zyklus gewissermaßen zu einem „Rückstau“. Damit der Rückstau nicht auch die Glykolyse beeinträchtigt und die Energiegewinnung gänzlich lahmlegt, wird das Pyruvat unter Protonenabgabe zu Lactat reduziert, was zu einer weiteren Ansäuerung des Blutes führt. Diesen Vorgang beobachtet man beispielsweise beim anaerob arbeitenden Muskel.
Wirkung des pH-Werts
An dem pH-abhängigen Effekt sind zum einen die Histidinreste 122 der α-Untereinheiten und 146 der β-Untereinheiten des Hämoglobins beteiligt und zum anderen die α-Aminogruppen der N-terminalen Aminosäuren der α-Untereinheiten.
Die pKs-Werte dieser Gruppen liegen in der Nähe von 7. Die pKs-Werte sind in der T-Form höher als in der R-Form. Ein höherer pKs-Wert bedeutet, dass die Protonenaufnahme thermodynamisch günstiger ist; Hintergrund ist hier, dass die positive Ladung der Protonen in der T-Konformation Salzbrücken stabilisieren kann, die es in der R-Konformation nicht gibt.
Der normale Blut-pH-Wert ist 7,4. Wenn der pH-Wert lokal so stark sinkt, dass er sich dem pKs-Wert dieser Gruppen annähert, führt dies zu einer rasch zunehmenden Protonierung. Weil die pKs-Werte in der T-Form höher sind als in der R-Form, verschiebt der niedrige pH-Wert das Gleichgewicht zwischen T-Form und R-Form auf die Seite der T-Form, was mit einer niedrigeren durchschnittlichen Sauerstoffaffinität und folglich mit Sauerstoffabgabe einhergeht. Die Senkung des pH-Werts um 0,2 hat bereits eine Abnahme der Sauerstoffaffinität um etwa 20 % zur Folge.
Wirkung des CO2-Partialdrucks
Neben dem oben beschriebenen pH-senkenden Effekt des Kohlenstoffdioxid spielt noch ein zweiter Mechanismus eine Rolle. Das Hydrogencarbonat reagiert reversibel mit endständigen Aminogruppen des Hämoglobins zu Carbamatgruppen.
Auch das führt zur Verschiebung des Gleichgewichts zwischen T-Form und R-Form auf die Seite der T-Form und damit zur Verringerung der durchschnittlichen Sauerstoffaffinität. Die Bildung von Carbamatgruppen ist außerdem zu einem kleinen Teil (zirka 5–7 %) am CO2-Rücktransport zur Lunge beteiligt.
Umkehr
In der Lunge ist die Situation umgekehrt. Da der Kohlenstoffdioxid-Partialdruck im Blut größer ist als in der Luft, tritt CO2 aus dem Blut in die Luft über. Weil CO2 aus dem chemischen Gleichgewicht entfernt wird, reagiert Hydrogencarbonat mit Protonen zu CO2 und Wasser. Die dabei verlorengehenden Protonen steigern den pH-Wert.
Ebenfalls aufgrund des chemischen Gleichgewichts hydrolysieren die Carbamatgruppen wieder zu Aminogruppen und CO2. All dies begünstigt den Übergang des Hämoglobins von der T-Form zur R-Form, die hochaffin Sauerstoff bindet.
Therapeutische Bedeutung
Eine zielgerichtete Anwendung des Bohr-Effekts wird in der Buteiko-Methode versucht.
Analytik
Die lokale Konzentration von Hämoglobin ohne Sauerstoff (Desoxyhämoglobin) kann in vivo durch funktionelle Magnetresonanztomographie nachgewiesen werden.[1][2] Bei Steigerung der Durchblutung sinkt die lokale Konzentration an Desoxyhämoglobin.[1] Diese Methode wird als Blood Oxygen Level-Dependent Contract (BOLD-Effekt) bezeichnet.[1]
Siehe auch
Literatur
- Berg, Stryer, Tymoczko: Biochemie. Spektrum Akademischer Verlag, 2007, ISBN 978-3-8274-1800-5
Einzelnachweise
- Jan Mayer: Mentales Training. Springer-Verlag, 2011, ISBN 978-3-642-13762-4, S. 211.
- Robert C. Eklund: Encyclopedia of Sport and Exercise Psychology. SAGE Publications, 2013, ISBN 978-1-483-36870-2, S. 130.