Aminopeptidasen
Aminopeptidasen sind Enzyme, die die Abspaltung einzelner Aminosäuren vom N-terminalen Ende eines Proteins katalysieren. Aminopeptidasen kommen in allen Lebewesen vor. Im Menschen wurden bisher etwa 20 von ihnen entdeckt. Außer zur Proteinreifung dienen sie im menschlichen Stoffwechsel auch zur Regulierung des Peptidhormonspiegels und der Verdauung von Proteinen im Darm.
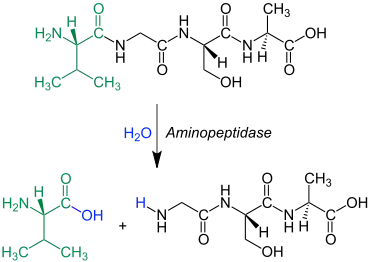
Aminopeptidasen gehören zur Gruppe der Exopeptidasen, d. h. der eiweißspaltenden Enzyme, welche Proteine an endständigen Peptidbindungen aufspalten. In den meisten Fällen gehören Aminopeptidasen zu den Metalloproteasen. Für alle natürlichen Aminosäuren existieren spezifische Aminopeptidasen, welche nur diese am N-terminalen Ende eines Proteins abspalten (Arginin-Aminopeptidase, Leucin-Aminopeptidase usw.). Viele dieser Enzyme sind fest an die Zellwand gebunden.[1]
Katalysierte Reaktionen
Peptidasen zerlegen Proteine durch Hydrolyse der Peptidbindungen. Während Endopeptidasen Eiweiße innerhalb deren Moleküle spalten, zerlegen Exopeptidasen diese vom „Molekülrand“ her. Aminopeptidasen speziell greifen am N-terminalen oder Amino-terminalen Ende der Peptide an und spalten dabei eine einzelne Aminosäure ab (wie Aminoacyl-Peptidhydrolasen und Iminoacyl-Peptidhydrolasen).[2]
Industrielle Anwendung
Aminopeptidase kann in der enzymatischen, kinetischen Racematspaltung von DL-2-Arylglycinamiden eingesetzt werden.[3] Bei Einsatz einer L-Aminopeptidase als Katalysator wird das L-2-Arylglycinamid enantioselektiv zu L-2-Arylglycin hydrolysiert, während D-2-Arylglycinamid unverändert bleibt.
Einzelnachweise
- H. Weber: Mikrobiologie der Lebensmittel. Milch und Milchprodukte, 1996, Behr's Verlag, ISBN 386022235X.
- Wissenschaft-Online-Lexika: Eintrag zu Aminpeptidasen im Lexikon der Biochemie (Memento des Originals vom 3. Dezember 2015 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis..
- R. A. Sheldon: The Industrial Synthesis of Optically Active Compounds, in Miklós Simonyi (Herausgeber), Problems and Wonders if Chiral Molecules, Akadémiai Kiadó, Budapest, 1990, S. 349–386, ISBN 9630558815.