Acetorphin
Acetorphin ist ein starkes Opioid-Analgetikum, bis zu 8700-mal stärker schmerzstillend wirksam als Morphin und unter gleichen Testbedingungen 2,7-mal potenter als Etorphin (Propylorvinol).
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
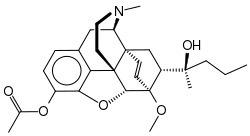 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Acetorphin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C27H35NO5 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Wirkmechanismus | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 453,57 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Acetorphin ist der Essigsäureester von Etorphin. Etorphin kommt als sehr potentes Schmerzmittel (Analgetikum) und Betäubungsmittel (Anästhetikum) in der Veterinärmedizin unter dem Handelsnamen Immobilon in erster Linie für die Ruhigstellung (Sedierung) von großen Tieren wie Elefanten, Giraffen und Nashörnern zum Einsatz.
Geschichte
Acetorphin wurde Anfang der 1960er Jahre von der Reckitt Forschungsgruppe[2] entwickelt, die auch Etorphin entwickelt hatte. Acetorphin wurde wie Etorphin und Dihydroetorphin mit der gleichen Absicht entwickelt, Opioid-Analgetika ohne unerwünschte Nebenwirkungen (Toleranzentwicklung, Suchtentwicklung) zu erhalten. Die hohe Potenz dieser Verbindungen stand weder im Fokus der Entwicklung noch wurde sie erwartet, weckte dann aber das Interesse, weil sich die Substanzen als starke Beruhigungsmittel zur Immobilisierung großer Tiere in der Tiermedizin eigneten. Trotz einiger Vorteile gegenüber Etorphin, zum Beispiel den geringeren toxischen Nebenwirkungen bei Giraffen, wurde Acetorphin als Tierarzneimittel nie populär und Etorphin (zusammen mit anderen Beruhigungsmitteln wie Carfentanil, Thiafentanil (A-3080) und Azaperon) gelten bei derartigen Anwendungen als Mittel der Wahl.
Sonstiges
Die Steigerung der Potenz von Etorphin (n-Propylorvinol) durch Veresterung der phenolischen OH-Gruppe um das 2,7fache ist gegenläufig zu der Beobachtung, dass bei allen anderen Etorphin-Analoga eine analoge Veresterung zu einer teilweise starken Verringerung der Potenz führt. Beispielsweise ist Isoamylorvinol als freies Phenol 9200 mal potenter als Morphin und fast 2,9 mal potenter als Etorphin. Dagegen hat Isoamylorvinol-3-acetat eine 7-fach geringere Potenz als Isoamylorvinol und nur noch die 0,4-fache Etorphin-Potenz, bzw. die 1300-fache Morphinpotenz.[2][3] Beim Morphin ändert eine Acetylierung (bzw. allgemein Veresterung) der phenolischen OH-Gruppe die Potenz im Allgemeinen nicht.
Anfang der 1960er Jahre war, damals noch ohne Kenntnisse über Opioidrezeptoren und biochemische Wirkmechanismen von Opioiden, das Ziel der Entwicklung durch Strukturabwandlung Substanzen zu erzeugen, die sich bei starker analgetischer Wirkung durch eine geringere Suchtentwicklung im Vergleich zu den bis dahin bekannten Opioiden auszeichnen sollten. Durch Zufall erhielt man Verbindungen (Etorphin, Dihydroetorphin), welche diesen Erwartungen entsprachen und zusätzlich eine extrem hohe, bis dahin nicht gekannte Potenz besaßen. Wegen der hohen Wirkstärke hielt man diese Verbindungen damals aber für die Humanmedizin für gänzlich ungeeignet und untersuchte sie nicht detailliert genug (insbesondere auch bei chronischer Gabe). Daher erkannte man das vergleichsweise geringe physische Suchtpotential von Etorphin und Dihydroetorphin damals nicht. Erst Ende der 1970er Jahre wurde diese Eigenschaft entdeckt.[4][5][6][7] Etorphin und Dihydroetorphin dienten von da an in der experimentellen Pharmakologie, um biochemische Mechanismen der Opioidabhängigkeit zu untersuchen.
Rechtsstatus
Acetorphin unterliegt in Deutschland dem Betäubungsmittelgesetz und findet sich als nicht verkehrsfähiges Betäubungsmittel in Anlage I zum Gesetz.
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Bentley, K. W.; Hardy, D. G. (1967). Novel analgesics and molecular rearrangements in the morphine-thebaine group. 3. Alcohols of the 6,14-endo-ethenotetrahydrooripavine series and derived analogs of N-allylnormorphine and -norcodeine. Journal of the American Chemical Society 89 (13): 3281–3292, doi:10.1021/ja00989a032.
- Robert E. Lister, Structure-activity requirements in some novel thebaine-derived analgesics. J. Pharm. Pharmacol. 16: 1964, 364–366.
- Mao Huang, Bo-Yi Qin Physical dependence of Dihydroetorphine in Mice and Monkeys. Acta Pharmaceutica Sinica 3(2): 1982, 81–84.
- B.Y. Qin, M. Huang, Y.C. Zhang, H. Miao Comparison of the dependence potential of Dihydroetorphine, Etorphine an Morphine, Regulatory Peptides 54: 1994, 237–238.
- M. Huang, D.X. Wang, B.Y. Qin Dihydroetorphine, a potent opioid with low dependence potential, Regulatory Peptides 53: 1994, 81–82.
- B.Y. Qin, D.X. Wang, M. Huang The application of Dihydroetorphine to detoxification of Heroin addicts Regulatory Peptides 53: Suppl.1, 1994, 293–294.