3-Hydroxypropionat/4-Hydroxybutyratzyklus
Der 3-Hydroxypropionat/4-Hydroxybutyratzyklus ist ein biochemischer Zyklus, der es einigen Archaea erlaubt, Kohlenstoffdioxid in Form von Bicarbonat (HCO3−) zu assimilieren. Der Zyklus kann in zwei Hälften unterteilt werden: Zunächst werden aus Acetyl-CoA sowie zwei Molekülen Bicarbonat ein Molekül Succinyl-CoA gebildet. Im zweiten Teil entstehen daraus dann über 4-Hydroxybutyrat zwei Moleküle Acetyl-CoA, wobei das eine für den nächsten Durchlauf verwendet wird. Der Zyklus verdankt seinen Namen, da als Intermediate 3-Hydroxypropionat bzw. 4-Hydroxybutyrat gebildet werden.
Vorkommen
Der Stoffwechselweg wurde in thermoacidophilen Archaea der Ordnung Sulfolobales (zum Beispiel Stygiolobus azoricus) nachgewiesen, Vertreter der Abteilung Crenarchaeota.[1] Diese Mikroorganismen sind entweder mikroaerophil oder im Falle von Stygiolobus strikt anaerob.[2]
Es steht noch zur Debatte, ob der Zyklus auch in mesophilen, marine Gruppe-I Crenarchaeota betrieben wird.[2] Diese sind häufig vorkommende Meeresarcheen, die unter mesophilen Bedingungen wachsen.
Biochemie
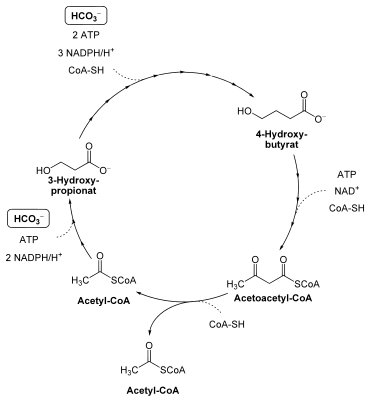
Ausgehend von Acetyl-CoA wird in zwei Reaktionsschritten Malonat-Semialdehyd gebildet, welches durch eine Malonat-Semialdehyd-Reduktase in 3-Hydroxypropionat reduziert wird. Für diese Reaktionsschritte werden zwei Moleküle NADPH, ein Molekül ATP und ein Molekül Bicarbonat benötigt. 3-Hydroxypropionat wird über mehrere Intermediate zu Succinyl-CoA umgesetzt, daran beteiligt ist auch ein Vitamin-B12-abhängiges Enzym, die Methylmalonyl-CoA-Mutase.
Aus Succinyl-CoA entsteht katalysiert dann eine Succinat-Semialdehyd-Reduktase unter NADPH-Verbrauch die Bildung von 4-Hydroxybutyrat aus Succinat-Semialdehyd. Die Bildung von 4-Hydroxybutyrat aus 3-Hydroxypropionat benötigt drei Moleküle NADPH, zwei Moleküle ATP, ein weiteres Molekül Bicarbonat und Coenzym A. Schließlich wird 4-Hydroxybutyrat zu Acetoacetyl-CoA unter Verbrauch je eines Moleküls ATP und Coenzym A sowie NAD+ umgesetzt. Dieses wird durch eine Acetoacetyl-CoA β-Ketothiolase in zwei Moleküle Acetyl-CoA gespaltet, so dass sich hier der Zyklus schließt und ein Acetyl-CoA freigesetzt wird.
Die Gesamtbilanz für die Bildung von einem Molekül Acetyl-CoA lautet folglich (ohne Bezug auf Coenzym A):
Biologische Bedeutung
Dieser Stoffwechselweg wurde erst kürzlich entdeckt und stellt eine Variante des 3-Hydroxypropionatzyklus dar. Bis zur Bildung von Succinyl-CoA entsprechen sich die beiden Zyklen weitestgehend. Jedoch sind die darin beteiligten Enzyme phylogenetisch nicht verwandt und scheinen sich unabhängig voneinander entwickelt zu haben.[3]
Der Kreislauf deckt sich auch teilweise mit dem kürzlich entdeckten Dicarboxylat/4-Hydroxybutyratzyklus, der auch von Vertretern der Crenarchaeota betreiben wird. Die Bildung von Acetoacyl-CoA aus Succinyl-CoA verläuft in beiden Zyklen identisch.
Die Empfindlichkeit gegenüber Sauerstoff kann man damit erklären, dass ein involviertes Enzym, die 4-Hydroxybutyryl-CoA-Dehydratase, sensitiv gegenüber Sauerstoff ist.[4]
Das durch den Kreislauf gebildete Acetyl-CoA kann zu Glycerinaldehyd-3-phosphat (GAP) aufgebaut werden und in den Baustoffwechsel einfließen. Hierbei werden weitere Cofaktoren, z. B. Ferredoxin (Fd), benötigt. Die Gesamtbilanz für die Bildung eines Moleküls GAP lautet somit:
Ob die beiden Moleküle Pyrophosphat hydrolysiert oder als Energiequelle verwendet werden, ist noch nicht bekannt.
Seit kurzem wird diskutiert, ob Pyruvat eher nicht aus Succinyl-CoA, einem Intermediat des Zyklus, gebildet wird.[2] Dabei wird Succinyl-CoA dem Kreislauf entzogen, zu Malat oder Oxalacetat umgesetzt und schließlich zu Pyruvat decarboxyliert. Um Succinyl-CoA aus Acetyl-CoA zu bilden, werden eineinhalb Runden des 3-Hydroxypropionat/4-Hydroxybutyratzyklus benötigt.
Der Aufbau einer phosphorylierten Triose, GAP, ähnelt energetisch gesehen dem Stoffwechselweg des Calvin-Zyklus, da auch hier neuen ATP-Äquivalente verbraucht werden (AMP zählt doppelt). Beim Calvin-Zyklus gehen jedoch durch die auftretende Photorespiration immer etwas mehr Energie und Reduktionsäquivalente verloren. Darüber hinaus haben die bei der Bicarbonatfixierung beteiligten Carboxylasen eine höhere Wechselzahl (28 ss−1 bei 65 °C) als RuBisCO beim Calvin-Zyklus (5 s−1).
Einzelnachweise
- Berg, IA. et al. (2010a): Study of the distribution of autotrophic CO2 fixation cycles in Crenarchaeota. In: Microbiology 156 (Pt 1); 256–269; PMID 19850614; doi:10.1099/mic.0.034298-0
- Berg, IA. et al. (2010b): Autotrophic carbon fixation in archaea. In: Nat Rev Microbiol. ; PMID 20453874; doi:10.1038/nrmicro2365
- Thauer, RK. (2007): Microbiology. A fifth pathway of carbon fixation. In: Science 318(5857); 1782–1783; PMID 18079388; doi:10.1126/science.1152209.
- Martins, BM. et al. (2004): Crystal structure of 4-hydroxybutyryl-CoA dehydratase: Radical catalysis involving a [4Fe–4S] cluster and flavin. In: PNAS 101(44); 15645–15649; PMID 15496473; PDF (freier Volltextzugriff, engl.)
Literatur
- Berg, IA. et al. (2007): A 3-hydroxypropionate/4-hydroxybutyrate autotrophic carbon dioxide assimilation pathway in Archaea. In: Science 318(5857); 1782–1786; PMID 18079405; doi:10.1126/science.1149976