Dicarboxylat/4-Hydroxybutyratzyklus
Der Dicarboxylat/4-Hydroxybutyratzyklus ist ein biochemischer Stoffkreislauf, der es manchen Archaeen erlaubt, Kohlenstoffdioxid (CO2), auch in Form von Bicarbonat (HCO3−), zu assimilieren. Der Zyklus kann in zwei Hälften unterteilt werden: Zunächst werden aus Acetyl-CoA, einem Molekül Kohlenstoffdioxid und Bicarbonat ein Molekül Succinyl-CoA gebildet. Im zweiten Teil entstehen daraus dann über 4-Hydroxybutyrat zwei Moleküle Acetyl-CoA, wobei das eine für den nächsten Durchlauf verwendet wird. Daher verdankt der Zyklus seinen Namen, da als erste Intermediate Dicarbonsäuren und im späteren Verlauf 4-Hydroxybutyrat gebildet werden.
Vorkommen
Der Stoffwechselweg wurde ursprünglich im hyperthermophilen Archaeon Ignicoccus hospitalis der Abteilung Crenarchaeota nachgewiesen. I. hospitalis ist der Wirt des obligaten Parasiten Nanoarchaeum equitans, auch ein Archaeon.[1] I. hospitalis lebt chemolithoautotroph unter anaeroben Bedingungen.
Auch in Thermoproteus neutrophilus, einem strikt anaeroben Archaeon, und Pyrolobus fumarii, einem fakultativ aeroben Archaeon, wurde der Dicarboxylat/4-Hydroxybutyratzyklus nachgewiesen.[2][3] Ersterer gehört zu der Ordnung Thermoproteales, letzterer zur Desulfurococcales, beide Vertreter der Crenarchaeota.
Biochemie
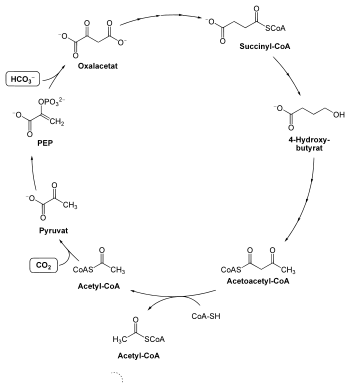
Ausgehend von Acetyl-CoA wird CO2 durch eine sauerstoffempfindliche Pyruvatsynthase zu Pyruvat assimiliert, wobei Reduktionsäquivalente benötigt werden. Wahrscheinlich stammen diese aus reduzierten Ferredoxinen. Pyruvat wird dann unter ATP-Verbrauch zu Phosphoenolpyruvat (PEP) umgesetzt, was eine Pyruvat:Wasser-Dikinase katalysiert. Ein Molekül Bicarbonat reagiert dann mit PEP zu Oxalacetat durch eine archeeische PEP-Carboxylase.
Oxalacetat wird analog im reduktiven Citratzyklus über L-Malat, Fumarat, Succinat zu Succinyl-CoA umgesetzt. Hierbei werden ATP und weitere Reduktionsäquivalente verbraucht. Durch diese isolierbaren Dicarbonsäuren verdankt der Zyklus die eine Hälfte seines Namens. Aus Succinyl-CoA entsteht durch eine Succinyl-CoA-Reduktase und einer Succinatsemialdehyd-Reduktase unter Verbrauch weiterer Reduktionsäquivalente schließlich 4-Hydroxybutyrat.
4-Hydroxybutyrat wird dann durch mehrere enzymatische Reaktionen zu 4-Hydroxybutyryl-CoA umgesetzt. Aus diesem entsteht durch das Schlüsselenzym des Zyklus, der 4-Hydroxybutyryl-CoA-Dehydratase, Crotonyl-CoA. Die Hydratase, ein 4Fe-4S und FAD-enthaltendes Enzym, katalysiert die Freisetzung des Wassers durch einen Ketylradikalmechanismus.[4] Weitere katalytische Reaktionen formen dieses schließlich über 3-Hydroxybutryryl-CoA in Acetoacetyl-CoA um. Eine Acetoacetyl-CoA β-Ketothiolase spaltet schließlich Acetoacetyl-CoA in zwei Moleküle Acetyl-CoA, wodurch der Zyklus geschlossen wird.
Die Bilanz für die Bildung von einem Molekül Acetyl-CoA lautet:
Acetyl-CoA wird dann in der Regel durch Fixierung eines weiteren Moleküls CO2 und Verbrauch von Reduktionsäquivalenten, z. B. Ferredoxin (Fd), sowie ATP zu Glycerinaldehyd-3-phosphat umgesetzt. Dieses kann dann im Kohlenhydratstoffwechsel weiter metabolisiert werden.
Infolgedessen beläuft sich die Gesamtbilanz für die Bildung eines Moleküls Glycerinaldehyd-3-phosphat (GAP):
Biologische Bedeutung
Dieser Stoffwechselweg ist der letzte entdeckte Weg zur CO2-Fixierung und ähnelt dem 3-Hydroxypropionat/4-Hydroxybutyratzyklus. Jedoch verläuft die Bildung zu Succinyl-CoA über Dicarbonsäuren, ab 4-Hydroxybutyrat entsprechen sich beide Zyklen dann wieder weitestgehend.
Der Aufbau einer phosphorylierten Triose, GAP, ist im Vergleich zum Calvin-Zyklus energetisch etwas günstiger: Es werden acht ATP-Äquivalente benötigt (AMP zählt doppelt). Bilanz Calvinzyklus:
Es sollte aber beachtet werden, dass beim Calvin-Zyklus durch die auftretende Photorespiration immer etwas Energie (und Reduktionsäquivalente) verloren gehen. Infolgedessen gilt der in der Gleichung angegebene ATP- und NAD(P)-Verbrauch unter optimalen und nicht unter den vorherrschenden Bedingungen in unserer sauerstoffreichen Atmosphäre.
Wegen der zahlreich involvierten sauerstoffempfindlichen Eisen-Schwefel-Proteine und Ferredoxine läuft dieser Zyklus nur unter strikt anaeroben oder mikroaeroben Bedingungen ab. Möglicherweise ist der Stoffwechselweg nur auf wenige Crenarchaeota beschränkt. Ob es sich hierbei um einen der ersten autotrophen Stoffwechselwege handelt, wird noch diskutiert.
Literatur
- Huber, H. et al. (2008): A dicarboxylate/4-hydroxybutyrate autotrophic carbon assimilation cycle in the hyperthermophilic Archaeum Ignicoccus hospitalis. In: Proc Natl Acad Sci USA 105(22); 7851–7856; PMID 18511565; PMC 2409403 (freier Volltext)
Einzelnachweise
- Podar, M. et al. (2008): A genomic analysis of the archaeal system Ignicoccus hospitalis-Nanoarchaeum equitans. In: Genome Biol 9(11); R158; PMID 19000309; PMC 2614490 (freier Volltext).
- Ramos-Vera, WH. et al. (2009): Autotrophic carbon dioxide assimilation in Thermoproteales revisited. In: J Bacteriol 191(13); 4286–4297; PMID 19411323; PMC 2698501 (freier Volltext).
- Berg, IA. et al. (2010b): Study of the distribution of autotrophic CO2 fixation cycles in Crenarchaeota. In: Microbiology 156 (Pt 1); 256–269; PMID 19850614; doi:10.1099/mic.0.034298-0.
- Berg, IA. et al. (2010a): Autotrophic carbon fixation in archaea. In: Nat Rev Microbiol. ; PMID 20453874; doi:10.1038/nrmicro2365.