3-Aminobenzoesäure
3-Aminobenzoesäure ist eine organische Carbonsäure, die zur Herstellung von Azofarbstoffen verwendet wird. Neben der 3-Aminobenzoesäure existieren zwei weitere stellungsisomere Formen: die Anthranilsäure (o-Aminobenzoesäure) und die 4-Aminobenzoesäure (p-Aminobenzoesäure).
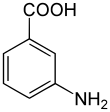
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | 3-Aminobenzoesäure | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C7H7NO2 | |||||||||||||||||||||
| Kurzbeschreibung |
beiger Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 137,14 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
1,51 g·cm−3[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
3,07; 4,79[2] | |||||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (5,9 g·l−1 bei 20 °C)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Gewinnung und Darstellung
3-Aminobenzoesäure kann durch die Reduktion von 3-Nitrobenzoesäure erhalten werden. Als Reduktionsmittel eignen sich beispielsweise elementares Zink in Salzsäure[4] oder Hydrazin[5].
Toxikologie
3-Aminobenzoesäure zeigt geringe Toxizität. Außerdem wurden keine Hinweise auf Reproduktionstoxizität, Mutagenität und Kanzerogenität gefunden.[1]
Weblinks
Einzelnachweise
- Eintrag zu 3-Aminobenzoesäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- CRC Handbook of Chemistry and Physics, 85th Edition, CRC Press, Boca Raton, 2004.
- Datenblatt 3-Aminobenzoesäure bei Sigma-Aldrich, abgerufen am 8. November 2008 (PDF).
- J. Wilbrand, F. K. Beilstein: Ueber eine neue Reihe isomerer Verbindungen der Benzoëgruppe. – Nitrodracylsäure und deren Derivate, in: J. Liebigs Ann. Chem., 1863, 128, S. 257–273; doi:10.1002/jlac.18631280302, (PDF).
- T. Curtius: Die Einwirkung von Hydrazinhydrat auf Nitroverbindungen. In: J. für prakt. Chemie 184, 233–237 (1907), Digitalisat auf Gallica.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.
