2,3,6,7-Tetrachlornaphthalin
2,3,6,7-Tetrachlornaphthalin ist ein chloriertes Derivat von Naphthalin. Die Struktur ähnelt zwar der als Sevesodioxin bekannt gewordenen Verbindung 2,3,7,8-Tetrachlordibenzodioxin, gehört jedoch zu den polychlorierten Naphthalinen (kurz PCN) und nicht zu den Dioxinen.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
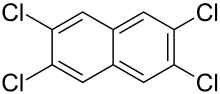 | ||||||||||
| Allgemeines | ||||||||||
| Name | 2,3,6,7-Tetrachlornaphthalin | |||||||||
| Andere Namen |
PCN 48 | |||||||||
| Summenformel | C10H4Cl4 | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 265,95 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
1,676 g·cm−3[1] | |||||||||
| Schmelzpunkt |
203–204 °C[2] | |||||||||
| Sublimationspunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| MAK |
Schweiz: 2 mg·m−3 (gemessen als einatembarer Staub)[4] | |||||||||
| Toxikologische Daten |
>3 mg·kg−1 (LD50, Meerschweinchen, oral)[5] | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Das 2,3,6,7-Tetrachlornaphthalin kann in einer 11-stufigen Synthese aus 3,4-Dichlorphthalsäureanhydrid hergestellt werden.[2] 1962 wurde es von Reimlinger und King erstmals synthetisiert.[1]
Eigenschaften
Physikalische Eigenschaften
2,3,6,7-Tetrachlornaphthalin bildet weiße Nadeln und sublimiert bei 135 °C.[1] Die Verbindung kristallisiert in einem monoklinen Gitter.[1] Im Infrarotspektrum der Substanz treten Absorptionsbanden bei den Wellenzahlen 1638, 1478, 1458, 1346, 1177, 965, 902, 761 und 650 auf.[6] Im Kernmagnetischen-Resonanz-Spektrum zeigen sich bei einer Lösung in Hexadeuterobenzol Wasserstoffatome bei 7,10 ppm (400 MHz, s, 4 H), Kohlenstoffatome bei 128,4 (quart.), 127,6 (quart.) und 128,0 (tert.) ppm (100 MHz).[2]
Chemische Eigenschaften
In einer 15-stündigen Elektrolyse bei −2,2 Volt an der Arbeitselektrode konnte 2,3,6,7-Tetrachlornaphthalin bis zu 98 % zu niederchlorierten oder halogenfreien Naphthalinderivaten abgebaut werden.[7]
Einzelnachweise
- Reimlinger, H.; King, G.: Über die Darstellung einiger Polychlor-naphthaline in Chem. Ber. 95 (1962), 1043–1048, doi:10.1002/cber.19620950436.
- Levy, L.A.: The Synthesis Of 2,3,6,7-Tetrasubstituted Naphthalenes: 2,3,6,7-Tetrachloronaphthalene in Synth. Common. 13 (1983), 639–648, doi:10.1080/00397918308060343.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 34588-40-4 bzw. 2,3,6,7-Tetrachlornaphthalin), abgerufen am 2. November 2015.
- Concise International Chemical Assessment Document (CICAD) für Chlorinated Naphthalenes, abgerufen am 9. Dezember 2014.
- Giachino, G.G.: Phosphorescence spectra and lifetimes of symmetrical tetrachloronaphthalenes in J. Phys. Chem. 84 (1980), 3522–3524, doi:10.1021/j100463a006.
- J. Voss, M. Altrogge, D. Golinske, O. Kranz, D. Nünnecke, D. Petersen, E. Waller: Degradation of Chlorinated Arenes by Electroreduction in Treatment of Contaminated Soil – Fundamentals, Analysis, Applications (Eds.: R. Stegmann, G. Brunner, W. Calmano, G. Matz), Springer Verlag, Berlin, Heidelberg, New York, 2001, S. 547–563, doi:10.1007/978-3-662-04643-2 (eingeschränkte Vorschau in der Google-Buchsuche, insbesondere S. 550–551).