Zeotropes Gemisch
Ein Gemisch von chemischen Stoffen wird als zeotrop bezeichnet, wenn die Zusammensetzung von Flüssigkeit und Dampf im Dampf-Flüssigkeit-Gleichgewicht immer unterschiedlich ist. Damit berühren sich Taukurve und Siedekurve in keinem Punkt. Gemische, deren Tau- und Siedekurven sich in mindestens einem Punkt berühren und somit die Zusammensetzung in Dampf und Flüssigkeit gleich ist, heißen azeotrope Gemische.
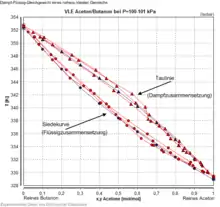
Dampfdruck und Siedetemperatur eines zeotropen Gemischs zeichnen sich dadurch aus, dass sie stets zwischen den Dampfdrücken und Siedetemperaturen der Reinstoffe liegen, während bei azeotropen Gemischen ein Druckmaximum/Temperaturminimum oder Druckminimum/Temperaturmaximum auftritt, das außerhalb des durch die Reinstoffwerte begrenzten Bereichs liegt.
Bedeutung
Zeotrope Gemische lassen sich durch Destillation bzw. Rektifikation, also wiederholte Verdampfung und Kondensation, in Trennkolonnen trennen. Ihre Trennfaktoren werden niemals 1, können jedoch so gering sein, dass eine Trennung durch Rektifikation technisch unmöglich wird.
Technisch von größerer Bedeutung sind Zeotropie und Azeotropie auch bei Kältemittelgemischen, bei denen schon bei der Namensgebung mit Kurzzeichen zwischen zeotropen (R4xx) und azeotropen Gemischen (R5xx) unterschieden wird. Zeotrope Gemische haben den Nachteil, dass ihre Zusammensetzung sich beim Verdampfen und Kondensieren ändert. Damit ändern sich auch Siedepunkte sowie andere Eigenschaften, insbesondere auch die in der Kühltechnik wichtigen kalorischen Größen wie Verdampfungsenthalpie und Wärmekapazität. Azeotrope Gemische hingegen verhalten sich bei der azeotropen Zusammensetzung wie reine Stoffe mit konstanten Eigenschaften. Bei zeotropen Gemischen muss daher darauf geachtet werden, dass die Differenzen gering bleiben und somit werden zeotrope Gemische mit kleinen Trennfaktoren bevorzugt.
Vorkommen
Zeotropie tritt auf, wenn die beteiligten Komponenten eines Gemischs chemisch ähnlich sind oder deren Siedepunktsdifferenz sehr groß ist. Chemisch ähnlich sind beispielsweise Gemische, die nur aus Alkanen oder monofunktionalen Ketonen bestehen. Hingegen tritt Azeotropie auf bei kleineren Siedepunktsdifferenzen und bei Stoffen mit verschiedenen funktionellen Gruppen, etwa beim Gemisch aus Methanol und Chloroform.

Ein Gemisch kann sowohl zeotrop als auch azeotrop sein, da die azeotrope Zusammensetzung temperatur- und druckabhängig ist, mal stärker und mal schwächer. Beispielsweise verhält sich das Gemisch aus Ethanol und Wasser unter etwa T = 305 K und p = 12 kPa zeotrop, während bei höheren Temperaturen und Drücken Azeotropie auftritt. Bei Normaldruck ist die Zusammensetzung etwa 90 Mol-% Ethanol und 10 Mol-% Wasser. Bei der Grenze sind jedoch die Unterschiede zwischen den Zusammensetzungen der Dampf- und der Flüssigphase ebenso wie die relative Flüchtigkeit noch sehr klein, so dass eine technische Nutzung des Effekts nahe dem azeotrop/zeotrop-Übergang kaum möglich ist, sondern erst bei deutlich geringeren Temperaturen und Drücken.
Beschreibung
Zeotropie ist die qualitative Aussage über ein Gemisch bei gegebenem Druck und gegebener Temperatur, dass die Flüssigkeit und der Dampf stets unterschiedliche Zusammensetzungen haben. Eine Angabe zu einer speziellen Zusammensetzung ist daher nicht sinnvoll.