Weinreb-Amid-Ketonsynthese
Die Weinreb-Amid Ketonsynthese ist eine chemische Reaktion, welche dazu dient, Carbonsäuren zu Ketonen oder Aldehyden umzusetzen.[1] Weinreb-Amide sind N,O-Dimethylhydroxylamide einer Carbonsäure. Die Namensreaktion wurde nach Steven M. Weinreb benannt.
Darstellung von Weinreb-Amiden
Weinreb-Amide werden normalerweise durch Amidierung von Carbonsäuren beispielsweise über ihre Carbonsäurehalogenide hergestellt.
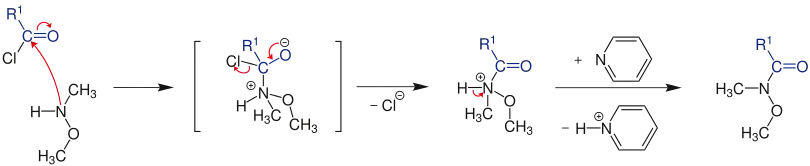
Auch die Aminolyse von Carbonsäureestern mit metalliertem N,O-Dimethylhydroxylamin ist eine Möglichkeit Weinreb-Amide herzustellen.
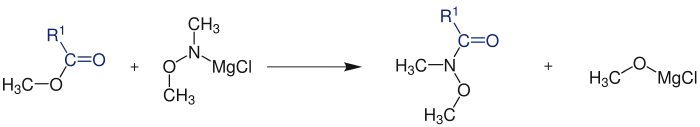
Mechanismus
Die Umsetzung von Carbonsäure-Derivaten wie Estern und Säurechloriden mit metallorganischen Nucleophilen wie z. B. Grignard-Verbindungen führt in der Regel nicht zu den Ketonen, weil hier die Abgangsgruppe gut ist und das Keton schon während der Reaktion entsteht und dieses dann mit einem weiteren Nucleophil zu den entsprechenden Alkoholen weiter reagieren kann. Bei Weinreb-Amiden ist die Abgangsgruppe verhältnismäßig schlecht und das Keton wird erst bei Aufarbeitung mit verdünnter, wässriger Säure freigesetzt. Während der Reaktion bleibt das Weinreb-Amid auf der Stufe des stabilen tetraedrischen Chelates stehen, welches die Addition von mehr als einem Äquivalent der metallorganischen Verbindung verhindert. Bei dem Chelat-Komplex handelt es sich um ein Halbaminal.
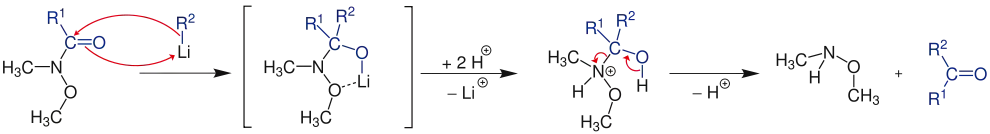
Bedeutung
Aus Weinreb-Amiden kann man über zwei Stufen und normalerweise in guten Ausbeuten aus Carbonsäuren Ketone, unter Knüpfung einer Kohlenstoff-Kohlenstoff-Bindung, herstellen. Mit den Reduktionsmitteln Diisobutylaluminiumhydrid (DIBAL-H) oder Lithiumaluminiumhydrid (LiAlH4)[2] werden Weinreb-Amide zu Halbaminalen reduziert, die nach der Hydrolyse Aldehyde liefern.[3]
Einzelnachweise
- S. Nahm, S. M. Weinreb: in Tetrahedron Letters 'N-methoxy-n-methylamides as effective acylating agents' 1981, 22, 3815–3818.
- Eintrag zu Weinreb-Amid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 5. August 2019.
- O. P. Goel, U. Krolls, M. Stier, S. Kesten: in Organic Synthesis Collectiv Volumen 8, 69 1989.
Literatur
- Kürti, László und Czakó, Barbara: Strategic Applications of Named Reactions in Organic Synthesis; Elsevier Academic Press, Burlington-San Diego-London 2005, 1. Auflage; ISBN 0-12-369483-3.