T7-RNA-Polymerase
Die T7-RNA-Polymerase ist die RNA-Polymerase aus dem Phagen T7, einem Virus, das Darmbakterien der Spezies Escherichia coli befällt. Das Enzym spielt eine bedeutende Rolle in der Biotechnologie bei der Expression von rekombinanten Proteinen, vor allem in E. coli aber auch in Bacillus subtilis und in Pseudomonaden existieren Anwendungen.
| RNA-Polymerase (Phage T7) | ||
|---|---|---|
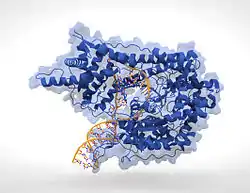 | ||
| nach PDB 1MSW | ||
|
Vorhandene Strukturdaten: s. UniProt | ||
| Masse/Länge Primärstruktur | 883 Aminosäuren | |
| Bezeichner | ||
| Gen-Name(n) | 1 (Entrez) | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 2.7.7.6, Nukleotidyltransferase | |
| Substrat | Nucleosidtriphosphat + RNAn | |
| Produkte | Diphosphat + RNAn+1 | |
| Vorkommen | ||
| Übergeordnetes Taxon | Caudovirales[1] | |
Funktion
Die ersten RNA-Transkripte des Bakterienvirus (Phagen) T7 werden mit der RNA-Polymerase des Wirts durchgeführt. Darunter auch die Information für die Translation der sehr promotorspezifischen T7-RNA-Polymerase. Die T7 eigene Polymerase erkennt nur ihren eigenen Promotor und ist deshalb eine sehr gute Methode den Stoffwechsel des Wirts zu assimilieren und für die eigene Reproduktion zu nutzen. Die T7-RNA-Polymerase gilt in Kombination mit dem T7 eigenen Promotor als besonders „starkes“ Expressionsystem. Das bedeutet, dass mit diesem Promotor sehr viel RNA und als Folge davon häufig viel Protein pro Kopie auf einer DNA produziert werden kann. T7-Polymerase hat während der Elongationsphase der Transkription eine Nukleotidadditionsgeschwindigkeit von 200 bis 260 Nukleotiden pro Sekunde (die normale E.-coli-RNA-Polymerase erreicht etwa 40 Nukleotiden pro Sekunde).
Der T7-Promotor
Der T7-Promotor hat eine spezifische Sequenz:
TAATACGACTCACTATAGGGAGA
wobei die Transkription mit GGGAGA startet. Der Promotor verfügt über fast keine Basaltranskription. Das heißt, bei Abwesenheit von T7-RNA-Polymerase wird er so gut wie nicht abgelesen.
Anwendung in der Biotechnologie
Die Stärke des T7-Expressionsystems machen den T7-Promotor und die T7-Polymerase sehr interessant für die Expression rekombinanter Proteine. Daher existieren inzwischen diverse Vektoren zur Proteinexpression die das T7-System verwenden, wie etwa die pET-Serie.
In der Regel befindet sich auf einem Vektor die T7-Promotorsequenz und dahinter (vor einer notwendigen RBS) die codierende Region für ein „protein of interest“. Da ein solches Expressionssystem wegen der oben genannten Gründe nicht funktionsfähig wäre (da vom Expressionsorganismus keine T7-Polymerase produziert wird), muss die T7-Polymerase künstlich in das System eingebracht werden. Die häufigste Methode hierzu ist die genomische Verankerung einer T7-Expressionskassette im Produktionsorganismus. Der am häufigsten hierfür benutzte Organismus ist E. coli. Bei ihm bezeichnet man den entsprechenden Genotyp, der eine genomische T7-Polymerase anzeigt, mit (DE3), da die T7-Polymerase mit Hilfe des "DE3-Prophagen" ins Genom integriert wurde. Hierbei steht die Expression der T7-Polymerase unter Kontrolle des lacUV5-Promotors, der mittels IPTG oder Lactose induziert werden kann.
Probleme bei der Verwendung von T7-Expressionssystemen
Es gibt mehrere Probleme die sich aus der Verwendung des T7-Expressionssystems ergeben:
Die verwendete, genomisch verankerte Expressionskassette für die T7-RNA-Polymerase ist nicht „dicht“, man spricht hier von einer sogenannten Basaltranskription. Die Folge ist, dass so stets eine gewisse Menge an T7-Polymerase vorhanden ist, die dafür sorgt, dass der Produktionsorganismus auch vor der eigentlichen Induktion schon Protein exprimiert. Das ist vor allem bei toxischen Produkten sehr nachteilig und außerdem bedeutet es eine unnötige metabolische Belastung des Produktionsorganismus. Auch die Addition eines lac Operators auf dem Vektor zwischen Promotor und proteincodierender Sequenz zeigt hier wenig Erfolg.
Eine weitere Methode ist die genomische Verankerung einer T7-Lysozym-Expressionskassette (Genotyp Bezeichnung in E. coli pLys) oder die Addition eines entsprechenden Plasmids. T7-Lysozym bindet an die T7-Polymerase und hemmt diese.[2] Allerdings bedeutet diese Methode ebenfalls eine zusätzliche Belastung für den Produktionsorganismus und sorgt nicht für optimale Ergebnisse im Bezug auf die Basaltranskription.
Die neusten Entwicklungen sind T7-Stämme, die nicht mehr über den DE3-Genotyp verfügen, das heißt die T7-Polymerase unter Kontrolle des lacUV5-Promotors tragen, sondern unter wesentlich dichteren Promotorsystemen wie etwa dem Rhamnose- oder Arabinoseoperon. Bei diesen Stämmen wird die T7-Polymerase erst nach Zugabe des entsprechenden Zuckers produziert. Das führt zu einer wesentlich geringeren Basaltranskription. Da diese Zucker im Vergleich zu IPTG relativ teuer sind, gelten solche Systeme allerdings nicht als wirtschaftlich bei der Produktion von kostengünstigen rekombinanten Produkten.
Ein zweites Problem bei der Verwendung des T7-Systems ist die starke Überexpression des „protein of interest“. Die Folge hiervon ist ein hoher Produktverlust durch Inclusion Bodies.
In vitro-Anwendung
Eine weitere wichtige Anwendung ist die in vitro-Transkription mit gereingter T7-RNA-Polymerase, ATP, CTP, GTP, UTP und einem DNA-Template, die es erlaubt spezifische RNAs im Labormaßstab zu produzieren. Die Methode, bei der auch SP6- und T3-RNA-Polymerasen eingesetzt werden, wurde von Douglas A. Melton entwickelt.[3] Als Template werden PCR-Produkte mit dem geeigneten Promoter oder linearisierte rekombinante Vektoren wie pGEM-T Easy verwendet. Die RNAs werden u. a. für die in vitro-Translation, die Injektion in Oocyten und die in situ-Hybridisierung verwendet.
Literatur
- Martin CT, Esposito EA, Theis K, Gong P: Structure and function in promoter escape by T7 RNA polymerase. In: Prog. Nucleic Acid Res. Mol. Biol.. 80, 2005, S. 323–47. doi:10.1016/S0079-6603(05)80008-X. PMID 16164978.
- Sousa R, Mukherjee S: T7 RNA polymerase. In: Prog. Nucleic Acid Res. Mol. Biol.. 73, 2003, S. 1–41. doi:10.1016/S0079-6603(03)01001-8. PMID 12882513.
- McAllister WT: Structure and function of the bacteriophage T7 RNA polymerase (or, the virtues of simplicity). In: Cell. Mol. Biol. Res.. 39, Nr. 4, 1993, S. 385–91. PMID 8312975.
- Sastry SS, Ross BM: Nuclease activity of T7 RNA polymerase and the heterogeneity of transcription elongation complexes. In: J. Biol. Chem. 272, Nr. 13, März 1997, S. 8644–52. doi:10.1074/jbc.272.13.8644. PMID 9079696.
- Garabed Antranikian: Angewandte Mikrobiologie. Springer, Berlin / Heidelberg 2006, ISBN 3-540-24083-7.
Einzelnachweise
- Homologe bei NCBI
- F. W. Studier: Use of bacteriophage T7 lysozyme to improve an inducible T7 expression system. In: Journal of molecular biology. Band 219, Nummer 1, Mai 1991, S. 37–44, PMID 2023259.
- P. A. Krieg, D. A. Melton: Functional messenger RNAs are produced by SP6 in vitro transcription of cloned cDNAs. In: Nucleic acids research. Band 12, Nummer 18, September 1984, S. 7057–7070, PMID 6207484, PMC 320142 (freier Volltext).