Stammbaumanalyse
Die Analyse von Stammbäumen ist ebenso wie die Zwillingsforschung und Analysen nach der populationsstatistischen Methode eine der ältesten Methoden der Erbforschung beim Menschen. Seit der Entdeckung der Chromosomen kam die Analyse von Karyogrammen hinzu. Voraussetzung zum Verständnis ist die Kenntnis der Mendelschen Regeln. Die Methode der Stammbaumanalyse wurde besonders anhand der Vererbung sichtbarer Erbkrankheiten entwickelt. Die beobachtbaren unterschiedlichen Erbgänge finden sich jedoch bei allen durch Chromosomen vererbten Erbeigenschaften, also auch bei den meisten, die den gesunden Gesamtorganismus ausmachen.[1]

Vorgehen bei der Stammbaumanalyse für genetische Merkmale, die auf der DNA in den Zellkernen codiert sind:
- Wird das betrachtete Merkmal dominant (in jeder Generation ausgeprägt) oder rezessiv vererbt?
- Wird das betrachtete Merkmal autosomal oder gonosomal (ein Geschlecht besonders betroffen) vererbt?
- Genaue Angabe jedes sicheren und möglichen Genotyps sowie Begründung dazu (zum Beispiel durch Kreuzungsschemata).
Wichtig ist auch, zu begründen, warum die jeweilige Alternative ausgeschlossen wurde.
Kennzeichen eines autosomal-dominanten Erbgangs
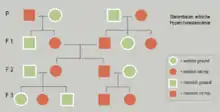
Beim autosomal-dominanten Erbgang ist auch ein heterozygotes Individuum am Phänotyp erkennbar. Hier reicht ein heterozygoter Merkmalsträger aus, um mit einem Partner, der das Merkmal nicht besitzt, also sicher homozygot gesund ist, durchschnittlich 50 % von dem Merkmal betroffene Nachkommen zu zeugen, die dann auch wieder heterozygot sind und das Merkmal phänotypisch aufweisen. Es kann auch vorkommen, dass keine betroffenen Nachkommen dabei sind, weil die Allele bei der Oogenese und Spermatogenese mehr oder weniger zufällig in die Gameten gelangen (Meiotic Drive), aber dann kommt das Merkmal auch in den folgenden Generationen mit gesunden Partnern nicht wieder zum Vorschein, weil in diesem Falle nur das gesunde rezessive Allel weitervererbt wurde. Bei denjenigen Individuen, die innerhalb eines dominant-rezessiven Erbgangs das dominante Merkmal nicht zeigen, kann man davon ausgehen, dass sie homozygot sind und es auch nicht vererben. Der Anteil der betroffenen Nachkommen kann auch höher sein als 50 %, je nachdem, wie die beiden Allele bei der Gametenbildung verteilt werden.
Das Erbschema für die Verbindung zweier heterozygoter Träger eines dominanten Merkmals entspricht der Mendelschen Spaltungsregel. Wenn zwei heterozygote Partner zusammen Nachkommen zeugen, werden durchschnittlich 75 % davon Merkmalsträger, wobei ein Drittel davon homozygot und zwei Drittel heterozygot sind. Diese beiden kann man am Phänotyp nicht unterscheiden. Man sieht ein gehäuftes Auftreten des Merkmals, und nur die restlichen durchschnittlich 25 % zeigen das Merkmal nicht, weil sie jeweils das rezessive Allel von beiden Eltern erhalten haben, also homozygot sind. Die Verteilung eines Merkmals auf die zwei Geschlechter ist bei autosomalen Erbgängen ungefähr gleich, sofern eine ausreichende Gesamtzahl von Individuen im Stammbaum eingetragen ist, so dass auf dieser Basis ein statistisches Mittel gebildet werden kann.
Kennzeichen eines autosomal-rezessiven Erbgangs
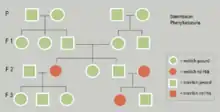
Bekommen zwei phänotypisch gesunde Eltern von einer autosomal vererbten Erbkrankheit betroffene Kinder, so kann daraus der Rückschluss gezogen werden, dass das krankheitsauslösende Gen rezessiv vererbt wird. Beide Eltern sind in diesem Fall Konduktoren, also Überträger der Erbkrankheit, ohne selbst betroffen zu sein. Ihr Genotyp ist heterozygot. Die Vererbung erfolgt nach der Spaltungsregel.
Nur diejenigen Kinder, die das rezessive Allel von beiden Eltern erhalten haben, also homozygot sind, erkranken. Diejenigen Kinder, die das rezessive Allel nur von einem Elternteil erhalten haben, sind selbst gesund, sind aber Konduktoren, können also die Erbanlage weitervererben. Die Kinder, die von jedem Elternteil jeweils nur das gesunde Allel erhalten haben, sind reinerbig gesund und können die Krankheit daher nicht vererben.
Bei einer Stammbaumanalyse kann dann auf einen autosomal-rezessiven Erbgang geschlossen werden, wenn der Anteil der Geschlechter bei den Betroffenen gleich ist (also eine geschlechtsunabhängige Vererbung) und wenn es außerdem vorkommt, dass an einzelnen Stellen in einzelnen Abstammungslinien eine oder mehrere Generationen "übersprungen" werden und erst in der darauf folgenden Generation wieder Merkmalsträger erscheinen. Manchmal können auch in folgenden Generationen gar keine Erkrankten mehr auftreten, wenn nur noch Verbindungen mit homozygot gesunden Partnern eingegangen wurden. Die Abfolge des Auftretens der Phänotypen erlaubt Rückschlüsse auf die Genotypen einzelner Individuen, die allerdings nicht immer eindeutig sind.
Kennzeichen von gonosomalen Erbgängen
In den meisten Fällen eines gonosomalen Erbgangs liegen die betroffenen Allele auf dem X-Chromosom (X-chromosomaler Erbgang). Es sind allerdings auch einige (wenige) Ausnahmen zu finden, bei denen sich das betreffende Allel auf dem Y-Chromosom befindet (Y-chromosomaler Erbgang). Allerdings ist diese Form des gonosomalen Erbganges nur sehr selten anzutreffen, weil das Y-Chromosom zu großen Teilen genleer und somit für die Vererbung von Merkmalen unerheblich ist. Typische Beispiele für X-chromosomale Erbgänge sind die Vererbung einer Bluterkrankheit sowie der Rot-Grün-Sehschwäche, bei denen sich das betroffene Allel auf dem X-Chromosom befindet, wobei die Frauen, die so einen Gendefekt auf einem ihrer beiden Allele haben, Konduktorinnen sind, also das Merkmal im Phänotyp nicht zeigen.
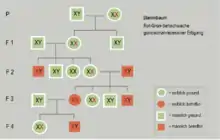
- Bei einem gonosomal-rezessiven Erbgang sind deutlich mehr Männer als Frauen von der Erbkrankheit betroffen, da Männer nur ein X-Chromosom besitzen, dem das Y-Chromosom nichts entgegensetzen kann, weil es kein wirklich homologes Chromosom ist. Deshalb wirkt sich, wenn ein männliches Kind gezeugt wird, bereits ein Allel auf seinem X-Chromosom im Phänotyp aus (Erbschema siehe Konduktorin). Bei Mädchen müsste das rezessive Allel auf beiden Chromosomen vorhanden sein, um sich im Phänotyp auszuwirken. Nur wenn ein Mann, der selbst betroffen ist, mit einer Konduktorin eine Tochter zeugt, ist diese mit einer Wahrscheinlichkeit von 50 % auch betroffen, je nachdem, ob sie von der Mutter das dominante gesunde oder das rezessive krankheitsauslösende Allel erhält. Bei den Störungen der Blutgerinnung gibt es auch seltene autosomal vererbte Gendefekte, die ebenfalls zur Hämophilie führen. Bei ihnen ist der Anteil der Geschlechter bei den Betroffenen gleich. Die Bluterkrankheit hat bei Mädchen ab dem Einsetzen der Menstruation lebensbedrohliche Auswirkungen.
- Bei einem gonosomal-dominanten Erbgang, bei dem das krankheitsauslösende Allel auf dem X-Chromosom liegt, ist die Tochter eines betroffenen Mannes auch betroffen, weil die Weitergabe seines X-Chromosoms bei der Spermatogenese bewirkt, dass es ein Mädchen wird. Väter übertragen das Allel nur auf ihre Töchter, da männliche Nachkommen vom Vater lediglich die Informationen auf dem Y-Chromosom des Vaters erben. Eine Vererbung des entsprechenden Merkmals vom Vater auf den Sohn ist daher biologisch nicht möglich. Das bedeutet, wenn dennoch ein Sohn betroffen ist, muss das krankheitsauslösende Allel auf dem von der Mutter stammenden X-Chromosom liegen.
Maternaler Erbgang
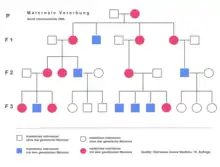
Durch die mitochondriale DNA vererbte genetische Merkmale folgen in der Regel einem maternalen Erbgang, werden also nur von der Mutter vererbt, denn die Zygote enthält nur die Mitochondrien der Eizelle. Das Mitochondrium des Spermiums gelangt meist nicht in die Zygote. Von Mutationen der mtDNA betroffene Frauen vererben das Merkmal an ihre Kinder beiderlei Geschlechts. Betroffene Männer vererben es an keines ihrer Kinder.[2]
Effizienz der Methode
Anhand dieser Kriterien lassen sich Familienstammbäume bei Menschen und auch Ahnentafeln bei Zuchttieren, die über mehrere Generationen gehen und deren Eintragungen korrekt und vollständig sind, relativ genau analysieren.[3] Aus der Art, wie ein Merkmal in der Generationenfolge auftritt, kann man auf den Genotyp einzelner Individuen rückschließen. Diese Methode eignet sich nur für Erbgänge bei monogen bedingten Merkmalen. Hierbei ist auch zu berücksichtigen, dass bei seltenen Erbanlagen Konduktoren auch unentdeckt bleiben können, solange sie nicht zufällig mit anderen Konduktoren gemeinsame Nachkommen hervorbringen. Deshalb waren bei der Entwicklung der Methode der Stammbaumanalyse gerade solche Stammbäume interessant, in denen Erbkrankheiten sichtbar auftraten. Die moderne Molekulargenetik und Humangenetik verfügen inzwischen über noch effizientere Methoden, wobei aber weiterhin auch Stammbaumanalysen im Vorfeld anderer Untersuchungen vorgenommen werden, da sich daraus wichtige Anhaltspunkte ergeben, welche Genloci gegebenenfalls zu untersuchen wären.[4][5]
Siehe auch
Weblinks
Einzelnachweise
- Biologie-Schule: Stammbaumanalyse
- Karl Skorecki, Doron Behar: Mitochondriale DNS und hereditäre Merkmale und Erkrankungen
- Dr. Carmen L. Battaglia: Pedigree Analysis
- Neil A. Campbell, Jane B. Reece: Biologie. Spektrum-Verlag 2003, ISBN 3-8274-1352-4, Seite 308–311.
- Ulrich Weber: Biologie Gesamtband Oberstufe, Cornelsen-Verlag 2001, ISBN 3-464-04279-0, Seite 178–182.