Neuguinea-Amethystpython
Der Neuguinea-Amethystpython (Simalia amethistina, Syn.: Morelia amethistina), auch kurz Amethystpython, zählt zur Familie der Pythons (Pythonidae) und wird dort in die Gattung der Amethystpythons (Simalia) gestellt. Die in Indonesien, Papua-Neuguinea und dem australischen Bundesstaat Queensland (Daintree National Park) beheimatete Schlange zeigt lokal unterschiedliche Farbmorphen. Bei der Auftrennung der Amethystpythons im Jahr 2000 wurde die Art neu definiert. Erste molekulargenetische Analysen erhärten den Verdacht, dass der Neuguinea-Amethystpython aus mindestens zwei eigenständigen Arten besteht. Über die Biologie dieses Pythons ist fast nichts bekannt.
| Neuguinea-Amethystpython | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
.jpg.webp)
Neuguinea-Amethystpython (Simalia amethistina), Sorong | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Simalia amethistina | ||||||||||||
| (Schneider, 1801) |
Beschreibung
Körperbau, Länge und Erbgut
Der Neuguinea-Amethystpython ist ein schlanker, aber dennoch ziemlich kräftig gebauter Python. Sein langer Schwanz kann über 17 % der Gesamtlänge ausmachen. Der Kopf ist deutlich vom Hals abgesetzt und bei adulten Weibchen deutlich verbreitert. Die Augen liegen an den Kopfseiten und sind leicht nach vorne gerichtet. Die rundliche, von oben betrachtet, halbovale Schnauze ist bei Männchen länger ausgeprägt als bei Weibchen. Ihr sitzen die runden Nasenlöcher schräg zwischen Kopfoberseite und Kopfseite auf. Diese große Art konnte bisher nur anhand weniger Individuen untersucht werden, wodurch noch keine Daten zur Durchschnitts- und Maximallänge adulter Tiere vorliegen. Ein in Gefangenschaft geborenes Individuum der Sorong-Population besaß nach sechs Jahren bereits eine Gesamtlänge von 4,72 Meter.[1] Das Erbgut der Art besteht aus 36 diploiden Chromosomen (2n = 36).[2]
Beschuppung

Das von oben nur mäßig sichtbare Rostrale (Schnauzenschild) hat, wie bei den meisten anderen Pythons auch, zwei tiefe Labialgruben. Die Nasenlöcher sind jeweils im oberen hinteren Teil des großen Nasale (Nasenschild) positioniert. Vom Nasenloch bis zum Hinterrand des Schildes zieht eine gut erkennbare Naht. Zur Kopfmitte hin sind die Nasalia von einem Paar Internasalia (Zwischennasenschilden) separiert. Von der Schnauzenspitze her entlang der Mittellinie der Kopfoberseite folgen den Internasalia ein großes langes vorderes Paar Präfrontalia (Vorstirnschilde). Das hintere Paar Präfrontalia liegt seitlich den vorderen Präfrontalia an und wird durch diese entweder komplett getrennt oder vereinigt sich an seinem Hinterteil. Bei der ersten Variante grenzen die vorderen Präfrontalia direkt an das dahinter liegende große, einfache Frontale (Stirnschild), oder werden durch ein kleineres Schild von diesem getrennt. Hinter dem Frontale schließen drei große Paare Parietalia (Scheitelschilde) an, die untereinander teilweise bis komplett fusioniert sein können.[3] Auf der Mittellinie zwischen diesen Schildpaaren können zudem bis zu zwei kleine Interparietalia (Zwischenscheitelschilde) liegen. Über den Augen befindet sich je ein großes dreieckiges Supraoculare (Überaugenschild). Präocularia (Voraugenschilde) existieren zwei bis drei, Postocularia (Hinteraugenschilde) drei bis fünf. Subocularia (Unteraugenschilde) fehlen bei dieser Art. Auf der Seite des Kopfes zwischen Auge und Nasenloch liegen in ein bis drei Reihen angeordnete Lorealia (Zügelschilde).[1] Von gewöhnlich 12 Supralabialia (Oberlippenschilden) tragen die vordersten vier an ihrem hinteren Rand tiefe Labialgrube, wobei die Labialgrubengröße gegen den Maulwinkel hin abnimmt. Supralabialia Nummer 6 und 7 berühren zudem den Augenunterrand.[3] Infralabialia (Unterlippenschilde) gibt es 18 bis 23[1], wovon die vordersten zwei schwach erkennbare und ab hinter dem Auge sechs bis acht, teilweise auch mehr, tiefe Labialgruben tragen. Die Kinngrube besteht aus schilderloser Haut, selten auch wenigen kleinen Schilden.[3]
Die Anzahl der Ventralia (Bauchschilde) variiert zwischen 320 und 346, die Anzahl der dorsalen Schuppenreihen in der Körpermitte zwischen 41 und 57. Von der Kloake bis zur Schwanzspitze finden sich 99 bis 106 meist paarige Subcaudalia (Schwanzunterseitenschilde). Das Anale (Analschild) ist ungeteilt.[3]
Färbung
Neuguinea-Amethystpythons zeigen sehr frappante ortsspezifische Färbungs- und Musterungsunterschiede, die auch von genetischen Differenzen begleitet sind. Geographisch konnten bisher zwei deutlich unterschiedliche Farbformen abgegrenzt werden:
- Populationen auf Nordost-Neuguinea (Nord-Irian Jaya und Soronghalbinsel) sind mittel- bis blassbraun und zeigt ein dunkles Muster, das auf dem hinteren Körperdrittel zunehmend verblasst.[1] Es besteht entlang der Wirbelsäule aus Querbändern, die auch X-förmigen Figuren bilden können sowie je zwei Längsbändern auf den Flanken.[3] Bei gewissen Tieren ist diese Körpermusterung nur geringfügig ausgeprägt oder fehlt ganz. Bei all diesen Tieren verläuft aber über den Hinterkopf und den Nacken je ein schwarzes, gut ausgeprägtes Band. Hiervon ist ersteres beidseits mit den Maulwinkeln verbunden. Von den aufgehellten Lippenschilden sind die vorderen deutlich dunkel umrandet. Die Zunge ist dunkelblau bis schwarz.[1]
- Populationen auf Südost-Neuguinea (Süd-Irian Jaya), sowie den kleineren Inseln Aru, Kai, Biak und Neubritannien zeigen eine mittel- bis dunkelbraune Grundfarbe. Sie kommen in gemusterter oder ungemusterter Form vor; Zwischenformen existieren nicht. Gemusterte Tiere tragen insbesondere auf der hinteren Körperhälfte eine gut sichtbare helle Musterung. Sowohl gemusterten als auch ungemusterten Tieren fehlen die schwarzen Nackenbänder. Die aufgehellten Lippenschilde können von einer dünnen dunklen Linie umrahmt sein. Die Zunge ist blau und besitzt rosa Spitzen.[1]
Im Osten Neuguineas (Papua-Neuguinea), östlich der Flussarme von Sepik und Fly, sind keine regionalen Abgrenzungen zwischen nördlichen und südlichen Populationen mehr auszumachen. Es wird vermutet, dass die oben beschriebenen beiden Farbformen von West-Neuguinea eigenständige Arten sind und auf Ost-Neuguinea als auch auf dem Bismarck-Archipel sympatrisch vorkommen.[1]
Eine weitere abweichende Farbform existiert auf Neuirland. Von dieser Insel sind ungemusterte Tiere mit braun-grau-rosa Körperfarbe und abweichender Genetik bekannt.[1]
Alle Neuguinea-Amethystpythons besitzen goldene Augen, ein vom Augenhinterrand oberhalb der Oberlippe bis zum Maulwinkel ziehendes dunkles Band, sowie einen weißgrau gefärbten Bauch.[1]
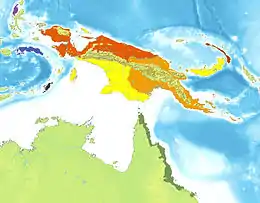
Verbreitung und Lebensraum
Die Art bewohnt den Bismarck-Archipel, Neuguinea, die Neuguinea angrenzenden Inseln Aru, Kai, Trobriand, Murray, Biak, Yapen, Normanby, Rossel, Daru, Bobo sowie die Inseln Misool und Salawati der Torres-Straße.[1]
Auf Neuguinea besiedeln diese Pythons eine Vielzahl verschiedener Habitate, von der Savanne bis zum Regenwald.[4] Am Mount Rawlinson der Huon-Halbinsel erreichen sie Höhenlagen bis 1585 Meter[5] über Meer und auf Irian Jaya sogar bis 1800 Meter[1].
Verhalten
Die Lebensweise dieses Pythons ist noch weitgehend unerforscht. Zur Nahrung zählen diverse Nagetiere und Vögel. Warane sollen gelegentlich auch gefressen werden. Zu den natürlichen Feinden des Neuguinea-Amethystpythons zählt unter anderem der ophiophage Papuapython.[4]
Systematik
Der Amethystpython wurde 1801 von Schneider unter der wissenschaftlichen Bezeichnung Morelia amethistina erstbeschrieben. 1933 wies Stull der australischen Population als Morelia amethistina kinghorni Unterartstatus zu. Im Jahr 2000 differenzierten Harvey et al. unter Berücksichtigung von morphologischen, biogeographischen und molekulargenetischen Aspekten fünf eigenständige Arten: Morelia amethistina, Morelia kinghorni, Morelia nauta, Morelia clastolepis und Morelia tracyae. Alle bisher beschriebenen Amethystpythons bewohnen räumlich voneinander getrennte Lebensräume (Allopatrie). Es wird jedoch vermutet, dass unter den bisher beschriebenen Arten noch weitere Arten differenziert werden können, die teilweise sogar gleiche Gebiete bewohnen (Sympatrie). Hierzu besteht insbesondere auf Neuguinea und Neuirland starker Verdacht.
Es wird vermutet, dass einst eine Urform der Amethystpythons auf dem entstehenden Neuguinea gelebt hat. Vor Millionen von Jahren haben sich dann in einer ersten Phase die Inseln Halmahera und Neuirland durch tiefe Meeresengen von Neuguinea getrennt was die dortigen Amethystpython-Populationen komplett isolierte. Während späterer Eiszeiten bildeten sich durch den niedrigen Meeresspiegel Landbrücken zwischen Neuguinea und benachbarten Inseln sowie dem australischen Festland. So besiedelten Amethystpythons in einer zweiten Phase die D’Entrecasteaux-Inseln, den Louisiade-Archipel, Aru. Seram, Ambon, Yapen, küstennahe Inseln der Torres-Straße und Nordaustralien. Mittels Treibholz konnten diese Pythons dann in einer dritten Phase von Aru auf die benachbarte Insel Kai, und solche von Yapen auf die Nachbarinsel Biak gelangten. Auch die Tanimbar-Inseln hatten nie Kontakt zu anderen Landmassen, wodurch Vorläufer dieser Population ebenfalls über den Wasserweg die Inseln besiedelt haben müssen. Da sich Neuguinea geotektonisch ebenfalls noch stark veränderte, konnte sich die Urform des Amethystpythons auch hier noch lokal differenzieren.
Diese Pythons sind am nächsten mit dem Boelen-Python (Morelia boeleni) verwandt. Die charakteristische Gemeinsamkeit von Amethyst- und Boelen-Pythons ist das Vorhandensein von mindestens zwei Paaren großer Scheitelschilde. 1984 wurde von Wells & Wellington[6] vorgeschlagen, Amethystpythons von den Rautenpythons (Morelia) als eigenständige Gattung mit Namen Australiasis abzutrennen.
Der Gattungsname Australiasis ist allerdings ungültig, da die Gattung in einer Zeitschrift beschrieben wurde, die kein Peer-Review-Verfahren durchführt.[7] Anfang 2014 wurde deshalb der Gattungsname Simalia (Gray, 1849) für eine neue aus dem Boelen-Python, dem Oenpelli-Python und den Amethystpythons zusammengesetzte Gattung eingeführt.[8]
Die Verwandtschaftsverhältnisse stellen sich nach Harvey et al. (2000) und Reynolds et al. (2014) wie folgt dar:
| Simalia |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Molekulargenetisch unterscheiden sich die Amethystpythons vom Nordwest-Neuguinea deutlich den anderen Neuguinea-Amethystpythons und auch von anderen Amethystpythonarten. Es scheint sich um eine eigene evolutionäre Linie zu handeln. Ausnahme bilden jedoch drei nahe der nordwestlichen Küste Neuguineas auf der Insel Biak untersuchte Tiere. Diese Individuen trugen nicht die sonst typischen Nackenbänder und waren genetisch viel näher mit der Population auf Südwest-Neuguinea verwandt. Weil die Untersuchung nur mit einer kleinen Datenmenge durchgeführt wurde und unklar ist, wie solch eine Besiedlung von Biak zustande kommen konnte, haben Harvey et al. 2000 vorderhand von einer weiteren Aufspaltung von Simalia amethistina abgesehen. Ihre bisherigen molekulargenetischen Ergebnisse legen jedoch nahe, dass es sich bei Simalia amethistina nicht um eine polyphyletische Art, sondern um mehrere Arten handelt.[1]
Quellen
Einzelnachweise
- M. B. Harvey, D. G. Barker, L. K. Ammerman, P. T. Chippindale: Systematics of Pythons of the Morelia amethistina Complex (Serpentes: Boidae) with the Description of three new Species. Herpetological Monographs 14, 2000, S. 139–185.
- G. A. Mengden, A. D. Stork: Chromosomal evolution in Serpentes: a comparison of G and C chromosome banding patterns of some colubrid and boid genera. Chromosoma 79, 1980, S. 53–64. Zit. in. M. B. Harvey, D. G. Barker, L. K. Ammerman, P. T. Chippindale: Systematics of Pythons of the Morelia amethistina Complex (Serpentes: Boidae) with the Description of three new Species. Herpetological Monographs 14, 2000, S. 156.
- S. B. McDowell: A catalogue of the snakes of New Guinea an the Solomons, with spezial reference to those in the Bernice P. Bishop Museum. Part II. Anilioidea and Pythoninae. Journal of Herpetology 9, 1975, S. 1–79. (Anhand der beschriebenen Lokalitäten, wurden so weit wie möglich artspezifische Daten entnommen, die auf den heutigen Neuguinea-Amethystpython zutreffen).
- M. O’Shea: A guide to the snakes of Papua New Guinea. Craft Print Pte Ltd., Singapore 1996, ISBN 9980-916-96-6, S. 76–77.
- S. B. McDowell: Results of the Archibold Expeditions. No. 112. The Snakes of the Huon Peninsula, Papua New Guinea. American Museum Novitates 2775, 1984, S. 1–28. Zit. in. M. B. Harvey, D. G. Barker, L. K. Ammerman, P. T. Chippindale: Systematics of Pythons of the Morelia amethistina Complex (Serpentes: Boidae) with the Description of three new Species. Herpetological Monographs 14, 2000, S. 156.
- R. W. Wells, C. R. Wellington: A classification of the Amphibia and Reptilia of Australia. Australian Journal of Herpetology, Supplementary Series, Heft 1, 1984 S. 1–61, Volltext (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis.
- Hinrich Kaiser, Brian I. Crother, Christopher M. R. Kelly, Luca Luiselli, Mark O´Shea, Hidetoshi Ota, Paulo Passos, Wulf D. Schleip, Wolfgang Wüster: Best Practices: In the 21st Century, Taxonomic Decisions in Herpetology are Acceptable Only When Supported by a Body of Evidence and Published via Peer-Review. In: Herpetological Review, 2013, 44(1), 8–23.. 44, 2013, S. 8–23.
- R. Graham Reynolds, Matthew L. Niemiller, Liam J. Revell: Toward a Tree-of-Life for the boas and pythons: Multilocus species-level phylogeny with unprecedented taxon sampling. Molecular Phylogenetics and Evolution, Volume 71, February 2014, Pages 201–213, doi: 10.1016/j.ympev.2013.11.011
Literatur
- M. B. Harvey, D. G. Barker, L. K. Ammerman, P. T. Chippindale: Systematics of Pythons of the Morelia amethistina Complex (Serpentes: Boidae) with the Description of three new Species. Herpetological Monographs 14, 2000, S. 139–185.
- S. B. McDowell: A catalogue of the snakes of New Guinea an the Solomons, with spezial reference to those in the Bernice P. Bishop Museum. Part II. Anilioidea and Pythoninae. Journal of Herpetology 9, 1975, S. 1–79.
Weblinks
- Simalia amethistina In: The Reptile Database
- Morelia amethistina in der Roten Liste gefährdeter Arten der IUCN 2013.2. Eingestellt von: Auliya, M., 2009. Abgerufen am 31. Januar 2014.