Seram-Python
Der Seram-Python (Simalia clastolepis, Syn.: Morelia clastolepis), auch Goldpython, zählt zur Familie der Pythons (Pythonidae) und wird dort in die Gattung der Rautenpythons (Morelia) gestellt. Die Art wurde erst im Jahr 2000 vom Amethystpython abgetrennt. Über die Biologie dieser auf Ambon und Seram beheimateten Schlange ist fast nichts bekannt.
| Seram-Python | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|

Simalia clastolepis, xanthisch | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Simalia clastolepis | ||||||||||||
| (Harvey, Barker, Ammerman & Chippindale, 2000) |
Beschreibung
Körperbau und Länge
Der Seram-Python ist ein schlanker, aber dennoch ziemlich kräftig gebauter Python. Der lange Schwanz macht bis zu 27 % der Gesamtlänge aus. Der Kopf ist deutlich vom Hals abgesetzt und bei adulten Weibchen deutlich verbreitert. Die Augen liegen an den Kopfseiten auf und sind leicht nach vorne gerichtet. Die rundliche, von oben betrachtet halbovale Schnauze ist bei Männchen länger ausgeprägt als bei Weibchen. Ihr sitzen die runden Nasenlöcher schräg zwischen Kopfoberseite und Kopfseite auf. Bei diesem Python handelt es sich um einen großen Vertreter unter den Amethystpythons. Da die Art bisher nur anhand weniger Individuen untersucht werden konnte, liegen noch keine Daten zur Durchschnittslänge adulter Tiere vor. Das größte bisher untersuchte Tier hatte eine Gesamtlänge von 3,8 Meter und ein Gewicht von 8,5 Kilogramm.
Beschuppung
Von allen Amethystpythons besitzt der Seram-Python die höchste Anzahl Schilder, wovon auch der wissenschaftliche Name herrührt. Das von oben nur mäßig sichtbare Rostrale (Schnauzenschild) hat, wie bei den meisten anderen Pythons auch, zwei tiefe Labialgruben. Die Nasenlöcher sind jeweils im oberen hinteren Teil des großen Nasale (Nasenschild) positioniert. Vom Nasenloch bis zum Hinterrand des Schildes zieht eine gut erkennbare Naht. Zur Kopfmitte hin sind die Nasalia von einem großen Paar dreieckiger Internasalia (Zwischennasenschilden) separiert. Von der Schnauzenspitze her entlang der Mittellinie der Kopfoberseite folgen den Internasalia ein großes vorderes Paar Präfrontalia (Vorstirnschilde). Das hintere Paar Präfrontalia hat charakteristischerweise keinen Kontakt zueinander, sondern wird durch die vorderen Präfrontalia oder einem bis mehreren zusätzlichen dazwischen liegenden Schilden separiert. Dahinter folgt ein einfaches großes Frontale (Stirnschild). Die anschließenden Schilde der Scheitel- und Hinterhauptsregion sind bei dieser Art viel variabler, meist asymmetrischer und in einer höheren Anzahl ausgebildet als bei anderen Amethystpythons. Häufig sind hinter dem Frontale zwei bis drei Paare größerer Parietalia (Scheitelschilde) vorhanden, die miteinander in der Mitte in Kontakt stehen oder durch bis 10 unregelmäßige, asymmetrische Interparietalia (Zwischenscheitelschilde) getrennt werden. Dahinter folgen unregelmäßige, in der Anzahl variierende Occipitalia (Hinterhauptsschilde), die etwas größer als die angrenzenden Nuchealia (Nackenschilde) sind. Über beiden Augen befindet sich je ein großes dreieckiges, manchmal partiell fragmentiertes Supraoculare (Überaugenschild). Präocularia (Voraugenschilde) existieren zwei bis vier, wobei das oberste oft vergrößert ist. Postocularia (Hinteraugenschilde) sind vier bis sechs vorhanden. Im Gegensatz zu allen andern Amethystpythons kann die Art zwischen einem bis drei Subocularia (Unteraugenschilde) besitzen. Auf der Seite des Kopfes liegen zwischen Auge und Nasenloch, in zwei bis drei Reihen angeordnet, Lorealia (Zügelschilde). Von den 12 bis 13 Supralabialia (Oberlippenschilde) tragen die vordersten drei an ihrem hinteren Rand lange, tiefe und zwei weitere dahinter anschließende kleine, oberflächliche Labialgruben. Sofern Unteraugenschilde fehlen, berühren ein bis drei Supralabialia den Augenunterrand. Infralabialia (Unterlippenschilde) gibt es 20 bis 23, wovon die vordersten zwei schwach erkennbare und, von Nummern 9 bis 11 beginnend, 6 bis 9 tiefe Labialgruben tragen. Die Kinngrube besteht aus schilderloser Haut; kann aber bis zu 10 Schilde beherbergen.
Die Anzahl der Ventralia (Bauchschilde) variiert zwischen 301 und 309, die Anzahl der dorsalen Schuppenreihen in der Körpermitte zwischen 45 und 52. Von der Kloake bis zur Schwanzspitze finden sich 93 bis 99 nur teilweise paarige Subcaudalia (Schwanzunterseitenschilde). Das Anale (Analschild) ist ungeteilt.
Färbung
Der Seram-Python kommt in zwei verschiedenen Farbmorphen, einer mit hohem Gelbanteil (xanthisch) und einer ohne Gelbanteil (axanthisch), vor:
- Xanthische adulte Tiere besitzen eine braune Grundfarbe und ein etwas aufgehelltes gelbliches Muster.
- Erwachsene, axanthische Vertreter haben eine graue Grundfarbe und sind in einem etwas aufgehellten Grauweiß gemustert.
Die Grundfarbe wird auf der hinteren Körperhälfte zur Schwanzspitze zunehmend dunkler. Der Rücken ist dunkler gefärbt als die Flanken; bei Weibchen kann sich dieser Bereich mit dem Alter jedoch auf das Farbniveau des Rückens abdunkeln. Auf der vorderen Körperhälfte subadulter und junger adulter Tieren verläuft beidseits der Wirbelsäule je eine Reihe kleiner, undeutlicher heller Flecken mit 2 bis 3 Schilden Durchmesser. Die Flecken jeder Reihe haben jeweils 3 bis 5 Schilde Abstand zueinander, sind quer über Rücken durch 2 bis 3 Schilde separiert, können entlang der Wirbelsäule parallel oder versetzt angeordnet sein und teilweise quer über die Wirbelsäule miteinander fusionieren. Weniger häufig verschmelzen diese Rückenflecken auch zu einer 2 bis 3 Schilde breiten hellen Mittellinie, die beidseits von einer 1 bis 2 Schilde breiten dunklen Linie begleitet wird. Auf der hinteren Körperhälfte Richtung Schwanzspitze werden die hellen Rückenflecken beidseits der Wirbelsäule zunehmend deutlicher, länger und bilden schlussendlich Bänder, die vom Rücken bis zum Unterrand der Flanken ziehen. Dadurch ergibt sich auf dem Schwanz eine abwechselnd hell- dunkle Bänderung. Mit zunehmendem Alter werden die Rückenflecken der Körperforderseite undeutlicher und können bei adulten Tieren komplett verschwinden. Auf der hinteren Körperhälfte bleibt die Musterung aber meist in undeutlicher Form erhalten. Von der einheitlich weißgrau gefärbten Bauchseite fließt die Farbe in relativ regelmäßigen Abständen bis an die unteren Flankenschilde empor. An ihrem oberen Rand wird sie insbesondere gegen den Schwanz hin von einer oft unterbrochenen dünnen dunklen Linie begleitet.
Kopfoberseite und Kopfseite sind ungemustert und entsprechen der Körpergrundfarbe. Die meisten Schilde der Kopfoberseite sind von einer feinen dunklen Linie umgeben. Lippen- und Kinnschilde sowie die Kehle sind bei beiden Farbformen weiß bis weißgrau. Im Gegensatz zu mehreren anderen Amethystpythons sind die Lippenschilde dieser Art nicht dunkel umrandet. Bei Jungtieren zieht ein dunkles Band hinter dem Auge oberhalb der Oberkante der Oberlippenschilde bis zum Maulwinkel. Dieses Band verschwindet im Verlauf der Entwicklung vollkommen, was den Seram-Python von allen anderen Amethystpythons abhebt. Ebenso fehlen ihnen die sonst für Amethystpythons typischen Nackenbänder. Die Iris ist bei axanthischen Tieren dunkelgrau bis schwarz, bei xanthischen Vertretern golden, kupferfarben bis orangebraun und um die Pupille herum mit einem aufgehellten Rand versehen. Die Spitzen der dunkelblau bis blaugrauen Zunge sind bei xanthischen Tieren rosa und bei axanthischen Vertretern grau oder weiß aufgehellt.
Farbwechsel
Xanthische Tiere machen einen beachtlichen ontogenetischen Farbwechsel durch. Die anfangs ziegelroten Jungtiere durchlaufen der Reihe nach eine rote-, eine braune-, eine orange, eine mattgelbe und dann eine kräftiggelbe Phase. Nach zirka zwei Jahren ändert sich diese gelbe Farbe zunehmend in braun. Die Flanken xanthischer Männchen bleiben das ganze Leben lang mattgelb oder golden während dieser Bereich bei Weibchen komplett braun wird. Tragende- und brütende Weibchen werden an ihrer Oberseite sogar beinahe komplett braunschwarz. Axanthische Tiere machen nur einen geringen ontogenetischen Farbwechsel durch; sie werden lediglich dunkler mit dem Alter.
Verbreitung
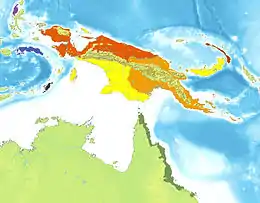
Der Seram-Python bewohnt auf den Molukken die Inseln Ambon und Seram. Es wird vermutet, dass die Art auch die benachbarten Inseln Haruku und Saparua besiedelt. Diese sind weniger als 200 Meter von Ambon und Seram entfernt und waren während der Eiszeiten stets über Landbrücken miteinander in Verbindung gestanden.
Lebensweise
Die Lebensweise des Seram-Pythons ist noch weitgehend unerforscht. Auf Seram im Nationalpark Manusela bewohnt sie Tiefland-Regenwald und Gewässern angrenzenden Tiefland-Wald. In diesem Gebiet wird sie auch unter tags angetroffen und hält sich sowohl im Geäst als auch auf dem Boden auf.[1] Das Nahrungsspektrum ist ebenfalls noch unbekannt. In einem großen Individuum ist bisher einzig ein Kuskus nachgewiesen worden.[2]
Systematik
Der Amethystpython wurde 1801 von Schneider unter der wissenschaftlichen bezeichnung Morelia amethistina erstbeschrieben. 1933 wies Stull der australischen Population als Morelia amethistina kinghorni Unterartstatus zu. Im Jahr 2000 differenzierten Harvey et al. unter Berücksichtigung von morphologischen, biogeographischen und molekulargenetischen Aspekten fünf eigenständige Arten: Morelia amethistina, Morelia kinghorni, Morelia nauta, Morelia clastolepis und Morelia tracyae. Alle bisher beschriebenen Amethystpythons bewohnen räumlich voneinander getrennte Lebensräume (Allopatrie). Es wird jedoch vermutet, dass unter den bisher beschriebenen Arten noch weitere Arten differenziert werden können, die teilweise sogar gleiche Gebiete bewohnen (Sympatrie). Hierzu besteht insbesondere auf Neuguinea und Neuirland starker Verdacht.
Es wird vermutet, dass einst eine Urform der Amethystpythons auf dem entstehenden Neuguinea gelebt hat. Vor Millionen von Jahren haben sich dann in einer ersten Phase die Inseln Halmahera und Neuirland durch tiefe Meeresengen von Neuguinea getrennt was die dortigen Amethystpython-Populationen komplett isolierte. Während späterer Eiszeiten bildeten sich durch den niedrigen Meeresspiegel Landbrücken zwischen Neuguinea und benachbarten Inseln sowie dem australischen Festland. So besiedelten Amethystpythons in einer zweiten Phase die D’Entrecasteaux-Inseln, den Louisiade-Archipel, Aru. Seram, Ambon, Yapen, küstennahe Inseln der Torres-Straße und Nordaustralien. Mittels Treibholz konnten diese Pythons dann in einer dritten Phase von Aru auf die benachbarte Insel Kai, und solche von Yapen auf die Nachbarinsel Biak gelangten. Auch die Tanimbar-Inseln hatten nie Kontakt zu anderen Landmassen, wodurch Vorläufer dieser Population ebenfalls über den Wasserweg die Inseln besiedelt haben müssen. Da sich Neuguinea geotektonisch ebenfalls noch stark veränderte, konnte sich die Urform des Amethystpythons auch hier noch lokal differenzieren.
Diese Pythons sind am nächsten mit dem Boelen-Python (Morelia boeleni) verwandt. Die charakteristische Gemeinsamkeit von Amethyst- und Boelen-Pythons ist das Vorhandensein von mindestens zwei Paaren großer Scheitelschilde. 1984 wurde von Wells & Wellington[3] vorgeschlagen, Amethystpythons von den Rautenpythons (Morelia) als eigenständige Gattung mit Namen Australiasis abzutrennen.
Der Gattungsname Australiasis ist allerdings ungültig, da die Gattung in einer Zeitschrift beschrieben wurde, die kein Peer-Review-Verfahren durchführt.[4] Anfang 2014 wurde deshalb der Gattungsname Simalia (Gray, 1849) für eine neue aus dem Boelen-Python und den Amethystpythons zusammengesetzte Gattung eingeführt.[5]
Die Verwandtschaftsverhältnisse stellen sich nach Harvey et al. (2000) und Reynolds et al. (2014) wie folgt dar:
| Simalia |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Simalia clastolepis erhielt ihren wissenschaftlichen Namen aufgrund ihrer zahlreichen und stark fragmentierten Schilde. Das altgriechische Adjektiv κλαστός klastós bedeutet ‚in Stücke zerbrochen‘ und das altgriechische Nomen λεπίς lepís, deutsch ‚Schild‘.
Quellen
Einzelnachweise
- P. W. Edgar, R. P. H. Lilley: Herpetofauna survey of Manusela National Park. In I. D. Edwards, A. A. MacDonald, J. Proctor (Hsg.): Natural History of Seram Maluku, Indonesia. Intercept Ltd 1993, S. 131–141. Zit. in M. B. Harvey, D. G. Barker, L. K. Ammerman, P. T. Chippindale: Systematics of Pythons of the Morelia amethistina Complex (Serpentes: Boidae) with the Description of three new Species. Herpetological Monographs 14, 2000, S. 161.
- F. Kopstein: Reptilien von den Molukken und den benachbarten Inseln. Zoologische Mededelingen 9, 1926, S. 71–112. Zit. in: M. B. Harvey, D. G. Barker, L. K. Ammerman, P. T. Chippindale: Systematics of Pythons of the Morelia amethistina Complex (Serpentes: Boidae) with the Description of three new Species. Herpetological Monographs 14, 2000, S. 161.
- R. W. Wells, C. R. Wellington: A classification of the Amphibia and Reptilia of Australia. Australian Journal of Herpetology, Supplementary Series, Heft 1, 1984 S. 1–61, Volltext (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis.
- Hinrich Kaiser, Brian I. Crother, Christopher M. R. Kelly, Luca Luiselli, Mark O´Shea, Hidetoshi Ota, Paulo Passos, Wulf D. Schleip, Wolfgang Wüster: Best Practices: In the 21st Century, Taxonomic Decisions in Herpetology are Acceptable Only When Supported by a Body of Evidence and Published via Peer-Review. In: Herpetological Review, 2013, 44(1), 8–23.. 44, 2013, S. 8–23.
- R. Graham Reynolds, Matthew L. Niemiller, Liam J. Revell: Toward a Tree-of-Life for the boas and pythons: Multilocus species-level phylogeny with unprecedented taxon sampling. Molecular Phylogenetics and Evolution, Volume 71, February 2014, Pages 201–213, doi: 10.1016/j.ympev.2013.11.011
Literatur
- M. B. Harvey, D. G. Barker, L. K. Ammerman, P. T. Chippindale: Systematics of Pythons of the Morelia amethistina Complex (Serpentes: Boidae) with the Description of three new Species. Herpetological Monographs 14, 2000, S. 139–185.