Mycobacterium bovis
Mycobacterium bovis ist ein beim Rind vorkommendes Bakterium und ist Erreger der Tuberkulose der Rinder. Mycobacterium bovis kann auch auf den Menschen sowie andere Haustiere (Ziegen) übertragen werden. Die Infektion des Menschen erfolgt vor allem durch nicht-pasteurisierte Milch (Rohmilch), ist aber in den industrialisierten Ländern mittlerweile sehr selten.[1]
| Mycobacterium bovis | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
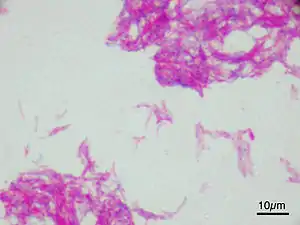
Mycobacterium bovis | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Mycobacterium bovis | ||||||||||||
| Karlson & Lessel 1970 |
Mycobacterium bovis zählt zum Mycobacterium tuberculosis-Komplex, aus dem es wahrscheinlich vor mehreren zehntausend Jahren entstanden ist.
Durch jahrelang wiederholte Kultivierung von M. bovis wurde der Lebendimpfstoff BCG (Bacillus Calmette-Guérin) geschaffen, ein Impfstoff gegen die durch M. tuberculosis ausgelöste Tuberkulose des Menschen.
Das Genom wurde vollständig sequenziert.
Merkmale
Mycobacterium bovis ist wie alle Arten und Stämme der Mycobacteriaceae Gram-positiv. Die unbeweglichen Zellen sind stäbchenförmig und bilden keine Sporen. Das Bakterium ist säurefest, ein typisches Merkmal der Mykobakterien. Ein weiteres wichtiges Merkmal ist bei allen Mykobakterien der Aufbau der Zellwand (unter anderem ein hoher Lipid-Gehalt und Gehalt an wachsartigen Substanzen, wie Mykolsäuren). Auf den speziellen Zellwandaufbau ist die Resistenz gegen verschiedene Antibiotika und die Säurefestigkeit zurückzuführen. Säurefeste Bakterien geben nach Einfärbung die Farbstoffe trotz einer Säurebehandlung nicht wieder ab. Eine erste Identifikation kann durch die Ziehl-Neelsen-Färbung erfolgen. Nach einer Färbung werden die Bakterien mit Säure behandelt, nur die säurefesten Bakterien bleiben gefärbt. Säurefest sind allerdings auch andere entfernt verwandte Bakterien wie Arten von Nocardia, Rhodococcus und Corynebacterium.
Alle Mykobakterien weisen einen chemoorganotrophen Stoffwechsel auf und benötigen Sauerstoff (allerdings überleben M. bovis-Kulturen auch kurze mikroaerobe Perioden).
Mycobacterium bovis ist obligat pathogen und wie Mycobacterium tuberculosis nicht in der Lage, sich außerhalb des Wirtes fortzupflanzen. Allerdings sind die Mykobakterien durch die besondere Zellwand sehr gut gegen äußere Einflüsse geschützt und können auch außerhalb des Wirtes eine Zeitlang überleben. Im Kot von Rindern sollen sie noch nach bis zu 13 Tage wachstumsfähig sein.[2]
Unterschiede zu anderen Mykobakterien
Die Polymerase-Kettenreaktion (PCR) ist eine gängige Methode, um Mycobacterium bovis von anderen Mykobakterien zu differenzieren. Des Weiteren haben die verschiedenen Stämme morphologische (an den Kulturen sichtbare) und biochemische Unterschiede. Kulturen von Mycobacterium bovis zeigen ein glattes, feuchtglitzerndes Aussehen und eine Zugabe von Glycerin wirkt wachstumshemmend. Zwei Differenzierungsmerkmale zu M. tuberculosis-Kulturen deren Wachstum durch Glycerin gefördert würde und die auf Nährmedien eher krümelig und trocken imponieren. Mycobacterium tuberculosis ist zur Bildung von Niacin im Zuge der Nitratreduktion befähigt, M. bovis nicht.
Direkt nach der Kultivierung verhält sich Mycobacterium bovis mikroaerophil, es wächst am besten in Umgebungen mit geringem Sauerstoffgehalt. Nach wiederholter Kultivierung benötigen die Stämme für das Wachstum einen normalen (21 %) Sauerstoffgehalt und sind dann wie alle anderen Mykobakterien obligat aerob. Dies ist ein weiterer Unterschied zu Mycobacterium tuberculosis, welches nur bei vollem Sauerstoffgehalt bestes Wachstum zeigt.
Tuberkulose der Rinder
_031_Tuberkul%C3%B6ses_Brustfell_eines_Rindes.png.webp)
Die Übertragung von Mycobacterium bovis erfolgt bei Rindern meist über den Luftweg (Tröpfcheninfektion). Die Bakterien können auch mit infiziertem Futter, Milch oder Wasser aufgenommen werden.
Mycobacterium bovis kann auf andere Tiere wie Katzen, Hunde, Schafe, Schweine und Ziegen übertragen werden. Rindertuberkulose kann auch in der Zoohaltung auftreten, M. bovis wurde z. B. aus Leoparden, Seelöwen und Pavianen isoliert.[3]
In Deutschland wurden in den 50er Jahren Bekämpfungsmaßnahmen gegen die Rindertuberkulose durchgeführt, wodurch diese Krankheit fast vollständig ausgerottet wurde. So waren im Jahr 1952 noch 38,5 % der untersuchten Rinder infiziert, im Jahr 1967 nur noch 0,09 %.[2] Nach der Ausrottung der Rindertuberkulose in den Industrieländern stellt das Rind selbst nicht mehr die Hauptinfektionsquelle dar. Vielmehr ist nun eine Ansteckung des Rindes durch Haustiere (z. B. Katzen) oder auch durch Wildtiere die Hauptgefahr für den Ausbruch der Rindertuberkulose. Auch der an offener Tuberkulose erkrankter Mensch stellt eine Infektionsquelle für Rinder (dann jedoch nicht nur durch M. bovis).[2]
Neuseeland
Mitte Juli 2017 wurde die Krankheit erstmals auf einem Milchviehbetrieb auf der Südinsel Neuseelands entdeckt, mittlerweile hat sie sich auch auf die Nordinsel ausgebreitet. Die Erreger können bei Kühen zu behandlungsresistenten Mastitiden, Fruchtbarkeitsstörungen und Fehlgeburten führen oder generell bei Rindern Lungenerkrankungen und Gelenkentzündungen auslösen. Das Landwirtschaftsministerium entschied Ende März 2018, dass alle Rinder auf infizierten Höfen gekeult werden müssten. Betroffen waren 22 Haltungen mit zusammen rund 22'300 Rindern. Bis zum Dezember 2017 waren bereits 3500 Tiere getötet worden.[4][5] Im Mai 2018 war von weiteren 150'000 geplanten Keulungen die Rede.[6][7][8]
Bedeutung für den Menschen
Die Rindertuberkulose, im englischen als „bovine TB“ bezeichnet, ist auch auf dem Menschen übertragbar und zählt somit zu den Zoonosen.[9] Die Infektion erfolgt (wie beim Rind) über die Atemwege oder durch Nahrungsaufnahme, oft durch unpasteurisierte Milch. Bei letzterer kann eine Darmtuberkulose ausgelöst werden. Die Rindertuberkulose kann zwischen Menschen und Rindern hin und her übertragen werden.
Durch die Einführung der Pasteurisierung der Milch ging die Anzahl der Übertragungen auf dem Menschen jedoch stark zurück. Die durch Mycobacterium bovis ausgelöste Tuberkulose spielt in den Industrieländern kaum noch eine Rolle, in den Entwicklungsländern ist sie allerdings noch von Bedeutung. In einer argentinischen Studie konnten zwei Prozent der 448 untersuchten Fälle von Lungentuberkulose auf Infektion mit M. bovis zurückgeführt werden. Die dort nachgewiesenen Bakterienstämme waren gleichzeitig diejenigen, die auch am häufigsten Rinder befallen.[10] Eine chinesische Studie ergab eine Prävalenz von 0,34 Prozent von M. bovis-Krankheitsfällen.[11]
Die Veränderungen der betroffenen Organe von einer durch Mycobacterium bovis ausgelösten Tuberkulose sind nicht von den M. tuberculosis-Tuberkuloseläsionen unterscheidbar.
Systematik
Innerhalb der Gattung Mycobacterium wird Mycobacterium bovis und auch M. bovis BCG dem „Mycobacterium tuberculosis-Komplex“ zugerechnet.
Die zwei Unterarten (Subspezies) Mycobacterium bovis subsp. bovis und Mycobacterium bovis subsp. caprae werden nicht mehr geführt. Die letztere wird nun zu der Art Mycobacterium caprae gestellt.[12]
Synonyme für Mycobacterium bovis sind Mycobacterium tuberculosis typus bovinus Lehmann & Neumann 1907 und Mycobacterium tuberculosis var. bovis Bergey et al. 1934.[12]
Meldepflicht
In Deutschland ist der direkte Nachweis von Mycobacterium bovis beim Menschen namentlich meldepflichtig nach § 7 des Infektionsschutzgesetzes.[13] Die Meldepflicht gilt nur soweit der direkte Nachweis auf eine akute Infektion hinweist sowie nachfolgend für das Ergebnis der Resistenzbestimmung; vorab auch für den Nachweis säurefester Stäbchen im Sputum.
In der Schweiz ist der positive und negative laboranalytische Befund von Erregern aus dem Mycobacterium tuberculosis-Komplex beim Menschen meldepflichtig und zwar nach dem Epidemiengesetz (EpG) in Verbindung mit der Epidemienverordnung und Anhang 3 der Verordnung des EDI über die Meldung von Beobachtungen übertragbarer Krankheiten des Menschen.
Literatur
- Martin Dworkin, Stanley Falkow, Eugene Rosenberg, Karl-Heinz Schleifer, Erko Stackebrandt (Hrsg.): The Prokaryotes, A Handbook of the Biology of Bacteria. 7 Bände, 3. Auflage. Springer, New York u. a. O., 2006, ISBN 0-387-30740-0. Band 3: Archaea. Bacteria: Firmicutes, actinomycetes. ISBN 0-387-25493-5.
- John G. Holt (Hrsg.): Bergey’s manual of systematic bacteriology. Band 2, 1986, ISBN 0-683-07893-3.
- Werner Köhler (Hrsg.) Medizinische Mikrobiologie. 8. Auflage. München/Jena 2001, ISBN 978-3-437-41640-8.
- Michael Rolle, Anton Mayr (Hrsg.): Medizinische Mikrobiologie, Infektions- und Seuchenlehre. 7. Auflage. Enke, Stuttgart 1993, ISBN 3-432-84686-X.
Weblinks
Einzelnachweise
- S. I. Cadmus, H. K. Adesokan u. a.: Mycobacterium bovis and M. tuberculosis in goats, Nigeria. In: Emerging Infect. Dis. Band 15, Nr. 12, Dezember 2009, S. 2066–2067, ISSN 1080-6059. PMID 19961707. PMC 3044523 (freier Volltext).
- Michael Rolle, Anton Mayr (Hrsg.): Medizinische Mikrobiologie, Infektions- und Seuchenlehre. 7. Auflage. Enke Verlag, Stuttgart 1993, ISBN 3-432-84686-X.
- M.F Thorel, C. Karoui, A. Varnerot, C. Fleury und V. Vincent: Isolation of Mycobacterium bovis from baboons, leopards and a sea-lion. In: Veterinary research, Bd. 29, Nummer 2, März-April, 1998: S. 207–12. PMID 9601152
- N: 22'300 Rinder werden gekeult In: schweizerbauer.ch, 2. April 2018, abgerufen am 2. April 2018.
- NZ: Bereits 3'500 Rinder gekeult In: schweizerbauer.ch, 19. Dezember 2017, abgerufen am 2. April 2018.
- Rinder-Seuche in Neuseeland: 150'000 Kühe müssen sterben – für den Garaus einer Bakterie In: srf.ch, 28. Mai 2018, abgerufen am 29. Mai 2018.
- Sophia Wagner: Rinderseuche in Neuseeland - 150.000 Tiere sollen gekeult werden. In: deutschlandfunk.de. 13. Juni 2018, abgerufen am 29. August 2018.
- apa: Neuseeland muss wegen Seuche mehr als 150.000 Rinder schlachten. In: derstandard.at. 28. Mai 2018, abgerufen am 29. August 2018.
- Geoff Brumfiel: Badger battle erupts in England. Cull plan splits farmers, conservationists – and scientists. In: Nature. Band 490, 2012, S. 317–318, doi:10.1038/490317a
- Etchechoury I, Valencia GE, Morcillo N, et al.: Molecular typing of Mycobacterium bovis isolates in Argentina: first description of a person-to-person transmission case. In: Zoonoses and Public Health. 57, Nr. 6, September 2010, S. 375–81. doi:10.1111/j.1863-2378.2009.01233.x. PMID 19912616.
- Y. Chen, Y. Chao et al.: Potential challenges to the Stop TB Plan for humans in China; cattle maintain M. bovis and M. tuberculosis. In: Tuberculosis (Edinb). Band 89, Nummer 1, Januar 2009, S. 95–100, ISSN 1873-281X. doi:10.1016/j.tube.2008.07.003. PMID 19056318.
- Jean Euzéby, Aidan C. Parte: Genus Mycobacterium. In: List of Prokaryotic names with Standing in Nomenclature (LPSN). Abgerufen am 23. Dezember 2013.
- Tuberkulose. RKI-Ratgeber. In: rki.de. Robert Koch-Institut, 21. Februar 2013, abgerufen am 18. März 2020 (Meldepflicht gemäß IfSG).