Muskelaufbau
Muskelaufbau bezeichnet eine Vergrößerung der Muskulatur, die durch Belastungen bei zielgerichtetem Training wie z. B. beim Bodybuilding oder Bodyshaping, oder durch andersartige erhöhte physische Widerstände (Sport, Arbeit etc.) ausgelöst wird. Bei der Anpassung des Muskels durch Muskelaufbau kann zwischen Muskelhypertrophie, der Verdickung vorhandener Muskelfasern, und Muskelhyperplasie, der Neubildung von Muskelfasern, unterschieden werden, wobei Letztere beim Menschen in ihrer Existenz umstritten ist.
Muskelhypertrophie
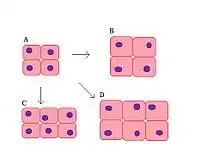
Muskelhypertrophie beschreibt die Vergrößerung des Muskulaturquerschnittes, hervorgerufen durch Dickenwachstum der Muskelfaser, nicht jedoch die Zunahme der Anzahl von Muskelzellen (Synzitien). Muskelhypertrophie in diesem Sinne findet statt, wenn die Muskulatur über ihr gewohntes Leistungsniveau hinaus beansprucht wird, was einen sogenannten Wachstumsreiz auslöst, welcher wiederum vermehrte Proteineinlagerung bewirkt (siehe dazu Anabolismus).
Muskelfasern sind die Bestandteile eines Muskels. Eine Muskelfaser ist eine Muskelzelle. Muskelzellen sind polyenergide Zellen, d. h., sie besitzen mehrere Zellkerne. Jeder Zellkern besitzt einen bestimmten „Einflussbereich“, den er durch seine Genexpression steuert. Dieser „Einflussbereich“ nennt sich myonukleare Domäne (engl. myonuclear domain, MND). Die Größe einer MND besitzt ein Maximum, das sich aus dem Verhältnis von Sarkoplasma und Zellkern ergibt, welches in einer Muskelzelle durch die Anforderungen eines optimalen Stoffwechsels bestimmt wird. Die MND kann sich durch Krafttraining vergrößern, indem durch einen Anabolismus Proteine eingelagert werden. Dies geschieht, indem mechanischer Stress in die Muskelzelle übertragen wird (Mechanotransduktion). Dabei werden Focal-Adhesion-Kinasen (FAK) aktiviert, die in der Folge eine Reaktionskette in Gang setzen, welche die Synthese von Muskelprotein (beispielsweise kontraktile Proteine wie Aktin und Myosin, zytoskeletale Proteine und Enzyme des Citratzyklus) anregen.
Dabei gibt es zwei bedeutende Stoffwechselwege: den mechanischen (über MAPKp3) und einen rein metabolischen (über MAPKerk1/2). Der Letztere wird durch metabolische Reize wie ein Sauerstoffdefizit und hypoxische Nebenprodukte wie Laktat und Sauerstoffradikale und durch die Änderung des pH-Wertes aktiviert. Es wird angenommen, dass der metabolische Wirkungsmechanismus einen deutlich geringeren Wachstumsreiz verursacht als der mechanische Stoffwechselweg. Er führt eher zu einer Anpassung der oxidativen Kapazität. Der mechanische Stoffwechselweg wird durch Mikrotraumata aktiviert und hat eine größere Bedeutung bezüglich Hypertrophie, da er neben einer Steigerung der Proteinbiosyntheserate, zu einer Fusionierung von Satellitenzellen mit der Muskelzelle führt, wodurch die Gesamtmenge an DNA in der Zelle zunimmt und somit das Hypertrophiepotential steigt.
Mikrotraumata sind kleinste Verletzungen der Zelle, ausgelöst durch überschwellige, mechanische Belastung und allerdings zu einem deutlich geringeren Anteil oxidativen Stress. Sie führen zu einer Produktion von muskelspezifischen IGF-1Ec (insulin-like growth factor, auch mechano growth factor [MGF] genannt), das nach außen dringt (parakrine Sekretion) und eine sogenannte Satellitenzellenkaskade in Gang setzt. Satellitenzellen (Myoblasten) sind eine Art Stammzellen, die noch weitestgehend undifferenziert sind und sich in der Nähe von Muskelfasern befinden. Diese werden durch den genannten Stoffwechselprozess aktiviert, differenzieren sich und bewegen sich zum Ort der Verletzung der Zellmembran (Chemotaxis), fusionieren dort mit der Muskelzelle und steuern dabei ihren Kern als weiteren Zellkern der Muskelzelle bei. So steigt die Gesamtmenge der DNA in der Muskelzelle und damit – aufgrund neuer MNDs – das Hypertrophiepotential. Mikrotraumata sind demnach essentiell für ein langfristig wirksames Training. Für den Muskelaufbau problematisch gestaltet sich, dass infolge der Synthese von Muskelprotein auch zytoskeletale Proteine (Stützproteine) synthetisiert werden, die die Zelle vor mechanischer Überlastung schützen soll. Aus diesem Grund muss das Training progressiv gestaltet werden.
Die genauen, äußerst komplexen Hypertrophiemechanismen sind noch nicht zur Gänze geklärt, aber dank neuer Technologien wie der Magnetresonanztomographie, mit der dreidimensionale Bilder einzelner Muskeln aufgenommen werden können, und der Dual-Röntgen-Absorptiometrie konnte die Hypertrophie in den letzten Jahren genauer erforscht werden. Die meisten bekannten, teilweise weiterhin populären Theorien, wie die Hypothese der gesteigerten Blutzirkulation, die Muskelhypoxie-Hypothese und die ATP-Mangel-Hypothese (das ATP-Niveau in der Zelle bleibt konstant), wurden widerlegt. Lediglich die Energietheorie und die Reiz-Spannungs-Theorie verbleiben theoretisch, die jedoch beide durch die neuen Erkenntnisse als Erklärungsmuster ad absurdum geführt wurden.
Muskelhypertrophie kann durch äußerliche Einwirkung wie gezieltes Training beim Bodybuilding, Kraftsport oder Krafttraining, erreicht werden.[1] Daneben kann das durch Training ausgelöste Muskelwachstum durch eine geeignete Ernährung, z. B. durch eiweißreiche Kost unterstützt werden. Darüber hinaus kann der Muskelaufbau durch exogene Faktoren künstlich stimuliert werden, z. B. durch die Einnahme von anabolen Hormonen (Wachstumshormone oder anabole Steroide). Diese Mittel nutzt man normalerweise für medizinische Therapien oder aber auch zum Doping. Insbesondere ihr regelmäßiger Einsatz zum Zweck des Muskelaufbaus birgt große gesundheitliche Risiken.
Durch Anabolika, Training und Protein nimmt die Anzahl der Muskelzellkerne deutlich zu (im Tierversuch um 66 %,[2] Muskelquerschnitt um 77 %), nach 3 Wochen ohne Anabolika hatte sich der Muskelquerschnitt wieder auf die Ausgangslage zurückentwickelt. Die Anzahl der Muskelkerne war jedoch nach 3 Monaten (=10 % der Lebenserwartung von Mäusen) noch immer so groß, dass 6-Tage Muskeltraining bei den zuvor behandelten Mäusen zu 31 % Muskelquerschnittsvergrößerung führte, bei einer nie behandelten Vergleichsgruppe jedoch nur um 6 %. Das zeigt nicht nur die Absurdität der Dopingkontrollen auf Anabolika, sondern widerlegt auch die MND-Hypothese.[3]
In einer Studie von Morton et al. (2016) wurde versucht zu zeigen, dass es keinen Unterschied für den Muskelaufbau macht, ob Gewichte schwer oder leicht sind. Vielmehr komme es darauf an, Gewichte „bis zur Erschöpfung“ anzuwenden:[4] Für die Studie stützen sich die Wissenschaftler auf zwei Probandengruppen, gebildet aus erfahrenen Gewichthebern. Obwohl die eine Gruppe bei geringerer Kraft und vielen Wiederholungen trainiert hatte und die andere bei nahezu Maximalkraft und wenigen Wiederholungen, war die Zunahme an Muskelmasse und Muskelfasergröße nach einigen Wochen nahezu identisch. Andere Studien wie die von Schoenfeld et al. (2016) weisen jedoch darauf hin, dass hohe Gewichte zu einer höheren Zunahme an Muskelmasse führt.[5] Aufgrund des hohen metabolischen Stresses bei leichtem Gewicht und hohen Wiederholungszahlen ist es bei hohem Gewicht und wenigen Wiederholungen oft einfacher den Muskel "bis zur Erschöpfung" zu belasten.
KAATSU-Training
Als eine effektive Methode zur schnellen Muskelhypertrophie – vor allem bei Senioren und Untrainierten – wurde das zunächst in Japan verwendete KAATSU-Training (auf Japanisch die Abkürzung von „Widerstandstraining kombiniert mit Blutfluss-Beeinträchtigung“) entwickelt.[6] Hierbei wird unter Verwendung einer Blutdruckmanschette der lokale Abtransport der Ermüdungsstoffe, vor allem der entstehenden Milchsäure erschwert, wodurch es schneller zu einer Erschöpfung kommt. Dieses Training hat trotz anfänglicher Befürchtungen keine negativen Nebenwirkungen.[7]
Muskelhyperplasie
Unter Muskelhyperplasie versteht man eine Faservermehrung innerhalb der Muskeln.
Dieser Effekt ist bislang nicht beim Menschen nachweisbar. Bei einigen Tieren wie der Maus konnte man ihn in Laborversuchen mit synthetischen Myostatin-Antikörpern belegen. Einige Forscher gehen davon aus, dass sich der Effekt auf andere Säugetiere übertragen lässt.[8]
Ernährung
Beim Muskelaufbau spielt die Einnahme von Eiweiß eine wichtige Rolle. Entgegen einem weitverbreiteten Gerücht, wonach tierisches Eiweiß gegenüber pflanzlichem Eiweiß besser beim Muskelaufbau abschneiden soll, konnten Wissenschaftler keinerlei Belege dafür finden.[9] Vielmehr spielt für den Muskelaufbau die Wertigkeit des Eiweißes eine entscheidende Rolle und diese ist bei entsprechender Kombination (z. B. Weizeneiweiß wie Seitan plus Sojaeiweiß wie Tofu) sogar höher als die von Muskelfleisch oder Eiern. Ein weiteres Gerücht betrifft Sojaproteine, die mit 85 eine hohe biologische Wertigkeit besitzen, die angeblich jedoch in hohen Mengen Östrogen-ähnliche Substanzen enthalten; tatsächlich sind diese Mengen jedoch sehr gering und in Studien konnten diesen keine schädliche Wirkung nachgewiesen werden.[10]
Schoenfeld et al. (2013) haben in einer Metastudie keinen Zusammenhang zwischen dem Zeitpunkt der Einnahme von Eiweiß und dem Trainingserfolg feststellen können; demnach kommt es beim Muskelaufbau einzig auf die Tagesmenge an Proteinen an und keineswegs auf den Zeitpunkt.[11] Früher noch gängige Empfehlungen, wonach Proteine am besten binnen einer Stunde vor oder nach dem Training (Anabolic- oder Metabolic Window) einzunehmen sind, wurden damit weitgehend widerlegt.
Literaturnachweise
- Ji-Guo Yu: Re-Evaluation Of Exercise-Induced Muscle Soreness – An Immunohistochemical and Ultrastructural Study. ISBN 91-7305-503-4 (PDF-Datei)
- Fawzi Kadi, Peter Schjerling, Lars L. Andersen, Nadia Charifi, Jørgen L. Madsen, Lasse R. Christensen, Jesper L. Andersen: The effects of heavy resistance training and detraining on satellite cells in human skeletal muscles. In: The Journal Of Physiology. doi:10.1113/jphysiol.2004.065904
- U. Proske, D. L. Morgan: Muscle damage from eccentric exercise: mechanism, mechanical signs, adaptation and clinical applications. In: The Journal Of Physiology. (online)
- Thomas J. Hawke, Daniel J. Garry: Myogenic satellite cells: physiology to molecular biology. (PDF-Datei)
- MacDougall u. a.: The time course for elevated muscle protein synthesis following heavy resistance exercise. In: Can J Appl Physiol. (4) 20. Dezember 1995, S. 480–486. PMID 8563679
- Fadia Haddad, Gregory R. Adams: Acute cellular and molecular responses to resistance exercise. In: J Appl Physiol. Vol. 93, Issue 1, 1. Juli 2002, S. 394–403. (online)
- Michael J. Rennie: How muscles know how to adapt. In: The Journal Of Physiology. 15. August 2001, PMC 2278760 (freier Volltext)
- Vladimir M. Zatsiorsky: Krafttraining. Praxis und Wissenschaft. April 1996, ISBN 3-89124-333-2.
- Markus Gerd Heinichen: Insulin-like Growth Factor-1, Mechano Growth Factor und Myosin Schwerketten Transformation beim Krafttraining. 2005. (PDF-Datei)
- M. S. Clarke, D. L. Feeback: Mechanical load induces sarcoplasmic wounding and FGF release in differentiated human skeletal muscle cultures. In: FASEB J. 10(4), 1996, S. 502–509.
- K. Hakkinen, P. V. Komi: EMG changes during strength training and detraining. In: Med. Sci. Sports Exerc. 15(6), 1983, S. 455–460.
- R. J. Maughan: Relationship between muscle strength and muscle Cross-sectional area. Implications for training. In: Sports Med. 1(4), 1984, S. 263–269.
- M. J. McDonagh, C. T. Davies: Adaptive response of mammalian skeletal muscle to exercise with high loads. In: Eur J Appl Physiol. 52(2), 1984, S. 139–155.
- J. D. MacDougall, G. R. Ward, D. G. Sale, J. R. Sutton: Biochemical adaptation of human skeletal muscle to heavy resistance training and immobilization. In: J Appl Physiol. 43(4), 1977, S. 700–703.
- K. Nosaka, P. M. Clarkson: Muscle damage following repeated bouts of high force eccentric exercise. In: Med. Sci. Sports Exrc. 27(9) 1995, S. 1263–1269.
- L. L. Smith, M. G. Fuylmer, D. Holbert, M. R. McCammon, J. A. Houmard, D. D. Frazer, E. Nsien, R. G. Israel: The impact of repeated bout of eccentric exercise on muscular strength, muscle soreness and creatine kinase. In: Br J Sp Med. 1994; 28(4)
- T. C. Chen, Taipei Physical Education College, und S. S. Hsieh, FACSM: The effects of a seven-day repeated eccentric training on recovery from muscle damage. In: Med. Sci. Sports Exrc. 31(5 Supp) 1999, S. S71.
- G. P. Bates: The relationship between duration of stimulus per day and the extent of hypertrophy of slow-tonic skeletal muscle in the fowl, Gallus gallus. In: Comp Biochem Physiol Comp Physiol. 106(4), Dezember 1993, S. 755–758.
- J. R. McLester, P. Bishop, M. Guilliams: Comparison of 1 and 3 day per week of equal volume resistance training in experienced subjects. In: Med. Sci. Sports Exrc. 31(5 Supp) 1999, S. S112.
- M. A. Curto, M. M. Fisher: The effect of single vs. Multiple sets of resistance exercise on strength in trained males. In: Med. Sci. Sports Exrc. 31(5 Supp) 1999, S. S114.
- H. Ohmori, S. Shimegi, K. Fujimoto, Y. Kano, M. Inaki, M. Myamaru, S. Katsuta: The effect of strength training is potentially memorized and reinforced by retraining. In: Med. Sci. Sports Exrc. 31(5 Supp), 1999, S. S327.
- J. N. Phelan, W. J. Gonyea: Effect of radiation on satellite cell activity and protein expression in overloaded mammalian skeletal muscle. In: Anat. Rec. 247, 1997, S. 179–188.
- J. D. Rosenblatt, D. J. Parry: Gamma irradiation prevents compensatory hypertrophy of overloaded extensor digitorum longus muscle. In: J. Appl. Physiol. 73, 1992, S. 2538–2543.
- J. D. Rosenblatt, D. Yong, D. J. Parry: Satellite cell activity is required for hypertrophy of overloaded adult rat muscle. In: Muscle Nerve. 17, 1994, S. 608–613.
- Y. Liu, L. Gampert, O. Prokopchuk, J. M. Steinacker: Satellitenzellaktivierung beim Krafttraining. In: Deutsche Zeitschrift für Sportmedizin. Jahrgang 58, Nr. 1 (2007). (PDF-Datei)
Einzelnachweise
- Claudio Viecelli, David Aguayo: May the Force and Mass Be With You—Evidence-Based Contribution of Mechano-Biological Descriptors of Resistance Exercise. In: Frontiers in Physiology. Band 12, 2022, ISSN 1664-042X, S. 2449, doi:10.3389/fphys.2021.686119 (frontiersin.org [abgerufen am 5. Januar 2022]).
- vgl. Egner, Bruusgaard et al.(2013): A cellular memory mechanism aids overload hypertrophy in muscle long after an episodic exposure to anabolic steroids, in: Journal of Physiology 591 (24), 6221–6230.
- Arnd Krüger (2019): Muskelgedächtnis, in: Leistungssport 49(3), 32.
- R. W. Morton, S. Y. Oikawa, C. G. Wavell, N. Mazara, C. McGlory, J. Quadrilatero, B. L. Baechler, S. K. Baker, S. M. Phillips: Neither load nor systemic hormones determine resistance training-mediated hypertrophy or strength gains in resistance-trained young men. In: Journal of applied physiology. Band 121, Nummer 1, Juli 2016, S. 129–138, doi:10.1152/japplphysiol.00154.2016, PMID 27174923, PMC 4967245 (freier Volltext).
- Brad J. Schoenfeld, Jacob M. Wilson, Ryan P. Lowery, James W. Krieger: Muscular adaptations in low- versus high-load resistance training: A meta-analysis. In: European Journal of Sport Science. Band 16, Nr. 1, 2016, ISSN 1536-7290, S. 1–10, doi:10.1080/17461391.2014.989922, PMID 25530577.
- Arnd Krüger: KAATSU-Training. In: Leistungssport. 41(2011)5, S. 38–41.
- J. P. Loenneke, R. S. Thiebaud, T. Abe: Does blood flow restriction result in skeletal muscle damage? A critical review of available evidence. In: Scand J Med Sci Sports. 20. März 2014. doi:10.1111/sms.12210.
- Se-Jin Lee: Regulation of muscle mass by myostatin. In: Annu. Rev. Cell Dev. Biol. 2004. 21. April 20, 2004, S. 61–86.
- K. M. Mangano, S. Sahni, D. P. Kiel, K. L. Tucker, A. B. Dufour, M. T. Hannan: Dietary protein is associated with musculoskeletal health independently of dietary pattern: the Framingham Third Generation Study. In: The American journal of clinical nutrition. Band 105, Nummer 3, März 2017, S. 714–722, doi:10.3945/ajcn.116.136762, PMID 28179224, PMC 5320406 (freier Volltext).
- Hamilton-Reeves et al. (2010), PMID 19524224.
- Schoenfeld et al., (2013), doi:10.1186/1550-2783-10-53