Molekülerkennung
Der Begriff Molekülerkennung oder molekulare Erkennung bezeichnet eine nicht kovalente Interaktion zwischen zwei oder mehr Molekülen, die spezifisch für genau diese Kombination von Molekülen ist. Oftmals gibt es bei dieser Interaktion ein größeres Wirtsmolekül, welches mit einem Gastmolekül interagiert. Die molekulare Erkennung erfolgt nach dem Schlüssel-Schloss-Prinzip.[2]
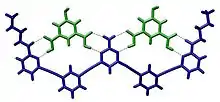
Arten von Wechselwirkungen
Es gibt eine Vielzahl von Wechselwirkungen, die bei der Molekülerkennung eine Rolle spielen. Dies sind unter anderem Wasserstoffbrückenbindungen, Van-de-Waals-Wechselwirkungen, Komplexbildungsreaktionen, Hydrophobieeffekte, Pi-Komplexe, Halogenbindungen oder Elektrostatische Wechselwirkungen.[3] Zusätzlich zu diesen direkten Wechselwirkungen können auch Lösungsmitteleffekte eine entscheidende Rolle spielen.[4][5]
Statisch oder dynamisch

Molekülerkennung lässt sich einteilen in statische Molekülerkennung und dynamische Molekülerkennung. Die statische Molekülerkennung ist dabei eine 1:1 Verbindung von einem Wirtsmolekül und einem Gastmolekül zu einem Wirts-Gast-Komplex.
Bei der dynamischen Molekülerkennung führt die Bindung eines ersten Gastmoleküls an eine erste Bindungsstelle zu einer Veränderung einer zweiten Bindungsstelle.[6] Bei positiven allosterischen Systemen verstärkt die Bindung des ersten Gastes die Bindung des zweiten, bei negativen wird sie geschwächt. Die dynamische Molekülerkennung kann die Fähigkeit, zwischen konkurrierenden Zielmolekülen zu unterscheiden, verbessern. Dynamische Molekülerkennungen werden auch für den Einsatz in chemischen Sensoren und molekularen Maschinen untersucht.
Komplexität der Molekülerkennung
Eine im Jahr 2011 durchgeführte Studie zur molekularen Simulation von Molekülerkennungsprozessen zeigte, dass schon für kleine Moleküle, wie etwa Kohlenhydrate, der Erkennungsprozess nicht vorhergesagt werden kann, obwohl die Stärken aller Wasserstoffbrückenbindungen bekannt waren.[7]
Vorkommen
Biologische Systeme
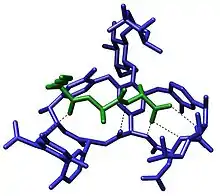
Die Molekülerkennung spielt eine sehr wichtige Rolle in biologischen Systemen. Zum Beispiel in Rezeptor-Ligand-, Antigen-Antikörper-, DNA-Protein- und Enzym-Substrat-Wechselwirkungen. Ein wichtiges Beispiel für Molekülerkennung liefert das Antibiotikum Vancomycin, welches selektiv mittels fünf Wasserstoffbrückenbindungen an Peptide mit endständigem D-Alanyl-D-Alanin in Bakterienzellen bindet. Durch die Verbindung mit dem Vancomycin werden die Peptide für den Aufbau der Zellwand unbrauchbar.
Supramolekulare Systeme
Inzwischen konnte gezeigt werden, dass künstliche supramolekulare Systeme so konstruiert werden können, dass sie eine Molekülerkennung aufweisen. Eines der frühesten Beispiele solcher Systeme sind Kronenether, welche nur an bestimmte Kationen binden.
Weblinks
- Molecular Recognition. (Spezialausgabe über Molekülerkennung des International Journal of Molecular Sciences; Englisch)
Einzelnachweise
- Christopher Bielawski, Yuan-Shek Chen, Peng Zhang, Peggy-Jean Prest, Jeffrey S. Moore: A modular approach to constructing multi-site receptors for isophthalic acid. (Free full text) In: Chemical Communications. Nr. 12, 1998, S. 1313–4. doi:10.1039/a707262g.
- Samuel H. Gellman: Introduction: Molecular Recognition. In: Chemical Reviews. 97, Nr. 5, 1997, S. 1231–1232. doi:10.1021/cr970328j. PMID 11851448.
- I Cosic: Macromolecular bioactivity: is it resonant interaction between macromolecules?—theory and applications. In: IEEE transactions on bio-medical engineering. 41, Nr. 12, 1994, S. 1101–14. doi:10.1109/10.335859. PMID 7851912.
- Riccardo Baron, Piotr Setny, J. Andrew McCammon: Water in Cavity-Ligand Recognition. In: Journal of the American Chemical Society. 132, Nr. 34, 2010, S. 12091–12097. doi:10.1021/ja1050082. PMID 20695475. PMC 2933114 (freier Volltext).
- Riccardo Baron, J. Andrew McCammon: Molecular Recognition and Ligand Binding. In: Annual Review in Physical Chemistry. 64, 2013, S. 151–175. doi:10.1146/annurev-physchem-040412-110047. PMID 23473376.
- Seiji Shinkai, Masato Ikeda, Atsushi Sugasaki, Masayuki Takeuchi: Positive allosteric systems designed on dynamic supramolecular scaffolds: toward switching and amplification of guest affinity and selectivity. In: Accounts of chemical research. 34, Nr. 6, 2001, S. 494–503. doi:10.1021/ar000177y. PMID 11412086.
- Jörg Grunenberg: Complexity in molecular recognition. In: Physical Chemistry Chemical Physics. Band 13, Nr. 21, 18. Mai 2011, S. 10136–10146, doi:10.1039/C1CP20097F.
- James R. Knox, R. F. Pratt: Different modes of vancomycin and D-alanyl-D-alanine peptidase binding to cell wall peptide and a possible role for the vancomycin resistance protein. (Free full text) In: Antimicrobial agents and chemotherapy. 34, Nr. 7, Juli 1990, S. 1342–7. doi:10.1128/AAC.34.7.1342. PMID 2386365. PMC 175978 (freier Volltext).