Mangan(II)-hydroxid
Mangan(II)-hydroxid ist eine anorganische chemische Verbindung des Mangans aus der Gruppe der Hydroxide.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
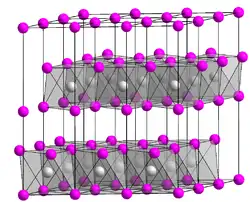 | |||||||||||||||||||
| _ Mn2+ _ OH− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Mangan(II)-hydroxid | ||||||||||||||||||
| Verhältnisformel | Mn(OH)2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer bis pinker Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 88,95 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
3,258 g·cm−3[1] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Mangan(II)-hydroxid fällt bei der Reaktion von Mangan(II)-salzlösungen mit Alkalilaugen unter Luftabschluss als gelblicher Niederschlag aus der Lösung aus.[5] So zum Beispiel durch Reaktion von Mangan(II)-chlorid-Tetrahydrat mit einer Kaliumhydroxid-Lösung.[2]
Eigenschaften
-hydroxid.jpg.webp)
Mangan(II)-hydroxid ist ein weißer bis pinker Feststoff[1], der praktisch unlöslich in Wasser ist. Er ist stabil, wenn er frei von Alkalihydroxiden und amorphen Anteilen ist. Ansonsten färbt er sich an Luft schnell braun (Bildung von Mangan(III)- und Mangan(IV)-oxidhydraten).[3] Es besitzt eine hexagonale Kristallstruktur isotyp zu der von Cadmiumhydroxid mit der Raumgruppe P3m1 (Raumgruppen-Nr. 164) (a = 334 pm, c = 468 pm).[2] Er kommt jedoch auch in einer orthorhombischen Modifikation mit der Raumgruppe Pbnm (Nr. 62, Stellung 3) vor.[3]
Einzelnachweise
- Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. Taylor & Francis US, 2011, ISBN 1-4398-1462-7, S. 264 (eingeschränkte Vorschau in der Google-Buchsuche).
- Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1581.
- Roger Blachnik (Hrsg.): Taschenbuch für Chemiker und Physiker. Band III: Elemente, anorganische Verbindungen und Materialien, Minerale. begründet von Jean d’Ans, Ellen Lax. 4., neubearbeitete und revidierte Auflage. Springer, Berlin 1998, ISBN 3-540-60035-3, S. 568 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9, S. 1484.